微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 在反应:2A+B?3C+4D中,所表示的反应速率最快的是( )
A.v(A)=0.4mol?L-1?s-1
B.v(B)=0.3mol?L-1?s-1
C.v(C)=1.2mol?L-1?s-1
D.v(D)=0.8mol?L-1?s-1
参考答案:把所有物质的反应速率都换算成B的反应速率.
A、v(A)=0.4mol?L-1?s-1 ,v(B)=0.2mol?L-1?s-1.
B、v(B)=0.3mol?L-1?s-1.
C、v(C)=1.2mol?L-1?s-1,v(B)=0.4mol?L-1?s-1.
D、v(D)=0.8mol?L-1?s-1,v(B)=0.2mol?L-1?s-1.
所以反应速率最大的是C,故选C.
本题解析:
本题难度:一般
2、选择题 影响化学反应速率的因素有多方面,如浓度、压强、温度、催化剂等。下列有关说法不正确的是
[? ]
A.增大压强不一定能加快反应速率
B.增大浓度能增加反应体系中活化分子的百分数
C.升高温度能增加反应物分子之间的有效碰撞次数
D.催化剂能改变反应的活化能
参考答案:B
本题解析:
本题难度:一般
3、选择题 将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应,?2A(g) + B(g)  ?2C(g) 若经 2 s 后测得 C 的浓度为 0.6 mol/L ;
?2C(g) 若经 2 s 后测得 C 的浓度为 0.6 mol/L ;
现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol/(L ・ s)?②用物质 B 表示的反应的平均速率为 0.6 mol/(L ・ s)?③ 2 s 时物质 A 的转化率为 70 %?④ 2 s 时物质 B 的浓度为 0.7 mol/L 其中正确是(?)。
A.①③
B.①④
C.②③
D.③④
参考答案:B
本题解析:2A(g) + B(g)  ?2C(g)
?2C(g)
初始:4 mol? 2 mol? 0 mol
△n:? 1.2mol? 0.6mol? 1.2mol
2s:? 2.8mol? 1.4mol? 1.2mol
本题难度:一般
4、实验题 (15分)氰化物有剧毒,氰化电镀会产生大量含氰化物的废水,该电镀含氰废水中的氰化物主要是以CN一和[Fe(CN)6]3-两种形式存在。研究表明可采用双氧水氧化法处理电镀含氰废水。某化学兴趣小组模拟双氧水氧化法探究有关因素对该破氰反应速率的影晌(破氰反应是指氧化剂将CN-氧化的反应)。
【查阅资料】
①Cu2+可作为双氧水氧化法废水处理过程中的催化剂;
②Cu2十在偏碱性条件下对双氧水分解影响较弱,可以忽略不计;
③[Fe(CN)6]3-较CN一难被双氧水氧化,pH越大,[Fe(CN)6]3-越稳定,越难被氧化。
[实脸设计]
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
实验编号
| 实验目的
| 初始pH
| 废水样品体积mL
| CuSO4溶液的体积/mL
| 双氧水溶液的体积/mL
| 蒸馏水的体积mL
|
①
| 为以下实验作参考
| 7
| 60
| 10
| 10
| 20
|
②
| 废水的初始pH对破氰反应速率的影响
| 12
| 60
| 10
| 10
| 20
|
③
|
|
|
|
|
| 10
|
【数据处理]
实验测得含氰废水中的总氰浓度(以CN一表示)随时间变化关系如下图所示。

(2)实验①中20――60 min时间段反应速率v(CN-)= ____mol・L-1?min-1。
【解释和给论]
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是______
(填一点即可)。
在偏碱性条件下,含氰废水中的CN一最终被双氧水氧化为HCO3- ,同时放出NH3,试写出该反应的离子方程式:
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实脸并验证上述结论,完成下表中内容。
(己知:废水中的CN一浓度可用离子色谱仪测定)
实验步骤(不要求写出具体操作过程)
| 预期实验现象和结论
|
|
|
参考答案:(1)(5分,第1空2分,后面4个空共3分,只要填错1个均给0分)
实验编号
实验目的
初始pH
废水样品体积/mL
CuSO4溶液的体积/mL
双氧水溶液的体积/mL
蒸馏水的体积/mL
③ 91ExAM.org
双氧水的浓度对破氰反应速率的影响
7
60
10
20
(2)0.0175(2分)
(3)初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用
(或初始pH增大,[Fe(CN)6]3- 较中性和酸性条件下更稳定,难以氧化)(2分)
CN?+H2O2+H2O==NH3↑+HCO3?(2分)
(4)(每空2分)
实验方案(不要求写出具体操作过程)
预期实验现象和结论
分别取等体积、等浓度的含氰废水于甲、乙两支试管中,再分别加入等体积、等浓度的双氧水溶液,只向甲试管中加入少量的无水硫酸铜粉末,用离子色谱仪测定相同反应时间内两支试管中的CN?浓度
相同时间内,若甲试管中的CN?浓度小于乙试管中的CN?浓度,则Cu2+ 对双氧水破氰反应起催化作用;若两试管中的CN?浓度相同,则Cu2+ 对双氧水破氰反应不起催化作用
本题解析:(1)由于该实验是在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,以实验①为参考,实验②是调节废水的pH来测定pH对实验的影响,所以实验③是控制浓度双氧水溶液的用量,测定对实验速率的影响。与实验①比较,只有双氧水的体积不同,其余都相同。即:初始pH是7;废水样品体积60ml,CuSO4溶液的体积10mL,双氧水溶液的体积20mL,蒸馏水的体积是10mL.(2)实验①中20――60 min时间段反应速率v(CN-)=(1.4mol/L-0.7mol/L)÷40min=0.0175mol・L-1?min-1;(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用(或初始pH增大,[Fe(CN)6]3- 较中性和酸性条件下更稳定,更难以被氧化);在偏碱性条件下,含氰废水中的CN一最终被双氧水氧化为HCO3- ,同时放出NH3。则根据电子守恒、电荷守恒及原子守恒,可得该反应的离子方程式是CN?+H2O2+H2O==NH3↑+HCO3?;(4)分别取等体积、等浓度的含氰废水于甲、乙两支试管中,再分别加入等体积、等浓度的双氧水溶液,只向甲试管中加入少量的无水硫酸铜粉末,用离子色谱仪测定相同反应时间内两支试管中的CN?浓度,相同时间内,若甲试管中的CN?浓度小于乙试管中的CN?浓度,则Cu2+ 对双氧水破氰反应起催化作用;若两试管中的CN?浓度相同,则Cu2+ 对双氧水破氰反应不起催化作用。
考点:考查化学反应速率的计算、化学实验方案的设计、评价及原因控制的知识。
本题难度:困难
5、选择题 t℃时,在容积为2 L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示。下列说法不正确的是
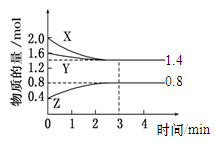
A.0~3 min,X的平均反应速率v(X)=0.2 mol・L-1・min-1
B.发生反应的方程式可表示为:3X(g)+Y(g)  2Z(g)
2Z(g)
C.保持其他条件不变,增大压强,平衡向正反应方向移动
D.温度不变,增大X的浓度,该反应的平衡常数不变
参考答案:A
本题解析:A项由图可知,在3min内X的物质的量变化量为2.0mol-1.4mol=0.6mol,故v(X)=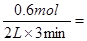 0.1mol・L-1・min-1,错误;B项由图可知,X、Y的物质的量减小,为反应物,△n(X)=2.0mol-1.4mol=0.6mol,△n(Y)=1.6mol-1.4mol=0.2mol,Z的物质的量增大,为生成物,△n(Z)=0.8mol-0.4mol=0.4mol,故X、Y、Z的化学计量数之比为0.6mol:0.2mol:0.4mol=3:1:2,反应最后各物质的物质的量不变,为可逆反应,故该反应为3X(g)+Y(g)?2Z(g),正确;C项根据反应“3X(g)+Y(g)?2Z(g)”,保持其他条件不变,增大压强,平衡向正反应方向移动,正确;D项平衡常数只与温度有关,温度不变,平衡常数不变,正确。
0.1mol・L-1・min-1,错误;B项由图可知,X、Y的物质的量减小,为反应物,△n(X)=2.0mol-1.4mol=0.6mol,△n(Y)=1.6mol-1.4mol=0.2mol,Z的物质的量增大,为生成物,△n(Z)=0.8mol-0.4mol=0.4mol,故X、Y、Z的化学计量数之比为0.6mol:0.2mol:0.4mol=3:1:2,反应最后各物质的物质的量不变,为可逆反应,故该反应为3X(g)+Y(g)?2Z(g),正确;C项根据反应“3X(g)+Y(g)?2Z(g)”,保持其他条件不变,增大压强,平衡向正反应方向移动,正确;D项平衡常数只与温度有关,温度不变,平衡常数不变,正确。
本题难度:一般