微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量。在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ。下列关系式中正确的是?
A.Q1+ Q2<2Q3
B.Q1+ Q2>2Q3
C.Q1+ Q2<Q3
D.Q1+ Q2>Q3
参考答案:A
本题解析:
本题从微观的角度考查反应热的计算。在化学反应中,断键需要吸热,而形成新的化学键时则会放出能量。氢气在氯气中燃烧属于放热反应,化学方程式为: 所以反应中放出的能量为:2Q3-Q1+ Q2,因此Q1+ Q2< 2Q3,即选项A符合题意。
所以反应中放出的能量为:2Q3-Q1+ Q2,因此Q1+ Q2< 2Q3,即选项A符合题意。
本题难度:一般
2、选择题 下列物质不能导电的是()
A.氢氧化钠溶液
B.醋酸溶液
C.熔融氯化钾
D.FeSO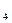 晶体
晶体
参考答案:D
本题解析:物质是否导电可从①物质是否存在着带电粒子,②物质内带电粒子能否在外电场作用下定向移动来判断。据此,金属、电解质熔融状态或其水溶液可导电。
本题难度:一般
3、选择题 下列有关化学能与热能的说法正确的是( )
A.铝热反应属于吸热反应
B.若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应
C.H2→H+H的变化需要吸收能量
D.凡经加热而发生的化学反应都是吸热反应
参考答案:A、铝热反应属于放热反应,故A错误;
B、反应的反应物的总能量大于生成物的总能量为放热反应,反应的反应物的总能量小于生成物的总能量为吸热反应,故B错误;
C、H2→H+H的变化断裂了H-H共价键,断裂化学键需要吸收能量,故C正确;
D、一个反应是吸热反应还是放热反应取决于反应物总能量和生成物总能量的相对大小,与反应的条件无关,有些放热反应也需要加热,如燃烧反应,故D错误;
故选:C.
本题解析:
本题难度:简单
4、选择题 根据下图提供的信息,下列所得结论不正确的是(?)
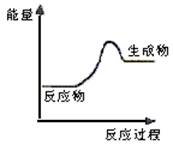
A.该反应为吸热反应
B.该反应一定有能量转化成了化学能
C.反应物比生成物稳定
D.因为生成物的总能量高于反应物的总能量,所以该反应不需要加热
参考答案:D
本题解析:根据图像可知,反应物的能量低于生成物的能量,因此是吸热反应。但反应是放热还是吸热,与反应条件无关系,所以选项D是错误的,答案选D。
本题难度:简单
5、选择题 已知25℃、101 kPa下,1mol石墨与1mol金刚石充分燃烧时
C(石墨)+O2(g)=CO2(g) 放出393.51 kJ的热量
C(金刚石)+O2(g)=CO2(g) 放出395.41 kJ的热量
金刚石和石墨均是由许多碳原子结合成的单质。据此判断,下列说法正确的是
[? ]
A.金刚石比石墨稳定
B.石墨比金刚石稳定
C.石墨转化为金刚石为放热反应
D.金刚石和石墨中所含化学键类型不同
参考答案:B
本题解析:
本题难度:一般