微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将1.15 g钠和0.4 g硫粉迅速混合,并放在石棉网上加热,反应后的固体可能是(?)
A.硫与硫化钠
B.氧化钠与硫化钠
C.过氧化钠与硫化钠
D.硫化钠
参考答案:C
本题解析:硫与钠反应的化学方程式为S+2Na====Na2S,从方程式可得钠与硫反应时的质量比是46∶32,1.15 g钠需要0.8 g硫,现只有0.4 g硫,金属钠过量。过量的金属钠在空气中燃烧生成过氧化钠,所以产物有硫化钠和过氧化钠。
本题难度:简单
2、计算题 KOH和KHCO3固体的混合物25.6 g,于250 ℃进行煅烧,冷却后混合物质量损失了4.9 g。
(1)求起始混合物的百分组成。
(2)若混合物的质量损失改为2.1 g,这时起始混合物的百分组成又是多少?
参考答案:21.875%和78.125%;45.6%和54.4%。
本题解析:用“差量法”判断谁过量。
假设25.6 g混合物是由KOH和KHCO3恰好完全反应的质量比混合而成的,则

 K2CO3+H2O?差量
K2CO3+H2O?差量
156? 18
25.6 g? x
经计算,求得理论差量x="2.95" g。
题目中,第一种情况实际差量>2.95 g,为KHCO3过量。由“钾守恒”,残留的固体25.6 g-4.9 g="20.7" g为K2CO3,则通过列二元方程组,可求得KOH和KHCO3固体各自的质量。题目中,第二种情况实际差量<2.95 g,为KOH过量,由方程式运算可直接求得KHCO3的质量。
本题难度:简单
3、选择题 2.1g平均相对分子质量为7.2的CO和H2组成的混合气体在足量O2中充分燃烧后,将产生的气体立即通入到足量Na2O2固体中,固体增加的质量是
A.2.1 g
B.3.6 g
C.7.2 g
D.无法计算
参考答案:A
本题解析:CO和氢气燃烧的生成物分别是CO2和H2O,CO2和H2O被过氧化钠吸收又生成氧气,所以固体增加的质量就相当于是原混合气的质量,因此答案选A。
本题难度:一般
4、填空题 用A、B两种常见化合物组成混合物,A、B的焰色反应均为黄色,其相互转化关系如下图(其他物质略去)。
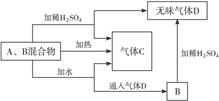
根据以上关系,完成下列问题:
(1)写出A、B、C、D的化学式:
A_____________________________________,
B_____________________________________,
C_____________________________________,
D_____________________________________。
(2)写出混合物与水反应的化学方程式:___________________________________________。
(3)加热后,若只得到一种固体化合物,则A与B的质量之比的最大值为___________。
参考答案:(1)Na2O2? NaHCO3? O2? CO2
(2)2Na2O2+2H2O====4NaOH+O2↑
NaOH+NaHCO3====Na2CO3+H2O
(3)
本题解析:(3)加热后,若只得到一种固体化合物,则只能是Na2CO3。求A与B质量之比的最大值,即是求当B完全分解后生成的CO2与A恰好完全反应生成Na2CO3时二者质量的比值。
由反应关系可看出:Na2O2―2NaOH―2NaHCO3,即Na2O2与NaHCO3的物质的量之比为1∶2时质量的比值。
本题难度:简单
5、选择题 将一粒钠投入下列溶液中,能产生气体和沉淀的是(? )
A.NaCl
B.BaCl2
C.H2SO4
D.CuCl2
参考答案:D
本题解析:2Na+2H2O====2NaOH+H2↑
2NaOH+CuCl2====Cu(OH)2↓+2NaCl
总反应为2Na+2H2O+CuCl2====Cu(OH)2↓+2NaCl+H2↑
本题难度:简单