微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在阅读资料时,小红发现,儿童从空气中吸入的铅量是成人吸入量的1.6~1.7倍.为了探讨这个现象,她展开了如下的研究.利用所学知识完成以下填空.
(1)课题名称为:______
(2)通过取样分析,得到了下表实验数据:
| 离地面高度(m) | 0.8 | 1.0 | 1.2 | 1.4 | 1.6 | 1.8 | 2.0
空气中铅的浓度(μg/m3)
1.10
0.98
0.91
0.72
0.66
0.54
0.50
|
分析以上实验数据,可以得出的结果是______造成此结果的原因可能是______在走访调查中,小红观察到某乡镇颜料厂排出的废水带有颜色,经鉴定含有铅.为了测定废水中铅的浓度,他设计了如下实验步骤:
废水样品含Pb2+溶液沉淀
(3)步骤中过滤需要的玻璃仪器是______、______和玻璃棒.
(4)步骤中a操作称为______,缺少此操作,测得结果______(填“偏高”、“偏低”、或“无影响”).
(5)通过研究,小红提出了一系列降低铅对环境污染的建议,下列建议中不恰当的事______
A.使用无铅汽油?B.开发新的无铅燃料www.
C.倡导使用铅蓄电池作动力的电动车?D.燃煤电厂、金属冶炼厂的废气经除尘后排放.
参考答案:(1)由(2)所给的图表可知,离地面高度越高,空气含铅量越低.可以得出的结果,离地面越低,含铅量越高.可知课题名称应为近地面不同高度空气含铅量的研究.
故答案为:近地面不同高度空气含铅量的研究.
(2)由所给的图表可知,离地面高度越高,空气含铅量越低.因为离地面越低,含铅量越高,说明铅和铅化合物密度大.
故答案为:铅和铅化合物密度大.
(3)由实验步骤可知,需在烧杯中处理废水,将废水中的铅转化为沉淀,并进行过滤,洗涤烘干,称量含铅沉淀.
故需玻璃仪器有烧杯、漏斗、玻璃棒.
故答案为:烧杯、漏斗.
(4)实验最后需称量过滤洗涤后不溶物,所以称量前应将过滤洗涤后的不溶物烘干.否则含铅不溶物的质量会偏大,测得废水中铅的含量偏高.
故答案为:烘干;偏高.
(5)A.使用无铅汽油,可以减少尾气中含铅废气的排放,故A正确;
B.开发新的无铅燃料,可以减少燃烧后,含铅废气物质的排放,故B正确;
C.铅蓄电池属于铅及氧化铅作电极,废弃的电池会造成对环境的污染,故C错误;
D.燃煤电厂、金属冶炼厂的废气经除尘后排放,可以减少废气中铅的含量,故D正确.
故选:B.
本题解析:
本题难度:简单
2、选择题 关于某无色透明溶液中所含离子的鉴别,下列叙述正确的是
A.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有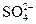
B.通入Cl2后,溶液变为黄色,加入淀粉后溶液变蓝,则原溶液中一定有I-
C.加盐酸,生成的无色无味气体能使饱和的澄清石灰水变浑浊,则原溶液中一定有
D.加入AgNO3溶液产生白色沉淀,则原溶液中一定含有Cl-
参考答案:B
本题解析:A项酸性条件下 可将
可将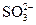 氧化成
氧化成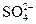 ;C项
;C项 、
、 遇盐酸均可产生CO2;D项Ag2SO4微溶,较浓情况下也能产生白色沉淀。
遇盐酸均可产生CO2;D项Ag2SO4微溶,较浓情况下也能产生白色沉淀。
本题难度:简单
3、选择题 现有两瓶溶液,新制饱和氯水和亚硫酸,下列方法或试剂(必要时可加热)能用于鉴别它们的是:①观察颜色;②石蕊试剂;③品红溶液?(?)
A?①②③? B?只有①③? C?只有②③? D?只有①②
参考答案:A
本题解析:
正确答案:A
①观察颜色,黄绿色的是氯水;②石蕊试剂,先红后褪色的是氯水;③品红溶液,先褪色,加热后又恢复成红色的是亚硫酸。
本题难度:简单
4、选择题 海水淡化方法较多,下列方法中也可以用来进行海水淡化的是
A.过滤法
B.萃取法
C.分液法
D.冰冻法
参考答案:D
本题解析:过滤适用于固体和液体之间的分离,萃取适用于溶质在不同溶剂中的溶解度不同,分液是互不相溶液体之间的分离,所以正确的答案是D。
本题难度:简单
5、选择题 用10mL?0.1mol?L-1?AgNO3溶液恰好可使相同体积的氯化钠、氯化铝和氯化镁三种溶液中的氯离子完全转化为氯化银沉淀,则三种盐溶液的物质的量浓度之比是
A.3:1:2
B.1:3:2
C.6:2:3
D.1:1:1
参考答案:C
本题解析:分析:用10mL?0.1mol?L-1?AgNO3溶液恰好可使相同体积的NaCl、AlCl3、MgCl2三种溶液中的氯离子完全转化为氯化银沉淀,则所生成的沉淀AgCl的物质的量相同,令AgCl的物质的量为1mol,根据氯原子守恒计算n(NaCl)、n(MgCl2)、n(AlCl3),体积相同,浓度之比等于物质的量之比.
解答:相同体积的NaCl、AlCl3、MgCl2三种溶液过量的硝酸银溶液反应,所生成的沉淀AgCl的物质的量相同,令AgCl的物质的量为1mol,根据氯原子守恒,则:
n(NaCl)=n(AgCl)=1mol
n(AlCl3)= n(AgCl)=
n(AgCl)= ×1mol=
×1mol= mol
mol
n(MgCl2)= n(AgCl)=
n(AgCl)= ×1mol=
×1mol= mol
mol
体积相同,浓度之比等于物质的量之比,故c(NaCl):c(AlCl3):c(MgCl2)=1mol: mol:
mol: mol=6:2:3,
mol=6:2:3,
故选C.
点评:本题考查物质的量浓度的有关计算,难度不大,注意利用假设法与守恒进行的计算,可以简化计算过程.
本题难度:简单