微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4・5H2O及CaCO3,步骤如下:
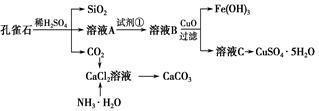
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为________(填代号),检验溶液A中Fe3+的最佳试剂为________(填代号)。
a.KMnO4? b.(NH4)2S? c.H2O2? d.KSCN
(2)由溶液C获得CuSO4・5H2O,需要经过加热蒸发、________、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是___________。
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。若实验过程中有氨气逸出,应选用下列________(填代号)装置回收。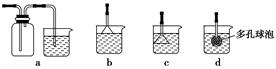
2、填空题 (10分)综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示:
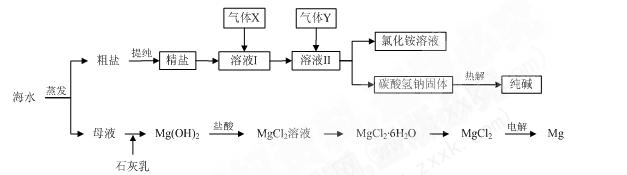 ?
?
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO 3溶液;⑤? ▲?;⑥加适量的盐酸;⑦? ▲?。
3溶液;⑤? ▲?;⑥加适量的盐酸;⑦? ▲?。
(2)溶液Ⅱ中发生反应的化学方程式是:? ▲?。
(3)Mg(OH)2沉淀中因混有Ca(OH)2,可选用? ▲?溶液进行洗涤以除之。
(4)高温灼烧六水 合氯化镁晶体(MgCl2・6H2O)所得固体是氧化镁,试写出该反应的化学方程式? ▲?。
合氯化镁晶体(MgCl2・6H2O)所得固体是氧化镁,试写出该反应的化学方程式? ▲?。
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:? ▲?。
3、填空题 钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率。
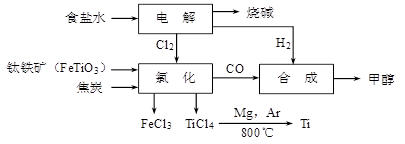
请回答下列问题:
(1)氢写出Ti原子的核外电子排布式______。
(2)写出钛铁矿在高温下与焦炭、氯气反应得到四氯化钛的化学方程式?。
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2・x H2O,再经焙烧制得。水解时需加入大量的水并加热,请结合化学方程式和必要的文字说明原因:?。
(4)由TiCl4→Ti 需要在Ar气中进行,反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于?℃即可。
?
| TiCl4
| Mg
| MgCl2
| Ti
|
熔点/℃
| -25.0
| 648.8
| 714
| 1667
|
沸点/℃
| 136.4
| 1090
| 1412
| 3287
|
?
(5)CH3OH(l)的燃烧热△H=-726.5kJ/mol,请写出甲醇燃烧的热化学方程式?。以甲醇和氧气(或空气)、电解液为Li2CO3和K2CO3的熔融物组成燃料电池,该电池负极反应式为__________________。
由CO和H2合成甲醇的方程式是:CO(g)+2H2(g)= CH3OH(g)。若不考虑生产过程中物质的任何损失,上述产业链中每合成9mol甲醇,至少需额外补充H2?mol。
4、填空题 海洋是资源的宝库,海水中几乎存在所有的天然元素。海洋资源化学就是研究从海洋中提取化学物质的学科,除了研究从海洋中提取常量元素外,还研究从海洋中提取微量元素(浓度小于1mg/L)。
(1)海洋中含量最高的卤素元素在周期表中的位置为?;与其同周期相邻且单质为固体的元素原子的核外电子排布式为?。
(2)海洋中元素含量位于前列的元素有氧、氯、钠、镁、硫,其离子半径从大到小的顺序为?(用离子符号表示),其中形成的化合物中能发生潮解的是?(用电子式表示)。
(3)微量元素铍在海水中主要以Be(OH)+形式存在,其性质与铝元素相似,目前是从绿宝石(主要成分为铍铝硅酸盐Be3Al2Si6O18)中提取,由于铍是航空、电子、汽车等工业不可替代的战略金属材料,因此海水提铍会成为海洋资源化学新的研究方向。请写出:
①铍铝硅酸盐的氧化物形式的化学式:?。
②Be(OH)+与强碱溶液反应的离子方程式:?。
(4)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是?(选填编号)。
a.海水提溴:海水浓缩
 溴蒸气
溴蒸气
 液溴
液溴
b.海水提镁:海滩贝壳
 石灰乳
石灰乳

 MgO
MgO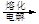 镁
镁
c.海带提碘:海带灼烧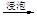
 滤液
滤液 含碘有机溶液
含碘有机溶液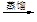 碘晶体
碘晶体
d.海盐提纯:海盐

 精盐
精盐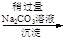
 滤液
滤液
 食盐晶体
食盐晶体
5、实验题 、(12分)钡盐生产中会排出大量的钡泥[主要含有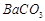 、
、 、
、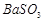 、
、 等]。某化工厂主要生产
等]。某化工厂主要生产 、
、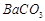 、
、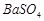 ,现利用钡泥制取
,现利用钡泥制取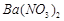 ,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3?(2)Fe3+在pH=3.7时即可水解即沉淀完全)
,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3?(2)Fe3+在pH=3.7时即可水解即沉淀完全)
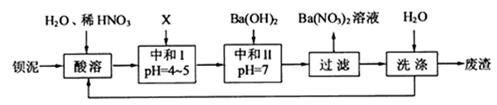
(1)酸溶后溶液中 ,
, 与
与 的反应化学方程式为:
的反应化学方程式为:
?。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,其原因是防止反应速率过快、浓硝酸挥发且易?。
(3)该厂结合本厂生产实际选用的X为?(填化学式);“中和Ⅰ”会使溶液中(填离子符号)?的浓度减少。
(4)从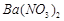 溶液中得到其晶体的分离方法叫?。
溶液中得到其晶体的分离方法叫?。
(5)废渣可直接排放。上述流程中洗涤的目的是?。