��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪G��Q��X��Y��Z��Ϊ�ȵĺ�����������Dz��˽����ǵĻ�ѧʽ����֪��������һ�������¾�������ת����ϵ��δ��ƽ��
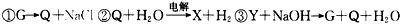
�����ֻ��������ȵĻ��ϼ��ɵ͵��ߵ�˳���ǣ�_________________________________
�ο��𰸣�GYQZX
���������
�����Ѷȣ�һ��
2��ѡ���� ��A��B��C���ֶ�����Ԫ�أ���֪AԪ�ص�ԭ��������������������Ӳ�����BԪ�ص�ԭ������������������Ӳ�����2����CԪ�ص�ԭ������������������Ӳ�?����3������������Ԫ����ɵĻ�����Ļ�ѧʽ�������ǣ�������
A��A3BC4
B��A2��BC4��3
C��A2BC3
D��A2BC4
�ο��𰸣���A��B��C���ֶ�����Ԫ�أ�������ԭ������������18������֪AԪ�ص�ԭ��������������������Ӳ���������A������HԪ�ء�BeԪ�ء�AlԪ�أ�BԪ�ص�ԭ������������������Ӳ�����2��������B������HeԪ�ء�CԪ�ء�SԪ�أ�CԪ�ص�ԭ������������������Ӳ�����3��������C��OԪ�أ�
ABC����Ԫ���γɵĻ���������Ǻ�����������Σ�
A������γɵ��Ǻ�����������Σ��������и�Ԫ�صĻ��ϼ۴�����Ϊ0����������A3BC4�и�Ԫ�صĻ��ϼ۴����Ͳ�Ϊ0����A����
B������γɵ��Ǻ�����������Σ����������ϸû�ѧʽA2��BC4��3����B��ȷ��
C������γɵ��Ǻ�����������Σ�̼�����������ϸû�ѧʽA2BC3����C��ȷ��
D������γɵ��Ǻ�����������Σ�������ϸû�ѧʽA2BC4����D��ȷ��
��ѡA��
���������
�����Ѷȣ�һ��
3������� (1)�����������ʢ�KI ��NH4Cl ��Na2O2 ��O2 ��H2S ��N2 ��CaF2 ��PCl3 ��NaOH����ֻ�������Ӽ�����_________ ��ֻ���м��Թ��ۼ�����__________ ���Ⱥ������Ӽ��ֺ��зǼ��Լ�����__________ �����������ִ��ţ�
(2)д���������ʵĵ���ʽ��Na2O2_____________ ��CCl4______________ �� CO2________________��
(3)�õ���ʽ��ʾ�������ʵ��γɹ��̣� MgCl2 _______________�� H2O2 __________________��
�ο��𰸣���1���٢�? ���ݢ�? ����
��2��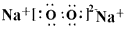 ?��
?�� 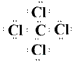 ?��
?��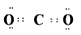
��3�� ?��
?��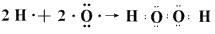
���������
�����Ѷȣ�һ��
4������� ��2008?�Ϻ���23�����ֶ�����Ԫ�ص����ʻ�ṹ��Ϣ���±����������Ϣ�ش��������⣮
| Ԫ�� | A | B | C | D
���ʻ�
�ṹ
��Ϣ
�����µ��ʳʷ�ĩ״���壬�������ۻ���������������ȼ�գ���������������ɫ����
���ʳ��¡���ѹ�������壬������ˮ��ԭ�ӵ�M������7������
��������������ɫ���塢������ǿ�������ڿ�����ȼ�շ�����ɫ�Ļ���
ԭ��������Ӳ���4�����ӣ�����Ϊ�ռ���״���壬���кܸߵ��ۡ��е�
|
��1��BԪ�������ڱ��е�λ����______��д��Aԭ�ӵĵ���ʽ______��
��2��д��C������ˮ��Ӧ�Ļ�ѧ����ʽ______��A��C�γɵĻ���������ˮ����Һ��pH______7������ڡ������ڡ���С�ڡ�����
��3��DԪ����������ᄃ���Ӳ��______�����С��������������______��
��4��A��B��Ԫ�طǽ����Խ�ǿ���ǣ�дԪ�ط��ţ�______��д����֤����һ���۵�һ��ʵ����ʵ______��
�ο��𰸣���1��BԪ�شӡ����塱��֪�Ƿǽ���Ԫ�أ���M������7�������ӡ�֪��ClԪ�أ�λ��Ԫ�����ڱ��������ڢ�A�壬
AԪ�صĵ�����������ȼ�գ���������������ɫ���棬Ӧ��SԪ�أ������ʽΪ
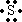
��
�ʴ�Ϊ���������ڢ�A�壻
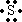
��
��2��C���ʵ���ɫ��Ӧ�ʻ�ɫ����CΪNa��Ϊ���ý�������ˮ���ҷ�Ӧ����NaOH��������
��Ӧ�ķ���ʽΪ2Na+2H2O�T2NaOH+H2��������NaOH����Һ�ʼ��ԣ�PH����7��
�ʴ�Ϊ��2Na+2H2O�T2NaOH+H2�������ڣ���
��3��DԪ������������Ϊ4����Ͽռ���״�ṹ�͡��ܸߵ��ۡ��е㡱Ӧ����CԪ�ػ�SiԪ�أ�
���������ΪSiO2��CO2��SiO2��ԭ�Ӿ��壬Ӳ�ȴ�CO2�Ƿ��Ӿ��壬Ӳ��С��
�ʴ�Ϊ����SiO2��ԭ�Ӿ��壨��С��CO2�Ƿ��Ӿ��壩��
��4��ͬ����Ԫ�ش�����Ԫ�صķǽ���������ǿ���Ƚ�Ԫ�طǽ����Ե�ǿ���ɴ�����֮�����û����⻯����ȶ��ԡ�����������ˮ���������ǿ���ȷ���ȥ�жϣ�
�ʴ�Ϊ��Cl������������Դ�����������Ի��Ȼ����ȶ��Ա�����ǿ��
���������
�����Ѷȣ�һ��
5������� ��H��C��O��Cl��Na����Ԫ�ء�
��1����������Ԫ����ɵĻ�������������ӻ�������(д2��)______________________�����ۻ�������(д2��)______________________��
��2����������Ԫ����ɵĻ�������������ӻ�������(д2��)______________________�����ۻ�������(д2��)______________________��
�ο��𰸣���1��Na2O��NaCl��Na2O2��CO2��CO��CH4��H2O(��д2��) ��2��Na2CO3��NaClO��H2CO3��HClO
����������������Ӽ��Ļ����������ӻ����ȫ���ɹ��ۼ��γɵĻ������ǹ��ۻ����������H��C��O��Cl��Na����Ԫ���У�
��1��������Ԫ����ɵĻ�������������ӻ�������Na2O��NaCl��Na2O2�ȣ����ۻ�������CO2��CO��CH4��H2O�ȡ�
��2��������Ԫ����ɵĻ�������������ӻ�������Na2CO3��NaClO�ȣ����ۻ�������H2CO3��HClO��HClO2��HClO3��HClO4�ȡ�
�����������ǻ���������Ŀ��飬�ѶȲ�����ȷ���ӻ�������ۻ�����ĺ����Լ��뻯ѧ����ϵ�Ǵ���Ĺؼ�������������ѧ���������������ͷ�ɢ˼ά������
�����Ѷȣ���