微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 下列框图题中,已知A、E、F、H是单质,其中只有A是固体,其它都是气体,且H是呈黄绿色;B是最常见液体,G的焰色反应呈黄色,L是白色沉淀,M是红褐色沉淀。部分反应的某些产物未标出。

回答下列问题:
(1)写出化学式:C________、I________;
(2)写出离子方程式:
①D+I溶液:____________________; ②K+H:____________________;
(3)写出化学方程式:①B+C:____________________; ②L→M:____________________;
(4)检验J中的阳离子的最好方法是___________________________________。
参考答案:
(1)Na2O2;HCl
(2)①Fe3O4+8H+==Fe2++2Fe3++H2O;②2Fe2++Cl2==2Fe3++2Cl-;
(3)①2Na2O2+2H2O=4NaOH+O2↑;②4Fe(OH)2+2O2+2H2O==4Fe(OH)3
(4)加入KSCN溶液,溶液呈血红色,证明有Fe3+
本题解析:
本题难度:一般
2、填空题 (14分)A、B、C、D、E、F六种的转化关系如右图,其中A为应用最广泛的金属,氧化物E既能与盐酸反应,又能与NaOH溶液反应。X、Y属于同一周期,且核电荷数相差4。

上述转化中某些反应条件未指出,请回答下列问题:
(1)指出C中的化学键类型:?;D的化学式为?;元素X、Y的原子半径大小顺序是?(用元素符号表示)。
(2)E与NaOH溶液反应的离子方程式为?。
(3)反应A+H2O→C+D的化学方程式为?。
(4)F能促进H2O的电离,其原因是?(用离子方程式表示)。
(5)250C时,将pH=1的盐酸与pH=12的NaOH溶液按体积比1:9混合(混合时溶液体积变化忽略不计),混合均匀后所得溶液的pH=?。
参考答案:每空2分,共14分
(1)共价键;? Fe3O4;? Al>Cl? (各2分)
(2)Al2O3+2OH-=2AlO2-+H2O? (2分)?
(3)Fe + 4H2O(g) =高温=Fe3O4 + 4H2?(2分)
(4) 3Fe3+ + 3H2O  ?Fe(OH)3?+ 3H+?(2分)
?Fe(OH)3?+ 3H+?(2分)
本题解析:A为应用最广泛的金属则为铁,与盐酸反应,生成氯化亚铁和氢气,铁与水反应生成Fe3O4和H2,即 Fe + 4H2O(g) ==Fe3O4 + 4H2?,那么C是氢气,存在的化学键是共价键,B为氯化亚铁,非金属单质X2为氯气,所以Y为Al ,F为氯化铁;氧化物E既能与盐酸反应,又能与NaOH溶液反应,E为Al2O3,Al2O3+2OH -=2AlO2-+H2O。
-=2AlO2-+H2O。
F能促进H2O的电离是因为Fe3+发生了水解,3Fe3+ + 3H2O  ?Fe(OH)3?+ 3H+;(5)中pH=12的NaOH溶液中OH-浓度为0.01mol/l,混合时H+过量,混合后CH+=(0.1×1-0.01×9)/10=0.001 mol/l,PH=3
?Fe(OH)3?+ 3H+;(5)中pH=12的NaOH溶液中OH-浓度为0.01mol/l,混合时H+过量,混合后CH+=(0.1×1-0.01×9)/10=0.001 mol/l,PH=3
(5)? 3?(2分)
本题难度:一般
3、填空题 (10分)已知A、B、C是单质,其中A是金属,各物质间的转化关系如图:
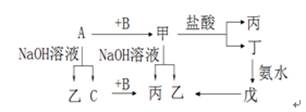
回答下列问题:(1)写出下列物质的化学式(各1分):
(1)A:________、B:________、乙:________、
丙:________、丁:________、戊:________
(2)写出A与NaOH溶液的化学方程式?;
写出丁生成戊的离子方程式?;
参考答案:(1)(各1分)A:Al、B:O2、乙:Na AlO2、丙:H2O、丁:AlCl3、戊:Al(OH)3
(2)(各2分)2Al+2NaOH+2H2O=2Na AlO2+3H2?
Al3++3NH3・H2O=Al(OH)3↓+3NH4+
本题解析:考查铝及其化合物的转化
金属单质A可与NaOH溶液反应,可判定为铝,产物C为氢气,乙为Na AlO2;
铝与单质B化合生成甲,甲即可与盐酸反应,也可与NaOH溶液反应,应是两性氧化物Al2O3的性质,而B为氢气,丙为水,丁为AlCl3,AlCl3与氨水生成戊:Al(OH)3
本题难度:简单
4、推断题 有A、B、C三种物质,每个分子中都各有14个电子,其中A的分子属于非极性分子,且只有非极性键;B的分子也属于非极性分子,但既有非极性键,又有极性键;C的分子属于极性分子。则A的电子式是________,B的结构式是________,C的名称是________。
参考答案: ;H-C≡C-H;一氧化碳
;H-C≡C-H;一氧化碳
本题解析:
本题难度:一般
5、填空题 (共10分)根据下面物质间转换的框图,回答有关问题:

(1)由反应①产生的A、B混合物的工业名称是?。
(2)写出框图中D、E的化学式:D? ?;E??
?;E??
(3)如果2mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积是多少?L,同时反应中转移电子总数是? 。(NA表示阿佛加德罗常数)
。(NA表示阿佛加德罗常数)
(4)请设计一个简单易行的小实验,证明反应⑤是放热反应。实验方法是?
(5)如果A、B混合气体7.8g(平均摩尔质量10g・mol-1),在与G充分反应后,通过足量Na2O2层,可使Na2O2增重?g,并得到O2?m ol。
ol。
参考答案:(1)水煤气(1分)
(2)CO2? NaOH?(各1分)?(3)2.24L? 2NA(各1分)
(4)Na2O2用棉花包裹,放入充满CO2的集气瓶中,棉花燃烧说明是放热反应(直接通CO2于被棉花包裹Na2O2也可,其它合理答案也给分)(3分)
(5)7.8g? 0.39mol?(各1分)
本题解析:略
本题难度:简单