��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1������Ӧ2FeCl3+Fe=3FeCl2��Ƴ�ԭ��ء�____________________
��2���ж���������д���缫��Ӧ��________________________
�ο��𰸣���1��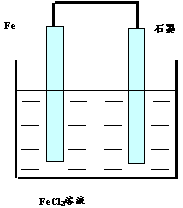
��2��������������Fe-2e-=Fe2+��������ʯī����Fe3++e-=Fe2+
���������
�����Ѷȣ�һ��
2��ѡ���� һ�������Ҵ�����û������������ܼ����ȼ״����Ч�ʸ߳�32��������ܷ�ӦΪ��C2H5OH +3O2�� 2CO2 +3H2O,���ʾ��ͼ����ͼ����������ֵ�ص�˵����ȷ����

A��b��Ϊ��صĸ���
B����ع���ʱ������a���ص��߾������ٵ�b��
C����������ĵ缫��ӦΪ��4H+ ��O2��4e����2H2O
D����״���£�ͨ��5.6LO2����ȫ��Ӧ����0.5mol����ת��
�ο��𰸣�BC
�����������
�����Ѷȣ�һ��
3��ѡ���� ijԭ����ܷ�ӦΪ2Fe3++Fe��3Fe2+������ʵ�ָ÷�Ӧ��ԭ�����
[? ]
A������ΪCu������ΪFe���������ҺΪFeCl3
B������ΪC������ΪFe���������ҺΪFe(NO3)3
C������ΪC������ΪFe���������ҺΪFe2(SO4)3
D������ΪAg������ΪFe���������ҺΪCuSO4
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ��п����������һ�ֿ��Է�����硢�ŵ��װ�ã���طŵ�ʱ�ķ�Ӧԭ���ǣ�Zn+Ag2O+H2O=2Ag+Zn��OH��2��

���ø����ص��c��NO3-��=6mol?L-1��KNO3��Cu��NO3��2�Ļ����Һ500mL����ͨ��һ��ʱ����������ռ���22.4L���壨��״���������صĵ缫��Ϊʯī�缫����
�ش��������⣺
��1����п�������ص�������ӦʽΪ______��
��2���������У�������ӦʽΪ______��������ӦʽΪ______��
��3�������������й�ת�Ƶ�������______��
��4�����õ���Cu������Ϊ______��
��5��ԭ�����Һ��c��K+��Ϊ______��
��6��������Һ��c��H+��______4mol/L��ѡ�������=������������
�ο��𰸣���1����ԭ����У��ϻ��õĽ���пʧ���������������������������������������õ��Ӻ�ˮ��Ӧ�����������������ӣ��缫��ӦʽΪ��Ag2O+H2O+2e-=2Ag+2OH-��
�ʴ�Ϊ��Ag2O+H2O+2e-=2Ag+2OH-��
��2���������У��������������ŵ�����������ˮ��4OH--4e-=2H2O+O2��������������ͭ���ӷŵ�����ͭ����ͭ������ȫ����ʱ�������ӷŵ������������缫��ӦʽΪCu2++2e-=Cu��2H++2e-=H2����4H2O+4e-=2H2+4OH-����
�ʴ�Ϊ��4OH--4e-=2H2O+O2����Cu2++2e-=Cu��2H++2e-=H2����4H2O+4e-=2H2+4OH-����
��3���������У�������ʧ���ӣ������ϵõ��ӣ�����������ת�Ƶ���֮��Ĺ�ϵʽ���㣮
��ת�Ƶ���ΪX��
4OH--4e-=2H2O+O2����
? 4NA? 22.4L
? X?22.4L?
X=4NA
�ʴ�Ϊ4NA��
��4������������ʧȥ4NA ��������22.4L����ת�Ƶ��ӣ������ӵõ�2NA��������22.4L����������ͭ���ӵõ�2NA
��������ͭ���ʣ�
��ͭ���ʵ�������y��
Cu2++2e-=Cu?
?2NA? 64g
? 2NA y
?y=64g��
�ʴ�Ϊ64g��
��5��ͭ��������64g�������ʵ�����1mol����C��Cu2+��=1mol0.5L=2mol/L��c��NO3-��=6mol?L-1��������ӵ����ʵ���Ũ��Ϊz��������Һ�ʵ����ԣ���Һ��������������������ȵã�2C��Cu2+��+C��K+��=c��NO3-��������
C��K+��=c��NO3-��-2C��Cu2+��=2mol/L��
�ʴ�Ϊ��2?mol?L-1 ��
��6������4OH--4e-=2H2O+O2��֪������22.4L������Ҫ����������4mol������2H++2e-=H2��֪������22.4L������Ҫ������2mol��ˮ������������Ӻ����������Ӹ�����ͬ��������Һ�������ӵ����ʵ�����2mol������������Һ�������С������c��H+����2mol0.5L=4mol/L��
�ʴ�Ϊ����
���������
�����Ѷȣ���
5������� �˹��̵���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̡�
I.���һЩ��ѧ���о����ø����ӵ����Ե�SCY�մɣ��ܴ���H+��ʵ�鵪�Ĺ̶�һ��ⷨ�ϳɰ����������˵�����������ת���ʡ��ܷ�ӦʽΪ��N2(g)��3H2(g) 2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________��
2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________��
II.�ݱ�������һ�������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ����Ҫ����ΪNH3����Ӧ�ķ�Ӧ����ʽΪ��2N2(g)��6H2O(g) 4NH3(g)��3O2(g)?��H��Q��
4NH3(g)��3O2(g)?��H��Q��
��1��������Ӧ��ƽ�ⳣ������ʽΪ_______________��
��2��ȡ��ݵ����N2��H2O�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ���������ͬ�ĺ����ܱ������У����¶Ȳ���ͬ������·�����Ӧ����Ӧ��ͬʱ���õ������������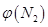 �뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������
�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������
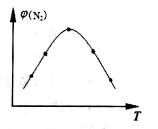
��3����������Ӧ���д���������·���������ͼ��ʾ��a��b��c��d���������У��ܱ�ʾ��Ӧ��ϵ�����仯����_______��ѡ����ĸ���ţ���ͼ�С�H�ľ���ֵΪ1530kJ��mol-1��
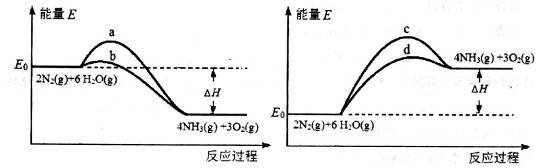
III.Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2(g)��3H2(g) 2NH3(g)?��H����93.0kJ/mol��
2NH3(g)?��H����93.0kJ/mol��
�ش��������⣺
��1�����II�е����ݣ���O2(g)��2H2(g)��2H2O(g)�ġ�H��______________��
��2����һ���¶��£���1molN2��3mol H2����������������ܱ������з�����Ӧ���ﵽƽ��״̬ʱ��������������ʵ���Ϊ2.8mol��
�ٴ�ƽ��ʱ��H2��ת���ʦ�1��______________��
������ͬ�����£�����ʼʱֻ��NH3���ڸ������У��ﵽƽ��״̬ʱNH3��ת����Ϊ��2������1����2��1ʱ������ʼʱNH3�����ʵ���n(NH3)��_____________mol��
�ο��𰸣���.?����1�֣�? N2��6H����6e��===2NH3 ��2�֣�
��.��1��K��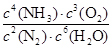 ��2�֣���2������2�֣�?��3��d��2�֣�
��2�֣���2������2�֣�?��3��d��2�֣�
��. ��1����572.0 kJ��mol��1��2�֣���λ��д�����֣�?��2����60%��2�֣�?��2��1�֣�
�����������.����������ʧȥ���ӷ���������Ӧ�������õ����ӣ�������ԭ��Ӧ�����Դ��ܷ�Ӧ�����жϳ�H2�DZ�������Ӧ��������ͨ�룬N2������������ԭ��Ӧ��������ͨ�룬�缫��Ӧʽ��N2+ 6H++6e-��2NH3��
��.��1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ����ʽ��֪���÷�Ӧ��ƽ�ⳣ���ı���ʽK��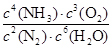 ��
��
��2������������ͬʱ���ڵ���������������¶ȱ仯�Ĺ�ϵ�����ߵı仯��������С���¶����߷�Ӧ���ʼӿ졣�ڴ����У���Ӧ��ͬʱ�䣬�����µ�������δ�ﵽƽ������㣬���¶ȵ����ߣ�����������������¶����߶�������ߵ���ߵ���ij�¶��´ﵽƽ��ĵ㣬֮������㣬����ƽ���ĵ�������������������¶����߶����ͣ���˵�������¶�ƽ��������Ӧ�����ƶ���������ɵ����ķ�Ӧ�Ƿ��ȷ�Ӧ�����˷�Ӧ������ӦΪ���ȷ�Ӧ��
��3�����ݣ�2���Ľ��ۣ���Ӧ�����ȷ�Ӧ��Ӧ��c��d�������Ҵ𰸡�ʹ�ô������Խ��ͷ�Ӧ�Ļ�ܣ����Ӧ��ѡd��
��.��1����Ӧ��N2(g)��3H2(g) 2NH3(g)�ͷ�Ӧ��2N2(g)��6H2O(g)
2NH3(g)�ͷ�Ӧ��2N2(g)��6H2O(g) 4NH3(g)��3O2(g)����������ݸ�˹���ɿ�֪���١�
4NH3(g)��3O2(g)����������ݸ�˹���ɿ�֪���١�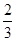 ���ڡ�
���ڡ�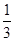 ���õ���ӦO2(g)��2H2(g)��2H2O(g)�����Ը÷�Ӧ�ķ�Ӧ�ȡ�H��2/3������93 kJ��mol��1����1/3��1530 kJ��mol��1����572 kJ��mol��1��
���õ���ӦO2(g)��2H2(g)��2H2O(g)�����Ը÷�Ӧ�ķ�Ӧ�ȡ�H��2/3������93 kJ��mol��1����1/3��1530 kJ��mol��1����572 kJ��mol��1��
��2������N2(g)��3H2(g) 2NH3(g)��֪��4mol�ķ�Ӧ����ȫ��Ӧ�������ʵ�����С2mol����˵����٣�4��2.8��mol��1.2molʱ���μӷ�Ӧ��H2Ϊ1.8mol������������ת����Ϊ
2NH3(g)��֪��4mol�ķ�Ӧ����ȫ��Ӧ�������ʵ�����С2mol����˵����٣�4��2.8��mol��1.2molʱ���μӷ�Ӧ��H2Ϊ1.8mol������������ת����Ϊ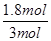 ��100%��60����
��100%��60����
���谱�������ʵ�����x����1����2��1�����Ԧ�2��40%��ƽ��ʱ���������ʵ�����1.2mol���������İ�����x��1.2mol����x��40%��x��1.2mol�����x��2.0mol��
�����Ѷȣ�һ��