��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ��������ʢ��ϡ���ᣬ���γ�ԭ�������Ϊ��������
[? ]
A��
B��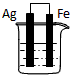
C��
D��
�ο��𰸣�A
���������
�����Ѷȣ���
2������� ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á���ͼΪ���ʾ��ͼ���õ�ص�
�������һ��ϸС�IJ��ۣ��������������ǿ�������ȶ�����ش�
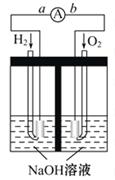
��1�� ����ȼ�ϵ�ص�����ת����ʽ��Ҫ��____ __��
��2�� �ڵ����е�����������Ϊ ____ �� __����a��b��ʾ����
��3�� ������ӦʽΪ__________ ________��
��4�� �缫����Ʋ��۵�ԭ��Ϊ_____ ____��
�ο��𰸣���1���ɻ�ѧ��ת��Ϊ���� (��)��a��b
������2H2 + 4OH--4e- = 4H2O���� H2+2OH--2e- = 2H2O
��4������缫��λ�������H2��O2���������ӿ�缫��Ӧ����
�����������1������ԭ��صĹ���ԭ����֪������ȼ�ϵ�ص�����ת����ʽ��Ҫ���ɻ�ѧ��ת��Ϊ���ܡ�
��2��ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ�����������ڸ���ͨ�룬ʧȥ���ӡ�����������ͨ�룬�õ����ӣ����ڵ����е�����������Ϊ��a��b��
��3����������ʧȥ���ӣ��ҵ������Һ�Լ��ԣ����缫��ӦʽΪH2+2OH--2e- = 2H2O��
��4���缫����Ʋ��ۺ�����缫��λ�������H2��O2���������ӿ�缫��Ӧ���ʡ�
���㣺����ԭ���Ӧ�õ��й��ж��Լ���������Է�Ӧ���ʵ�Ӱ��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ���������������淶�Ĵ�������������Ĺؼ�����ȷԭ��صĹ���ԭ����Ȼ��������������ü��ɡ�
�����Ѷȣ���
3��ѡ���� ����пƬ�ʹ�ͭƬ��ͼ��ʽ����100mL��ͬŨ�ȵ�ϡ������һ��ʱ�䣬����˵����ȷ���ǣ�������
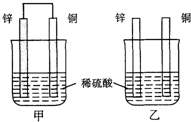
A���ס��Ҿ�Ϊ��ѧ��ת��Ϊ���ܵ�װ��
B������ͭƬ��������ð��
C������ͭƬ�������١�����пƬ��������
D�����е�����ͭƬ�ص�������пƬ
�ο��𰸣�����ԭ��صĹ��������жϣ�����ԭ��أ��Ҳ���ԭ��أ�
A������ԭ��أ��Ҳ���ԭ��أ����Լ��ǰѻ�ѧ��ת��Ϊ���ܵ�װ�ã��Ҳ��ǣ���A����
B������пƬ��������ð������B����
C���ס�����пƬ���������٣���C ����
D�����е�����ͭƬ�ص�������пƬ��������пƬ�ص�������ͭƬ����D��ȷ��
���������
�����Ѷȣ���
4��ѡ���� ����������ȷ����
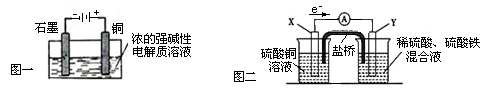
A��Cu2O��һ�ְ뵼����ϣ�������ɫ��ѧ������Ƶ���ȡCu2O�ĵ���ʾ��ͼ��ͼһ��ʾ��ʯī�缫�ϲ���������ͭ�缫����������Ӧ
B��ͼһ��ʾ����0.1mol����ת��ʱ����0.1molCu2O����
C��ͼ��װ���з�����Cu��2Fe3+ = Cu2+��2Fe2+��X���Ǹ�����Y�����Ͽ�����ͭ
D����ͼ�������ŵ������Ǵ��ݵ����ά�ֵ��ƽ�⣬Fe3+�������Ž�������ձ���
�ο��𰸣�A
���������ͼһΪ����,�������ҺΪǿ������Һ��ʯī�缫���Դ��������Ϊ������������ԭ��Ӧ��2H2O + 2e- = H2��+ 2OH-��ͭ�缫���Դ��������Ϊ����������������Ӧ��2Cu �C 2e- + 2OH- = Cu2O + H2O ������ܷ�ӦΪ��2Cu+H2OCu2O+H2�����ɴ˿�֪Aѡ����ȷ�����ݵ���ܷ�Ӧ��֪������0.2mol����ת��ʱ������0.1molCu2O���ɣ� Bѡ���ȷ��ͼ��װ��Ϊԭ��أ�����ͼ�и����ĵ����������ж�X���ǵ�صĸ�����Y���ǵ�ص�����������װ���з����ķ�Ӧ��Cu��2Fe3+ = Cu2+��2Fe2+����֪X��Ϊ������ʧ���ӣ�����������Ӧ����Cu-2e- = Cu2+������X���IJ���Ӧ����ͭ������ԭ��ص��γ�������Y������Ӧ���ǻ�Ա�ͭ���Ľ�����ʯī�Ȳ��ϣ���Cѡ���ȷ�����ŵ����â����������ӵĶ���Ǩ�ƹ����˵���ͨ·���Ӷ���ͨ�ڵ�·���γɱպϻ�·�������˵���ͨ�����·�ӵ�ظ����������IJ���ת�ƣ�ʹԭ��ز��ϲ�����������ƽ���ɣ����ſ�ʹ�������ӵ����������е���Һ���ֵ����ԣ�ͬʱ������ֹ��Ӧ��ֱ�ӽӴ������ԣ�Fe3+�Dz��ܾ������Ž�������ձ��У���Dѡ���ȷ��
�����Ѷȣ���
5��ѡ���� ����пƬ�ʹ�ͭƬ��ͼ��ʾ��ʽ������ͬŨ�ȵ�ϡ�����У������й���������ȷ����?
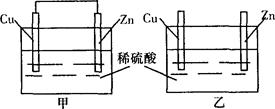
A����װ����ͭƬ��������������
B����װ���е���ת��Ϊ��ѧ��
C����װ���е���ת��Ϊ��ѧ��
D����װ����ͭƬ��������������
�ο��𰸣�A
�������������װ��ͼ��֪����װ����ԭ��أ���ѧ��ת��Ϊ���ܡ�����п��ͭ���ã�������ʧȥ���ӡ�ͭ����������Һ�е��������������õ�����������������װ����п��ϡ����ֱ�ӷ������û���Ӧ����ͭ��ϡ�����Ӧ������ѡ��A��ȷ������ѡ����Ǵ���ģ���ѡA��
�����������Ǹ߿��ֵij������ͺ���Ҫ�Ŀ��㣬��Ҫ�ǿ���ѧ����ԭ���ԭ�����缫���ơ��缫��Ӧʽ���˽����������ּ������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷԭ��صĹ���ԭ����Ȼ���������װ��ͼ������ü��ɡ�
�����Ѷȣ���