微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)某学生做浓硫酸性质的实验:在一支试管中放入一块很小的铜片,再加入2mL浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃管口处缠放一团蘸有Na2CO3溶液的棉花。加热试管,观察现象.回答下列问题:
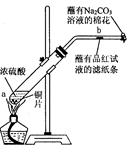
(1)写出试管中发生反应的化学方程式?。
(2)试管中的液体反应一段时间后,b处滤纸条的变化为?,待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为?。
(3)蘸有Na2CO3溶液的棉花团作用是?。
(4)硫酸型酸雨的形成过程可用下列反应中的?来表示。
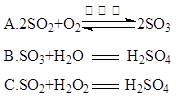
(5)浓硫酸有许多重要性质,在与含有水分的蔗糖作用过程中不能显示的性质是?
A.酸性
B.脱水性
C.强氧化性
D.吸水性
参考答案:(12分)(1)Cu+2H2SO4(浓)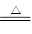 CuSO4+ SO2↑+2H2O
CuSO4+ SO2↑+2H2O
(2)蘸有品红溶液的滤纸褪色?,滤纸变红
(3)吸收多余SO2,防止污染空气 (4)A B?(5)A
本题解析:(1)在加热的条件下,浓硫酸和铜反应的化学方程式是Cu+2H2SO4(浓)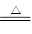 CuSO4+ SO2↑+2H2O。
CuSO4+ SO2↑+2H2O。
(2)硫酸的还原产物SO2具有漂泊性,能使品红溶液褪色。但SO2的漂白是不稳定的,在加热的情况下,可以恢复到用来的颜色,所以滤纸条又恢复红色。
(3)SO2是大气污染物,因此蘸有Na2CO3溶液的棉花团作用是吸收多余SO2,防止污染空气。
(4)空气中的SO2被氧化生成SO3,SO3溶于水生成硫酸,即形成酸雨,答案选AB。
(5)浓硫酸具有脱水性、吸水性和强氧化性。可以使蔗糖炭化,进而氧化生成CO2、SO2和水,所以在该变化过程中,没有体现硫酸的酸性,答案选A。2的检验和尾气处理
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,难易适中,有利于考查学生能力,也有利于培养学生的实验探究、分析以及逻辑推理能力。同时也有利于培养学生的环境保护意识,增强学生的社会责任感。
本题难度:一般
2、选择题 用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的是( )
A.
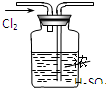
干燥Cl2
B.
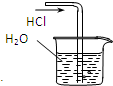
吸收HCl
C.
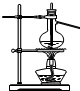
石油的分馏
D.
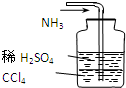
吸收NH3
参考答案:A、气体干燥装置的特点是长导管进气短导管出气,故A错误;
B、氯化氢极易溶于水,如果把导管直接插入水中容易产生倒吸现象,故B错误;
C、石油的分馏是根据馏分的沸点不同分离的,所以温度计测得温度应是气体的温度,故C错误;
D、氨气能和酸反应生成盐,四氯化碳和氨气不反应,且稀硫酸和四氯化碳不互溶,虽然氨气在稀硫酸中的溶解度较多,但因为在四氯化碳中不溶解,所以不含产生倒吸现象,所以能用该装置吸氨气,故D正确;
故选D.
本题解析:
本题难度:一般
3、选择题 下列气体中,不能用排空气收集的是
A.NO
B.NO2
C.CO2
D.H2
参考答案:A
本题解析:NO极易被氧气氧化生成NO2,所以不能用排气法收集,而是用排水法收集。其余都可以用排气法收集,所以答案是A。
本题难度:一般
4、选择题 下列反应制取气体合理可行的是
A.Zn + 2HNO3(稀)= Zn(NO3)2 + H2↑
B.CaCO3 + H2SO4(稀)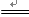 CaSO4 + H2O + CO2↑
CaSO4 + H2O + CO2↑
C.NH4Cl(aq) + NaOH(aq)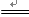 NaCl + H2O + NH3↑
NaCl + H2O + NH3↑
D.MnO2 + 4HCl(浓)  MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
参考答案:D
本题解析:硝酸属于氧化性酸,和金属反应不能生成氢气。实验室制取CO2,不能使用硫酸,因为生成物硫酸钙微溶,会附着在碳酸钙表面,阻止反应的进行。实验室制取氨气不能在稀溶液中进行,而是利用熟石灰和氯化铵加热来制取。所以选项D是正确的,答案选D。
本题难度:一般
5、选择题 下列除杂或鉴别方法正确的是
A.用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液
B.用点燃的方法除去CO2中的CO
C.用加热法除去Na2CO3溶液中的NaHCO3
D.用品红溶液或酸性KMnO4溶液鉴别 CO2和SO2
参考答案:D
本题解析:
正确答案:D
A.不正确,用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液,两者均产生沉淀。
B. 不正确,无法用点燃的方法除去CO2中的CO,引入O2,,或点不着;
C. 不正确,用加热溶液中的NaHCO3,达不到分解温度。
本题难度:一般