��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���д�ʩ������ѧ��Ӧ������Ч�����ǣ�������
A��KClO3�ֽ�������ʱ����������MnO2�����Ҽ���
B��������ϡ���ᷴӦ��ʵ��ʱ������Ƭ��Ϊ����
C������ϡ���ᷴӦ��ȡ����ʱ��������������Ϊ98%��Ũ����
D��п��ϡ���ᷴӦʱ�����������Ȼ�ͭ����
�ο��𰸣�A�������ܸı仯ѧ��Ӧ���ʣ���A��ȷ��
B������Ƭ��Ϊ���������˷�Ӧ��ĽӴ������������Ӧ���ʣ���B��ȷ��
C������ϡ���ᷴӦ����������������Ũ�����ܷ����ۻ�������ò�����������C����
D��п��ϡ���ᷴӦʱ�����������Ȼ�ͭ��п�û���ͭ��п��ͭ����ϡ�����ܹ���ԭ��ض��ӿ췴Ӧ���ʣ���D��ȷ��
��ѡC
���������
�����Ѷȣ���
2������� �Ͼ�ӡˢ��·��Ļ������ÿ�ʵ����Դ��������������Ⱦ���Ͼ�ӡˢ��·�徭������룬�ܵõ��ǽ�����ĩ�ͽ�����ĩ��
��1�����д���ӡˢ��·��ǽ�����ĩ�ķ����У������ϻ��������������__________������ĸ����
A�����ѽ��γ�ȼ�� B��¶����� C����Ϊ�л����Ͻ������ϵ�ԭ�� D��ֱ������
��2����H2O2��H2SO4�Ļ����Һ���ܳ�ӡˢ��·�������ĩ�е�ͭ����֪
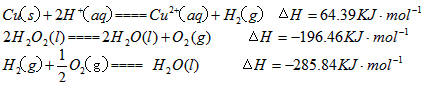
��H2SO4��Һ��Cu��H2O2��Ӧ����Cu2+��H2O���Ȼ�ѧ����ʽΪ__________________________��
��3����������������ͬ��ӡˢ��·��Ľ�����ĩ��10�GH2O2��3��0mol/L H2SO4�Ļ����Һ��������ò�ͬ�¶���ͭ��ƽ���ܽ����ʣ����±�����
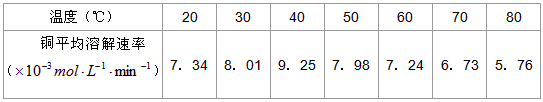
���¶ȸ���40��ʱ��ͭ��ƽ���ܽ��������ŷ�Ӧ�¶����߶��½�������Ҫԭ����___________________��
��4�����ᴿ���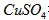 ��Һ�м���һ������
��Һ�м���һ������ ��Һ�����ȣ�����
��Һ�����ȣ����� �������Ʊ�
�������Ʊ�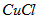 �����ӷ���ʽ��______________________________��
�����ӷ���ʽ��______________________________��
�ο��𰸣���1��BD
��2��Cu(s)+H2O2(l)+2H+(aq)==Cu2+(aq)+2H2O(l) ��H=-319��68kJ/mol
��3��H2O2�ֽ����ʼӿ�
��4��2Cu2++SO32-+2Cl-+H2O2 CuCl��+SO42-+2H+
CuCl��+SO42-+2H+
���������
�����Ѷȣ�����
3������� ��ѧ��Ӧ������?ʱ����?��?��?�ı仯����ʾ�����ݻ�����ķ�Ӧ���У�ͨ������?ʱ���ڷ�Ӧ��Ũ�ȵ�?��������Ũ�ȵ�?����ʾ��������ʽ?����ѧ��Ӧ���ʳ��õĵ�λ��?��
�ο��𰸣���λ?����Ӧ�������?��Ũ��?��?��λ?��С?������? V=��C/��t��? mol/��L?s����? mol/��L��min��?��
�����������
�����Ѷȣ���
4��ѡ���� ���и�ͼ���ܱ�ʾA(g)+B(g)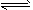 2C(g)������ӦΪ���ȷ�Ӧ��������淴Ӧ��ͼ��Ϊ
2C(g)������ӦΪ���ȷ�Ӧ��������淴Ӧ��ͼ��Ϊ
A��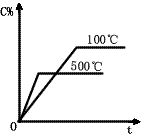
B��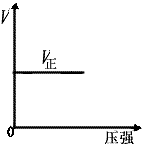
C��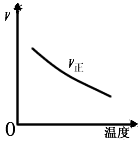
D��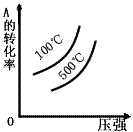
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5������� ��15�֣���ش��������⣺
��1���ֱ���Ũ��ϡ�����ܽ����������ͭ�ۣ�������������ʵ������ٵ���_________���ᣨ�Ũ����ϡ��������Ӧ�����ӷ���ʽ��_____________.
��2�� 800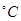 ʱ����2L�ĺ����ܱ������г���2molNO��1molO2������Ӧ��2NO(g)+O2(g)
ʱ����2L�ĺ����ܱ������г���2molNO��1molO2������Ӧ��2NO(g)+O2(g) 2NO2(g)����5min�ﵽƽ�⣬���c��NO)="0.5" mol/L��������QkJ��5min�� v(O2)=___________��
2NO2(g)����5min�ﵽƽ�⣬���c��NO)="0.5" mol/L��������QkJ��5min�� v(O2)=___________��
�ڸ������£�2NO(g)+O2(g) 2NO2(g)�ġ�H=?��
2NO2(g)�ġ�H=?��
������ƽ���������ٳ���NO��NO2��1mol,��ʱv��?v�棨�>������=����<������
������ƽ�������н�����lmolNO2��ƽ����_______�������������������
��������ƽ��ʱ��NO2���������________�����������С�����䡱����
��3��Ⱦ�Ϲ�ҵ�ŷŵķ�ˮ�к��д����ж���NO2����������ǿ���������¼������۳�ȥ����Ӧ����������̬�������ɡ����ȷ�Ӧ�����Һ����ʹʪ��ĺ�ɫʯ����ֽ�����������ݳ�������д���÷�Ӧ�����ӷ���ʽ________
�ο��𰸣�27�������15�֣���һ��1�֣�����ÿ��2�֡���
��1��ϡ�� 3Cu + 8H+ + 2NO3���� 3Cu2+? + 4 H2O + 2NO��?
��2����0.05 mol/(L��min)?�ڣ�2Q kJ/mol?�� ��?�� ��������
��3��2Al+NO2��+OH��+2H2O��2AlO2��+NH3��H2O
�����������1��ͭ��ϡ����ķ�ӦΪ��3Cu+8HNO3=3Cu(NO3)2+NO��+H2O��ͭ��Ũ����ķ�ӦΪ��Cu+4HNO3(Ũ��=Cu(NO3)2+2NO2��+2H2O������ͭΪ1mol������ϡ����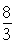 ������Ũ����4mol��������ϡ��������ʵ�����С����2����NO����ʼŨ��Ϊ1mol/L������Ϊ0.5mol/Lʱ��ת��Ũ��Ϊ0.5mol/L������Ϊ0.1mol/(L
������Ũ����4mol��������ϡ��������ʵ�����С����2����NO����ʼŨ��Ϊ1mol/L������Ϊ0.5mol/Lʱ��ת��Ũ��Ϊ0.5mol/L������Ϊ0.1mol/(L min)������֮�ȵ���ϵ��֮�ȣ�����������ʾ�ķ�Ӧ����Ϊ0.05mol/(L
min)������֮�ȵ���ϵ��֮�ȣ�����������ʾ�ķ�Ӧ����Ϊ0.05mol/(L min)���ڵ�NO��Ũ�ȱ�Ϊ0.5mol/Lʱ��ת����Ϊ1mol���ų�����ΪQ����ת����Ϊ2molʱ���ų�����Ϊ2Q����
min)���ڵ�NO��Ũ�ȱ�Ϊ0.5mol/Lʱ��ת����Ϊ1mol���ų�����ΪQ����ת����Ϊ2molʱ���ų�����Ϊ2Q���� ��HΪ-2QKJ/mol�����ٳ���NO��NO2��1molʱ���Ũ����Q=K��ƽ�ⲻ�����ƶ���������Ӧ���ʺ��淴Ӧ������ȣ�������ͨ��NO2�������˲����Ũ�ȣ�ƽ�������ƶ�����NO2�����ʵ������ӣ������������3������̬������Ⱥ��������������һˮ�ϰ����ɣ�������ԭ������ǿ������Һ������AlO2-�����ԭ���غ��������ԭ����ʽ����ƽ�ۺϷ���д�����ӷ���ʽ��
��HΪ-2QKJ/mol�����ٳ���NO��NO2��1molʱ���Ũ����Q=K��ƽ�ⲻ�����ƶ���������Ӧ���ʺ��淴Ӧ������ȣ�������ͨ��NO2�������˲����Ũ�ȣ�ƽ�������ƶ�����NO2�����ʵ������ӣ������������3������̬������Ⱥ��������������һˮ�ϰ����ɣ�������ԭ������ǿ������Һ������AlO2-�����ԭ���غ��������ԭ����ʽ����ƽ�ۺϷ���д�����ӷ���ʽ��
�����Ѷȣ�һ��