��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��14�֣���̼����(��Ҫָ����CO2)�ڽ������������ŷ��о�����Ҫ�����á�ĿǰNH3��(NH4)2CO3�Ѿ���������ҵ��̼����������CO2�ɷ������¿��淴Ӧ��
��Ӧ��2NH3(l)��H2O(l)��CO2(g)  ?(NH4)2CO3(aq)? ��H1
?(NH4)2CO3(aq)? ��H1
��Ӧ��NH3(l)��H2O(l)��CO2(g)  NH4HCO3(aq)? ��H2
NH4HCO3(aq)? ��H2
��Ӧ��(NH4)2CO3(aq)��H2O(l)��CO2(g)  2NH4HCO3(aq)? ��H3
2NH4HCO3(aq)? ��H3
��ش��������⣺
(1)��H3�릤H1����H2֮��Ĺ�ϵ�ǣ���H3��?��
(2) ��Ӧ��Ļ�ѧƽ�ⳣ������ʽΪ ?��
(3)Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�������һ������CO2����(�õ�����Ϊϡ�ͼ�)����tʱ�̣����������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��T4��T5�£�����������ʼʵ���������䣬�ظ�����ʵ�飬������ͬʱ����CO2����Ũ�ȣ��õ�����ͼ(��ͼ1)����
�٦�H3?0(�����������������)��
����T1��T2��T4��T5�����¶����䣬������CO2����Ũ�ȳ�����ͼ1��ʾ�ı仯���ƣ���ԭ����?
?��
�۷�Ӧ�����¶�ΪT1ʱ����ҺpH��ʱ��仯������������ͼ2��ʾ����ʱ�䵽��t1ʱ�����÷�Ӧ��ϵ�¶�Ѹ��������T2����ά�ָ��¶ȡ����ڸ�ͼ�л���t1ʱ�̺���Һ��pH�仯���������ߡ�
 ?
?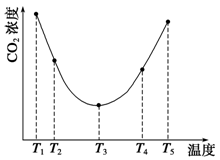
ͼ1?ͼ2
(4)���÷�Ӧ��CO2����(NH4)2CO3��ʼŨ�Ⱥ����ȷ��������£����CO2�������Ĵ�ʩ��?
?��
(5)����������Ҳ������ΪCO2���������?��
A��NH4Cl
B��Na2CO3
C��HOCH2CH2OH
D��HOCH2CH2NH2
�ο��𰸣�(1)2��H2����H1?(2)? K��c2 (NH4HCO3) /��c [(NH4)2CO3)]��c(CO2)��
(3)�٣�?����T1��T2���䣬��ѧ��Ӧδ�ﵽƽ�⣬�¶�Խ�ߣ���ѧ��Ӧ����Խ�죬����CO2������������¶����߶���ߡ�T4��T5���䣬��ѧ��Ӧ�Ѵﵽƽ�⣬��������Ӧ�Ƿ��ȷ�Ӧ���¶�����ƽ�����淴Ӧ�����ƶ������Բ�����CO2����
�� (4)�����¶ȣ�����CO2Ũ��(���ѹ)?(5)BD
(4)�����¶ȣ�����CO2Ũ��(���ѹ)?(5)BD
�����������1������Ӧ������д����NH4��2CO3��aq�� 2NH3��l��+H2O ��l��+CO2��g��-��H1������Ӧ���2��2NH3��l��+2H2O ��l��+2CO2��g��
2NH3��l��+H2O ��l��+CO2��g��-��H1������Ӧ���2��2NH3��l��+2H2O ��l��+2CO2��g�� 2NH4HCO3��aq��?2��H2���ã���NH4��2CO3��aq��+H2O ��l��+CO2��g��
2NH4HCO3��aq��?2��H2�����NH4��2CO3��aq��+H2O ��l��+CO2��g�� 2NH4HCO3��aq����H3=2��H2-��H1 ��
2NH4HCO3��aq����H3=2��H2-��H1 ��
��2����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ����˷�Ӧ��Ļ�ѧƽ�ⳣ������ʽΪK��c2 (NH4HCO3) /��c [(NH4)2CO3)]��c(CO2)����
��3������ͼ1��֪�����¶�ΪT3ʱ��Ӧ��ƽ�⣬�˺��¶����ߣ�c��CO2������ƽ�������ƶ���˵����Ӧ���Ƿ��ȷ�Ӧ��H3��0��
��T1��T2���䣬��ѧ��Ӧδ�ﵽƽ�⣬�¶�Խ�ߣ���ѧ��Ӧ����Խ�죬����CO2������������¶����߶���ߡ�T4��T5���䣬��ѧ��Ӧ�Ѵﵽƽ�⣬��������Ӧ�Ƿ��ȷ�Ӧ���¶�����ƽ�����淴Ӧ�����ƶ������Բ�����CO2����
�۷�Ӧ�����¶�ΪT1ʱ����ƽ�����ͼ2��֪����ҺpH����ʱ��仯���仯����Ѹ��������T2��ά���¶Ȳ��䣬ƽ�������ƶ�����ҺpH������T2ʱ�ֽ����µ�ƽ�⣬ͼ��ӦΪ�� ��
��
��4������ƽ���ƶ�ԭ���������¶Ȼ�����c��CO2����
��5�����м��Ե����ʾ��ܲ���CO2����Ӧ���£�Na2CO3+CO2+H2O��2NaHCO3��HOCH2CH2NH2+CO2+H2O��HOCH2CH2NH3++HCO3-���ʴ�ΪB��D��
�����Ѷȣ�һ��
2������� (14��)T��ʱ����һ�����Ϊ2L�������У�A������B���巴Ӧ����C���壬��Ӧ������A��B��CŨ�ȱ仯��ͼ��ʾ��
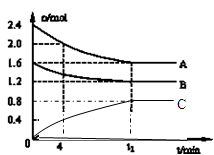
��1��д���÷�Ӧ�ķ���ʽ��__ ___
��2��������¶��¸÷�Ӧ��ƽ�ⳣ����___ ___
��3��������A�������ӣ���÷�Ӧ��______�ȷ�Ӧ��
��4��0��4����ʱ��C��ƽ����Ӧ����Ϊ��___ ___
��5������ƽ��ʱA��ת����Ϊ��______
��6�����������£����д�ʩ����ʹn��A��/n��C����С����______��
A�����뺤��
B��ʹ�ô���
C���ٳ���2.4molA��1.6molB
D�������¶�
��7�� ���ijһʱ�̺�ѹ��ƽ�����ƣ������һ�����ԭ�������
���ijһʱ�̺�ѹ��ƽ�����ƣ������һ�����ԭ�������
�ο��𰸣���1��2A(g)+B(g) 2C(g) ��2��
2C(g) ��2��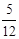 ��3���ţ�4��0.05mol?L-1?min-1��
��3���ţ�4��0.05mol?L-1?min-1��
��5��33.3%��6��CD��7��AҺ����̻�
�����������1������ͼ����������ʵ������ٵ�Ϊ��Ӧ����ʵ������ӵ�Ϊ�������ABΪ��Ӧ�CΪ���������ͬ��ʱ���ڣ�A�ı���2.4-1.6=0.8��B�ı���1.6-1.2=0.4��C�ı���0.8���ʷ���ʽд��2A(g)+B(g) 2C(g)����2������ƽ�ⳣ���ļ��㹫ʽ���㣬K= c(C)2 /c(A)2c(B)= 0.42/0.82��0.6=5/12,����3������ƽ�������ȷ����ƶ���A��������˵�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ����4��A��ƽ������="(2.4-2.0)��2��4=0.05" mol?L-1?min-1�����ݼ������ȣ�����C��ƽ������Ϊ���ʵ����ʱȵ���0.05 mol?L-1?min-1����5��A��ת����=(2.4-2.0)/2.4=33.3%����6�����������£�Ҫʹn��A��/n��C����С����Ҫʹƽ�������ƶ������뺤����ƽ�ⲻ�ƶ���ʹ�ô�����ƽ�ⲻ�ƶ����ٳ���2.4Ħ����A��1.6Ħ����B ���൱�ڼ�ѹ��ƽ�������ƶ��������¶ȣ�ƽ�������ƶ�����ѡCD����7����ѹ��ƽ�����ƶ���˵�����巴Ӧ��Ļ�ѧ������С������������Ļ�ѧ���������Ҳ�Ļ�ѧ������Ϊ2��������ΪС��2����ֵ�����Կ�����A�Ѿ�Һ����̻���
2C(g)����2������ƽ�ⳣ���ļ��㹫ʽ���㣬K= c(C)2 /c(A)2c(B)= 0.42/0.82��0.6=5/12,����3������ƽ�������ȷ����ƶ���A��������˵�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ����4��A��ƽ������="(2.4-2.0)��2��4=0.05" mol?L-1?min-1�����ݼ������ȣ�����C��ƽ������Ϊ���ʵ����ʱȵ���0.05 mol?L-1?min-1����5��A��ת����=(2.4-2.0)/2.4=33.3%����6�����������£�Ҫʹn��A��/n��C����С����Ҫʹƽ�������ƶ������뺤����ƽ�ⲻ�ƶ���ʹ�ô�����ƽ�ⲻ�ƶ����ٳ���2.4Ħ����A��1.6Ħ����B ���൱�ڼ�ѹ��ƽ�������ƶ��������¶ȣ�ƽ�������ƶ�����ѡCD����7����ѹ��ƽ�����ƶ���˵�����巴Ӧ��Ļ�ѧ������С������������Ļ�ѧ���������Ҳ�Ļ�ѧ������Ϊ2��������ΪС��2����ֵ�����Կ�����A�Ѿ�Һ����̻���
���㣺���淽��ʽ����д����ѧƽ���ƶ�����ѧƽ�ⳣ����
�����Ѷȣ�һ��
3��ѡ���� �����й�˵������ȷ���ǣ�������
A���ϳɰ��в��ü�ʱ���백����߷�Ӧ���ת����
B�������¶���ʹ���ȷ�Ӧ���ʼӿ죬ʹ���ȷ�Ӧ���ʼ���
C������ѹǿ����ѧ��Ӧ����һ���ӿ죬ƽ��һ�������ƶ�
D����ѧ��Ӧ��Ȼ��������״̬�ı仯
�ο��𰸣�A������������������������Ũ�ȣ�ƽ�������ƶ���������߷�Ӧ���ת���ʣ���A��ȷ��
B�������¶�ʹ��ѧ��Ӧ���ʼӿ죬�뷴Ӧ����ЧӦ�أ���B����
C��������μӵķ�Ӧ������ѹǿ����Ӧ���ʼӿ죬����Ӧ���ʲ����ͬ�ȳ̶ȵı仯����ѧƽ�ⲻ�ƶ�����C����
D����ѧ��Ӧ�����ʵ�״̬��һ���仯����ϳɰ��ķ�Ӧ����Ӧ�����������Ϊ���壬��D����
��ѡA��
���������
�����Ѷȣ�һ��
4��ѡ���� ������Fe����һ���������ᷴӦ��Ϊ�˼�����Ӧ���ʣ����ֲ�Ӱ�����������������Ӧ�������������еģ�������
A��NaNO3��Һ
B��NaCl����
C��Na2SO4��Һ
D��CuSO4��ĩ
�ο��𰸣����ݷ����ķ�ӦΪFe+2H+�TFe2++H2�������С�����ӵ�Ũ�ȶ����ı������ӵ����ʵ����������������Ӧ���ʣ����ֲ�Ӱ�����������������
A������NaNO3��Һ��Fe����������ӡ������ӷ���������ԭ��Ӧ����NO������������������A����
B������NaCl���壬�Է�Ӧ��Ӱ�죬���������Ӧ���ʣ���B����
C������Na2SO4��Һ�������Ʋ����뷴Ӧ����Һ�������������ӵ�Ũ�ȼ�С���������ӵ����ʵ���û�б仯����Ӧ���ʼ��������ֲ�Ӱ�������������������C��ȷ��
D������CuSO4������Fe��Cu������ԭ��أ��ӿ췴Ӧ���ʣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
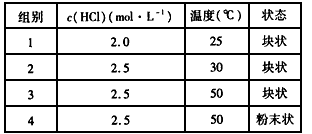
5��ѡ���� ����������������������ڲ�ͬ��ʵ�������½��з�Ӧ���ⶨ�ڲ�ͬʱ��t�����������V�����ݣ��������ݻ��Ƶõ���ͼ��ʾ���ߣ�������a��b��c��d����Ӧ��ʵ����������
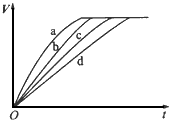 ?
? 
[? ]
A.4.3.2.1
B.1.2.3.4
C.3.4.2.1
D.1.2.4.3
�ο��𰸣�A
���������
�����Ѷȣ�һ��