微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
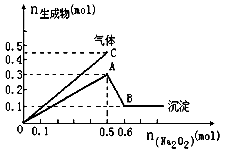
1、选择题 向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中三种离子的物质的量之比为
[? ]
A.2∶1∶2
B.1∶2∶2
C.2∶2∶1
D.9∶2∶4
参考答案:B
本题解析:
本题难度:一般
2、选择题 Na2O2、HCl、Al2O3三种物质在水中完全反应后并充分过滤,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为
[? ]
A.3∶2∶1
B.2∶4∶1
C.2∶3∶1
D.4∶2∶1
参考答案:B
本题解析:
本题难度:一般
3、选择题 有镁铝混合粉末10.2 g,将它溶于500 mL 4 mol/L的盐酸中,若要使沉淀的质量最大,则需加入2 mol/L的氢氧化钠溶液的体积是
[? ]
A.1000 mL
B.500 mL
C.100 mL
D.1 500 mL
参考答案:A
本题解析:
本题难度:一般
4、选择题 XSO4溶液与NaOH溶液反应,可生成X3(OH)4SO4沉淀和Na2SO4溶液,现有v1mL 0.1 mol/L XSO4溶液和v2 mL 0.2 mol/L NaOH溶液(v1+v2=50),为了使沉淀的质量达到最大值,v1和v2的取值应为
[? ]
A.V1=30,V2=20
B.V1=20,V2=30
C.V1=10,V2=40
D.V1=15,V2=35
参考答案:A
本题解析:
本题难度:一般
5、计算题 在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除去氧化膜、并用针刺一些小孔的铝箔包好,然后放人盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27 g,水槽和容器内溶液的总体积为2.0L,溶液中
NaOH的浓度为0.050 mol/L(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式。
(2)试通过计算确定该钠块中钠元素的质量分数。
参考答案:(1)①2Na+2H2O=2NaOH+H2↑;②Na2O+H2O=2NaOH;③2Al+2NaOH+2H2O=2NaAlO2+3H2↑ (2)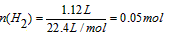
 根据化学方程式,反应③中n(H2)=0.015 mol
根据化学方程式,反应③中n(H2)=0.015 mol
反应①中n(H2)=0. 05 mol-0.015 mol=0. 035mol
n(Na)=0.07 mol
溶液中n(Na+)=n(NaOH)+n(NaAlO2) =2.0L×0.05 mol/L+0.01 mol =0.11 mol 根据Na守恒n(Na2O)= =0.02mol
=0.02mol
Na元素的质量分数为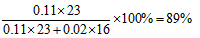
本题解析:
本题难度:一般