��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
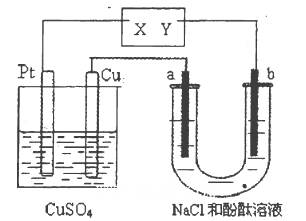
1��ѡ���� ��ͼ��ʾa��b ���Ƕ��Ե缫��ͨ�硪��ʱ���a��������Һ�Ժ�ɫ������˵������ȷ����(? )��
 ?
?
A��X��������Y�Ǹ���
B��X�Ǹ�����Y������
C��CuSO4��Һ��Ũ����С
D��CuSO4��Һ��pH��С
�ο��𰸣�B
�����������װ��Ϊ���װ�ã�a���Ժ�ɫ��˵��a������������Ũ������������Ũ�ȼ�С������a�������ӷŵ磬��a��Ϊ������b��Ϊ������YΪ����XΪ������A����B��ȷ����˲���Ϊ������ͭ���ӷŵ��Ϊ����ͭ��ͭ��Ϊ������ͭ�ŵ��Ϊͭ���ӽ�����Һ������CuSO4��Һ��Ũ�Ȼ������䣬pH�������䣬C��D����ѡB��
�����Ѷȣ���
2��ѡ���� ��ʯī��������ͭ��������ⱥ��NaCl��Һ����ʼԼ30s��������������ɫ���ǣ�Ȼ��ʼ���ֳȻ�ɫ���ǣ��������ɽ϶�ijȻ�ɫ����������˵����ȷ����
A��������Cu �C 2e- = Cu2+
B��ˮ������������ɫ������NaCl
C���Ȼ�ɫ������CuCl
D���Ȼ�ɫ���������ð�ˮ�ܽ�
�ο��𰸣�C
�����������
�����Ѷȣ���
3������� ��?H+��Cu2+��Na+��SO42-��Cl-��ѡ���ʵ���������ɵ���ʣ�ʹ֮��������Ҫ��
��1����ʯī��Ϊ�缫�����ʱ�����������С��ˮ�����䣬Ӧѡ�õĵ������______��
��2����ʯī��Ϊ�缫�����ʱ������������䣬ˮ�����٣�Ӧѡ�õĵ������______��
��3����ʯī��Ϊ����������Ϊ���������ʱ����ʺ�ˮ�������٣�Ӧѡ�õĵ������______��
�ο��𰸣��������ӷŵ�˳��ΪCu2+��Na+��H+�������ӷŵ�˳��ΪCl-��OH-��SO42-��
��1�����Ե缫���CuCl2��Һʱ��ͭ���ӡ������ӷŵ磬������������С��ˮ�����䣬�ʴ�Ϊ��CuCl2��
��2�����Ե缫���H2SO4����Na2SO4����Һʱ�������ӡ����������ӷŵ磬�������������䣬ˮ�����٣��ʴ�Ϊ��H2SO4����Na2SO4����
��3��ʯī��Ϊ����������Ϊ���������CuSO4����NaCl����Һʱ����ͭ���ӡ����������ӣ��������ӡ������ӣ��ŵ磬���Ե���ʺ�ˮ�������٣��ʴ�Ϊ��CuSO4����NaCl����
���������
�����Ѷȣ�һ��
4��ѡ���� ��ͼ��ʾ��������װ������ͭ��Һ��ѡ�ò�ͬ���ϵĵ缫���е�⡣�±���˵����ȷ����

?
| �缫����
| ͨ���ı仯
|
����
| ����
|
A
| ʯī
| ʯī
| �����������ӣ���Һ��pH����
|
B
| ͭ
| ͭ
| ������������������������
|
C
| ��
| ��
| �����������������仯
|
D
| ��
| ��
| �����������ӣ���Һ��Ũ�Ȳ���
�ο��𰸣�B
�������������ʯī��Ϊ�缫�������ͭ��Һ��������OH���ŵ������������Һ�ļ��Լ�����pH���ͣ�����Cu2���ŵ�����ͭ��A����ȷ������ͭ�缫�������ͭ��Һ�������ڴ�ͭ���ᴿ��ѡ��B��ȷ���������缫�������ͭ��Һ������Cu2���ŵ�����ͭ��������ʧȥ���Ӷ��ܽ⣬C����ȷ�����ò������������������������ͭ��Һ����Ȼ������Cu2���ŵ�����ͭ��������ʧȥ���Ӷ��ܽ⣬����Һ��Cu2��Ũ�ȼ�С��Fe2������DҲ����ȷ��
�����Ѷȣ�һ��
5��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A����ͭ����ʱ�����Դ�����������Ǵ�ͭ���õ缫��Ӧʽֻ�У�Cu ��2e��= Cu2+
B����KIO3����������Һ�е�KI�� 5I��+IO3��+3H2O =3I2+6OH��
C���Ȼ�����Һ��ͭ��Ӧ��Fe3++Cu=Fe2++Cu2+
D��0.01 mol��L��1 NH4Al(SO4)2��Һ��0.02 mol��L��1 Ba(OH)2��Һ�������ϣ�
|
NH4++Al3++2SO42-+2Ba2++4OH��=2BaSO4��+Al(OH)3��+NH3��H2O
�ο��𰸣�D
���������A��������ͭʱ�����Դ�����������Ǵ�ͭ����Ϊ��ͭ�к�������п���ʣ����Ի��ᷢ��Fe-2e-=Fe2+�ȷ�Ӧ������B��������Һ�е������ﲻ���������������ӣ����ӷ���ʽӦΪ5I��+IO3��+6H+=3I2+3H2O������C����ɲ��غ㣬����D��0.01 mol��L��1 NH4Al(SO4)2��Һ��0.02 mol��L��1 Ba(OH)2��Һ�������ϣ���������ʵ�����ǰ�ߵ�2���������������ȫ�����������������������ӷ�Ӧ������������������笠����������������ӷ�Ӧ����һˮ�ϰ�����ȷ����ѡD��
���㣺�������ӷ���ʽ��д������ж�
�����Ѷȣ�һ��