微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是( )
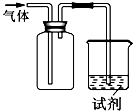
A.气体NO,试剂紫色石蕊试液,现象溶液变红,结论NO与水反应生成硝酸
B.气体Cl2,试剂KI淀粉溶液,现象溶液变蓝,结论Cl2有氧化性
C.气体SO2,试剂酸性KMnO4溶液,现象溶液褪色,结论SO2有漂白性
D.气体NH3,试剂酚酞试剂,现象溶液变红,结论NH3有碱性
参考答案:A、NO易与氧气反应,不能用排空法收集,故A错误;
B、淀粉碘化钾溶液变蓝,说明碘离子被氯气氧化成碘单质,证明氯气具有氧化性,故B正确;
C、二氧化硫密度比空气大,可用向上排空法收集,具有还原性,可与酸性高锰酸钾发生了氧化还原反应,故C错误
D、氨气密度比空气小,不能用向上排空法收集,应用向下排空法收集,故D错误;
故选B.
本题解析:
本题难度:简单
2、实验题 (8分)用如图所示的装置进行制取NO实验(已知Cu与HNO3的反应是放热反应)。
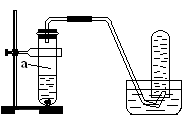
(1)在检查装置的气密性后,向试管a中加入10ml 6 mol・l-1稀HNO3和1gCu片,然后立即用带导管的橡皮塞塞紧试管口。请写出Cu与稀HNO3反应的化学方程式:_______________________________________________________。
(2)实验过程中通常在开始反应时反应速率缓慢,随后逐渐加快,这是由于
_________________________________________________; 进行一段时间后速率
又逐渐减慢,原因是______________________________________________。
(3)欲较快地制得NO,可采取的措施是_____________。
A.加热
B.使用铜粉
C.稀释HNO3
D.改用浓HNO3
参考答案:(1)3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
(2)反应放热,使温度升高,反应速率加快;反应一段时间后,硝酸的浓度减小了,反应速率又逐渐减慢。?(3)AB
本题解析:(1)稀硝酸具有强氧化性,和铜反应生成硝酸铜、NO和水。
(2)影响反应速率的因素一般是温度和浓度等。随反应的进行,浓度是降低的,但反应速率是逐渐加快的,说明在反应过程中,温度升高导致反应速率加快的,即该反应是放热反应。当反应进行到一定程度时,硝酸的浓度降低,此时浓度的影响超过了温度对反应速率的影响,因此反应速率又降低。
(3)根据外界条件对反应速率的影响,要加快反应速率可以通过升高温度,或增大反应物的接触面积。C是稀释硝酸,浓度降低,反应速率降低。浓硝酸和铜反应的还原产物是NO2。所以正确的答案是AB。
本题难度:一般
3、实验题 (12分)某化学学习小组采用下图所提供的仪器装置(夹持仪器已略去)设计实验:验证浓硝酸的氧化性。实验表明浓硝酸能将NO氧化成NO2,由此得出的结论是浓硝酸具有氧化性。
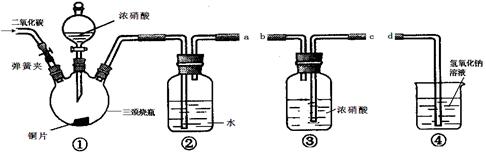
试回答有关问题:
(1)仪器接口的连接顺序为___________? ____________;
(2)按(1)中连接顺序安装好装置后下一步的操作是___? ____;
加入药品后,打开弹簧夹,通入CO2一段时间,通入CO2的目的是___________________________________________________;
关闭弹簧夹,将装置④中的导管末端伸入氢氧化钠溶液中是为了_________________? __________________;
(3)装置②发生反应的化学方程式是___________________________________;
(4)该小组得出的结论所依据的实验现象是_____________________________。
参考答案:(1)a→c→b→d?
(2)检验装置气密性;排尽装置中的空气;
吸收二氧化氮,防止其扩散到空气中污染空气
(3) 3NO2+H2O=2HNO3+NO?(4)②中逸出的无色气体通过③时变成红棕色
本题解析:(1)①是气体的发生装置,浓硝酸和铜反应生成NO2,NO2溶于水即生成NO,所以要检验浓硝酸的氧化性,需要把NO通入到浓硝酸中,氮的氧化物属于大气污染物,需要进行尾气处理,因此最后要通入到氢氧化钠溶液中,即顺序为a→c→b→d。
(2)装置连接好以后,必须最÷检验装置的气密性。因为空气中的氧气也能氧化NO,所以为了防止干扰,需要排尽装置中的空气。
(3)NO2溶于水的方程式为3NO2+H2O=2HNO3+NO。
(4)NO是无色,被氧化生成NO2后气体颜色变为红棕色,所以当②中逸出的无色气体通过③时变成红棕色,即说明结论是正确的。
本题难度:一般
4、填空题 (每空2分,共12分)实验室欲配制220mL 0.2 mol・L-1的碳酸钠溶液,回答下列问题:
可供选择的仪器:①量筒②胶头滴管③托盘天平④药匙⑤烧瓶⑥烧杯
(1)通过计算可知,应用托盘天平称取?g碳酸钠晶体(Na2CO3?10H2O)
(2)配制过程需要的仪器______________(填序号),还缺少的仪器有?
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)_____________;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.用托盘天平准确称取所需的Na2CO3固体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀