微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (19分)黄铜矿的主要成分是CuFeS2(硫元素显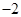 价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下:
价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下:
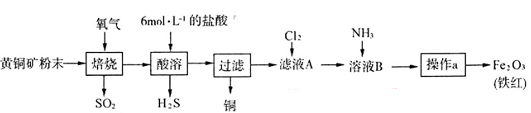
已知:
 ?
? =
=
(1)在实验室中,应将黄铜矿粉末放在__________(填仪器名称)中焙烧。
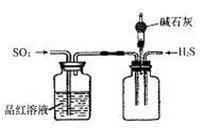
(2)将反应过程中产生的SO2和H2S通入下图所示装置中检验它们的性质。该实验证明SO2具有_________性和__________性。
(3)欲选用下列部分装置在实验室中以MnO2和浓盐酸为原料制取纯净、干燥的氯气。
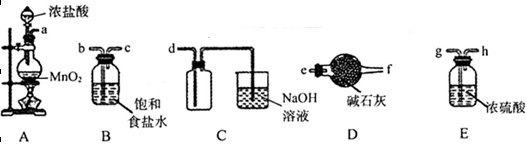
①圆底烧瓶中发生反应的离子方程式为_________________________________________。
②按气流方向由左到右,导管口连接顺序为a→__________________________________。
③装置连接好后,在装药品前,需检验装置的气密性,具体方法是__________________。
④向滤液A中通入C12,某同学取通入C12后的溶液滴加KSCN溶液,用来证明C12的氧化性比Fe3+强的结论。该实验设计是否合理________(填“是”或“否”),请用简要文字解释你的理由_____________________________________________________________。
(4)若使用20 g黄铜矿粉末可制得8 gFe2O3(铁红),则该黄铜矿中含CuFeS2的质量分数是________ (假设各步反应均完全进行且过程中无额外物质损耗)。
参考答案:(19分)
(1)坩埚(2分)
(2)漂白(2分);氧化(2分)
(3)①MnO2+4H++2Cl? Mn2++Cl2↑2H2O(3分)②b→c→g→h→d(2分)
Mn2++Cl2↑2H2O(3分)②b→c→g→h→d(2分)
③关闭分液漏斗的活塞,将导管插入水中,微热圆底烧瓶,若导管末端产生气泡,停止加热,导管中有一段水柱形成,说明装置不漏气。(3分)
④否(1分),在通氯气前滤液A中就可能含有Fe3+,无法确定Fe3+一定是Fe2+被Cl2氧化得来的。(2分)
(4)92%(2分)
本题解析:(1)固体的焙烧在坩埚内进行。
(2)SO2通入品红溶液,证明SO2具有漂白性;SO2通入H2S溶液,生成S淡黄色沉淀,证明SO2具有氧化性。
(3)①MnO2与浓盐酸反应生成Cl2、MnCl2、H2O。离子方程式为:MnO2+4H++2Cl? Mn2++Cl2↑2H2O
Mn2++Cl2↑2H2O
②生成的Cl2含有HCl、H2O,所以a连接b、c,通过饱和食盐水除去HCl、继续连接g、h,通过浓硫酸,除去H2O,再连接d,即可收集纯净、干燥的氯气。
③利用加热气体膨胀的原理进行装置气密性的检验,所以检验方法为:关闭分液漏斗的活塞,将导管插入水中,微热圆底烧瓶,若导管末端产生气泡,停止加热,导管中有一段水柱形成,说明装置不漏气。
④因为该检验方法是先通入氯气,再滴加KSCN溶液,在通氯气前滤液A中就可能含有Fe3+,无法确定Fe3+一定是Fe2+被Cl2氧化得来的,所以该实验设计不合理。
(4)根据Fe元素守恒可得:2CuFeS2~ Fe2O3,所以该黄铜矿中含CuFeS2的质量分数=8g×368/160÷20g×100%=92%
本题难度:一般
2、选择题 用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列操作会导致测定结果偏低的是?(?)
A.酸式滴定管用蒸馏水洗后未用标准液润洗就装标准液滴定
B.锥形瓶未用待测液润洗
C.读取标准液读数时,滴前仰视,滴定到终点后俯视
D.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失
参考答案:C
本题解析:A中酸式滴定管用蒸馏水洗后未用标准液润洗就装标准液滴定,则盐酸的浓度被稀释,消耗盐酸的体积增加,所以测定结果偏高;B中锥形瓶未用待测液润洗,属于正确的操作要求,不会影响结果;C中读取标准液读数时,滴前仰视,读数偏大。滴定到终点后俯视,读数偏小,所以消耗的盐酸的体积减少,测定结果偏低。D中滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失,说明消耗盐酸的体积增加,所以测定结果偏高,答案选C。
点评:该题是高考中的常见题型和重要考点,属于中等难度试题的考查。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养和方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力。该类试题需要注意的是误差分析的总依据为:由C测==C标V标/V测 由于C标、V待均为定植,所以C测的大小取决于V标的大小,即V标:偏大或偏小,则C测偏大或偏小。
本题难度:简单
3、实验题 请完成有关氨气的问题。
(1)实验室常用下列装置和选用的试剂制取NH3,其中正确的是__________(填序号)。

(2)若实验室收集NH3要采用法__________。
(3)若检验NH3,可用__________。
参考答案:(1)B、D
(2)向下排空气
(3)湿润的红色石蕊试纸变蓝(或用蘸取浓盐酸的玻璃棒,接近容器口,将产生大量的白烟)
本题解析:(1)C装置不对,试管口应略低于试管底部,A装置在试管口部位又生成NH4Cl得不到NH3。(2)NH3易溶于水且比空气轻。(3)利用NH3・H3O易分解生成NH3的性质。
本题难度:简单
4、实验题 (20分)现用质量分数为98%.密度为1.84 g/ml的浓硫酸来配制500ml0.2mol/l的稀硫酸,可供选择的仪器如下;①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙请回答下列问题。
(1)上述仪器中,在配制稀硫酸时用不到的仪器有??(填序号)
(2)经计算,需浓硫酸的体积为?。现有①10ml.②50ml.③100ml三种规格的量筒,你选用的量筒是??(填序号)
(3)将浓硫酸稀释后,冷却片刻,随后全部转移到?ml的容量瓶中,转移时应用玻璃棒?,转移完毕后,用少量蒸馏水洗涤烧杯玻璃棒2~3次,并将洗涤液也转入容量瓶中,在加适量蒸馏水直到液面接近刻线?处。改用?滴加蒸馏水到瓶颈刻度的地方,将溶液振荡,摇匀后,装瓶,贴签。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏高、偏低、无影响填写)
A、容量瓶用蒸馏水洗涤后未干燥_________________;
B、所用的浓硫酸长时间放置在敞口容器内_________________;
C、定容时仰视溶液的凹液面_________________;
参考答案:(20分,每空2分)
(1)②⑦⑧
(2)5.4ml?①
(3)? 500?引流? 1~~2cm?胶头滴管
(4) 无影响,偏低,偏低
本题解析:略
本题难度:一般
5、填空题 用如图所示装置可以收集以下几种气体(烧瓶位置不动)(填字母,下同);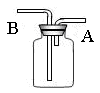
①H2?②SO2?③CH4④ HCl ⑤ NH3?⑥ NO?⑦H2S
(1)若烧瓶是干燥的,则由A口进气,可收集到的气体有?,由B口进气,可收集的气体有?。
(2)若在烧瓶中充满水,可收集的气体有?,气体由?口进入。
(3)若此装置用于净化气体,在烧瓶内装有洗涤液,则混合气体应由?口进入。
参考答案:(1)①③⑤;②④⑦?(2)①③⑥? A?(3)B
本题解析:(1)关键装置图可知,若烧瓶是干燥的,由A口进气收集气体,这说明该气体的密度小于空气的,因此符合条件的是氢气、甲烷和氨气,答案选①③⑤;由B口进气收集气体,这说明该气体的密度大于空气的,因此符合条件的是SO2、氯化氢和H2S,NO极易被氧化,不能用排空气法收集,答案选②④⑦。
(2)若在烧瓶中充满水,收集气体,说明气体不溶于水,和水与不反应,则符合条件氢气、甲烷和NO,则答案选①③⑥,此时气体由A口进入。
(3)当烧瓶中装入洗液,用于洗气时,要使洗气更充分,则气体应从B口进入烧瓶。
点评:该题是高考中的常见题型,属于中等难度试题的考查。试题针对性强,注重答题的灵活性,有利于培养学生的实验能力和实验分析和评价能力。注意收集气体时常根据气体的密度、溶解性等性质,有时还要考虑与氧气的反应等问题,如NO与氧气反应,则只能用排水法收集。
点评:
本题难度:一般