微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在一耐温绝热带透明活塞的容器底部放足量的白磷一块,如下图用力迅速将活塞下压,能观察到的现象是____________________________________,慢慢将手松开,活塞最终回到刻度______________处。该实验说明了什么?
参考答案:白磷自燃,火焰为黄色,生成大量白烟? 4?白磷着火点低;压强增大,气体温度升高;氧气约占空气体积的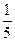
本题解析:本题为理化综合题,要求学生具有较强的学科间综合能力。下压活塞,外界对气体做功,气体内能增加,温度升高,而白磷着火点较低,容易达到着火点引起燃烧。当活塞内氧气耗完,燃烧立即停止,而白磷燃烧现象为黄色火焰并生成大量白烟。
本题难度:简单
2、选择题 向lL0.8mol/L硫酸溶液中加入20.2gKN03和19.2g铜粉,充分反应后产生的气体是 ____,在标准状况下的体积为______,( )
A.氢气2.24L
B.一氧化氮4.48L
C.氢气 4.48L
D.一氧化氮2.24L
参考答案:B
本题解析:酸性条件下,硝酸根离子与金属反应不会产生氢气,A、C错。根据氢离子与硝酸根离子、铜之间反应的离子方程式,可判断出0.2mol硝酸根离子恰好完全反应,所以生成标准状况下NO0.2mol,即4.48L
本题难度:一般
3、填空题 (5分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
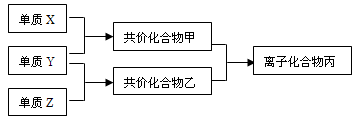
已知:a、常见双原子单质分子中,X分
子含共用电子对数目最多。b、甲分子含
10个电子,且能使湿润的红色石蕊试纸
变蓝,乙分子含18个电子。
(1)X的结构式:?;丙的电子式:?
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
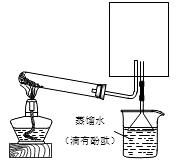
①在图中方框内绘出用烧瓶收集甲的仪器装置简图。
②试管中发生反应的化学方程式是:?
③烧杯中溶液由无色变为红色,其原因是:(用电离方程式表示)
?
参考答案:(1)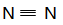 ?
?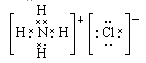 ?
?
(2)①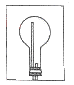 ?②2NH4Cl+Ca(OH)2
?②2NH4Cl+Ca(OH)2 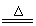 CaCl2+2NH3↑+2H2O?
CaCl2+2NH3↑+2H2O?
③NH3.H2O 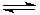 ?NH4++OH-
?NH4++OH-
本题解析:甲分子含10个电子,且能使湿润的红色石蕊试纸变蓝,说明甲是氨气。又因为X分
子含共用电子对数目最多,所以X是氮气,则Y是氢气。乙分子含18个电子,且和氨气发生化合反应,所以乙是氯化氢,则Z是氯气。
(1)氮气中含有氮氮三键,丙是氯化铵,含有离子键和极性键,属于离子化合物。
(2)氨气的密度小于空气的,且极易溶于水,所以用向上排空气法收集氨气。氨气溶于水生成一水合氨,能电离出OH-,溶液显碱性。
本题难度:一般
4、选择题 下列叙述中正确的是
A.酚类中加入浓溴水一定能产生白色沉淀
B.氮化硅陶瓷属于无机非金属材料
C.浓硝酸存放于带橡胶塞的棕色细口瓶中
D.淀粉和纤维素的分子式都是(C6H10O5)n
参考答案:B
本题解析:A. 不一定会有白色沉淀,酚羟基的邻位和对位没有氢原子可取代时,即是不能被溴取代;B.氮化硅陶瓷从元素的角度属于非金属材料,正确;C.浓硝酸会氧化橡胶,应用玻璃塞,错误;D.淀粉和纤维素不能讲分子式为(C6H10O5)n,因为它们的n值不一样,只能说通式。
本题难度:一般
5、填空题 (6分)实验室常加热氯化铵与氢氧化钙固体制取氨气,写出该反应的化学方程式:??,可用?来检验氨气,现要制得2.24L(标况)氨气,理论上需要氯化铵固体?g。(相对原子质量:N-14? H-1 Cl-35.5)
参考答案: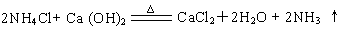 湿润的红色石蕊试纸(或蘸有浓盐酸的玻璃棒),5.35
湿润的红色石蕊试纸(或蘸有浓盐酸的玻璃棒),5.35
本题解析:反应的化学方程式:2NH4Cl+Ca(OH)2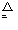 CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑
检验氨气: 湿润的红色石蕊试纸(或蘸有浓盐酸的玻璃棒)
要制得2.24L(标况)氨气即0.1mol,理论上需要氯化铵固体0.2mol,即5.35g。
本题难度:一般