微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定质量的铁铝合金完全溶于过量的热浓硝酸中,反应中共产生13.44LNO2(标况下),若在反应后的溶液中加入足量的氢氧化钠溶液,则生成沉淀的质量不可能为
A.7.8g
B.15.6g
C.21.4g
D.10.7g
参考答案:C
本题解析:铁铝合金与过量的热浓硝酸反应生成硝酸铁和硝酸铝,13.44LNO2(标况下)的物质的量为0.6mol,反应的过程中转移电子的物质的量为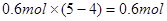 ,假设全部是由铁与热的浓硝酸反应,即参加反应的铁的物质的量为0.2mol,当加入过量的氢氧化钠后,生成的沉淀为氢氧化铁沉淀,其物质的量为0.2mol,质量为21.4g ,所以实际上生成沉淀的质量不可能为21.4g ,应小于21.4g
,假设全部是由铁与热的浓硝酸反应,即参加反应的铁的物质的量为0.2mol,当加入过量的氢氧化钠后,生成的沉淀为氢氧化铁沉淀,其物质的量为0.2mol,质量为21.4g ,所以实际上生成沉淀的质量不可能为21.4g ,应小于21.4g
本题难度:一般
2、选择题 已知P2O5可与冷水反应生成HPO3(偏磷酸),根据其他已学过的知识判断下列叙述正确的是……( )
A.HPO3与H3PO4互为同素异形体
B.P2O5既是磷酸又是偏磷酸的酸酐
C.HPO3与H3PO4互为同位素
D.HPO3与H3PO4都是中等强度的三元酸
参考答案:B
本题解析:A、同素异形体是指由同种元素所形成的不同的单质。
B、P2O5与冷水反应生成偏磷酸,与热水反应生成磷酸,是这两个酸的酸酐。作为酸酐,其中心原子应该与酸中中心原子具有相同的化合价,P2O5具备这个条件。
C、同位素是指同种元素的不同原子。
D、HPO3是一元酸。
本题难度:一般
3、选择题 将磷矿石加工成过磷酸钙的目的是?
A.增加磷的含量
B.使它的性质稳定,便于运输
C.有利于改良土壤
D.使它转化为较易溶于水的物质
参考答案:D
本题解析:磷矿石中磷主要以Ca3(PO4)2形式存在,难溶于水,则难于被植物吸收,将其与一定量浓H3PO4作用制成过磷酸钙即Ca(H2PO4)2,易溶于水,也易被植物吸收。
本题难度:简单
4、填空题 (10分)现正开始使用一种安全气袋以防止汽车撞车时在驾驶室的人因向前冲撞发生意外。这种气袋内装有一种能在高温下分解出气体的混合物。例如有一种配方为:
61%―68%NaN3(叠氮化钠)、0%―5%NaNO3、0%―5%陶土、23%―28%Fe2O3粉、1%―2%SiO2粉、2%―6%石墨纤维。这些粉末经加压成型后,装在一个大袋子里,袋子放在驾驶室座位前。撞车时,约在10毫秒(10-3秒)内引发下列反应: 2NaN3=2Na+3N2(365℃分解)反应在约30毫秒内完成,袋内充满N2气而胀大,阻止人体前冲。在以后的100~200毫秒内气体“ 消失”,所以不致使人反弹,同时袋内的钠变成氧化钠。
消失”,所以不致使人反弹,同时袋内的钠变成氧化钠。
(1)你认为完成上述引发分解、生成气体的“消失”、钠变成氧化钠过程各需上述配方 里哪些物质和起什么作用?。
里哪些物质和起什么作用?。
(2)若气袋内放300g NaN3,在充满氮气时,袋内气体体积为(1大气压,300K)?L 。若袋内气体压力达到4大气压(此时为350K),则袋内气体体积为?L。
(3)配方中Fe2O3的量是如何控制的?。
(4)叠氮离子中有三个氮原子连成直线,N―N键等长(116pm)。写出其电子式?。
(5)怎样做到既使混合物在30毫秒内迅速分解,但又不燃烧、爆炸?。
参考答案:(10分)(1) NaN3分解供产生N2 ,陶土、SiO2吸附N2,Fe2O3使Na 变为Na2O 。
(2)V=6.9×0.082×300=169.7(L)
V=6.9×0.082× 350/4 =49.5(L)
(3) 6Na+Fe2O3=2Fe+3Na2O
(4)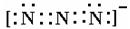 或
或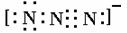
(5)原料粉碎、混匀、成型, 使反应快、扩散快,反应要足够快,使所释放的热“全”用于后续反应,而不使气袋明显升温。
使反应快、扩散快,反应要足够快,使所释放的热“全”用于后续反应,而不使气袋明显升温。
本题解析:略
本题难度:一般
5、选择题 下列反应属于氮的固定的是
①N2和H2在一定条件下反应生成NH3
②雷雨闪电时空气中的N2和O2化合生成NO
③NH3经过催化氧化生成NO
④NH3和HNO3反应生成NH4NO3
A.①③
B.②④
C.③④
D.①②
参考答案:D
本题解析:略
本题难度:简单