微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NaH是离子化合物,与水反应可生成碱和氢气。现有NaH与Al粉混合物共mg,跟足量水反应共收集到氢气的质量为ng,则原混合物中Al粉的质量可能为
A.(12n-m)g
B.(24m-5n)g
C.(36n-3m)g
D.(m-24n/5)g
参考答案:CD
本题解析:依题意,本题可分两种情况讨论,第一种情况NaH过量Al不足。设NaH xmol,Al ymol。
NaH + H2O =" NaOH" + H2↑? 2Al + 2NaOH = 2NaAlO2 + 3H2↑
xmol? xmol? ymol? 1.5ymol
所以? 24x+27y=m?解得? x=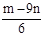 ?则Al的质量为27×
?则Al的质量为27× =(36n-3m)g。
=(36n-3m)g。
2x+3y=n? y=
第二种情况NaH不足,Al过量,设NaH xmol,Al ymol
NaH + H2O =" NaOH" + H2↑? 2Al + 2NaOH = 2NaAlO2 + 3H2↑
xmol? xmol? xmol? xmol? 1.5xmol
则2x+3x=n,x=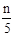 ,所以NaH的质量为(24n/5)g,Al的质量为(m-24n/5)g。
,所以NaH的质量为(24n/5)g,Al的质量为(m-24n/5)g。
答案选CD。
点评:本题难度较大,主要是要进行讨论,当Al过量时,氢气的量由NaOH的量决定。
本题难度:一般
2、选择题 14C是碳的一种同位素,NA为阿伏加德罗常数,下列说法不正确的是
[? ]
A.1mol14CH4分子中所含中子数为8NA?
B.7g14C原子形成的石墨中所含质子数为3NA
C.17g甲基(-14CH3)所含电子数为8NA?
D.标准状况下22.4L14CO2的分子数为NA
参考答案:C
本题解析:
本题难度:简单
3、选择题 25℃时,某硫酸铜溶液的质量分数为w,物质的量浓度为cmol/L,密度为ρg/mL,将此溶液蒸去ag水或再向原溶液中加入bg无水硫酸铜粉末,充分静置并恢复至25℃时,均恰好全部转化为CuSO4・5H2O晶体。则下列关系式正确的是
[? ]
A.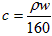
B.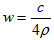
C.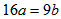
D.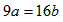
参考答案:C
本题解析:
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是(?)。
A.常温常压下,5.6 g乙烯和环丙烷的混合气体中含有的碳原子数为0.4 NA
B.1 mol Cl2通入足量水中反应转移的电子数为NA
C.0.1 mol・L-1 Na2CO3溶液中CO32-、HCO3-和H2CO3总数为0.1 NA
D.标准状况下,2.24 L三氯甲烷中含有C―Cl数目为0.3 NA
参考答案:A
本题解析:本题以阿伏加德罗常数为载体考查物质的量的计算及有关物质的性质。Cl2与H2O的反应为可逆反应,B项错;溶液体积未知无法求CO32-、
HCO3-和H2CO3总数,C项错;CHCl3在标准状况下为液体,不能用气体摩尔体积计算,D项错。
本题难度:一般
5、选择题 将15g两种金属的混合物投入足量的盐酸中,反应完全后得到H2 11.2L(标准状况)该混合物的组成可能是( )
A.钠和铁
B.镁和铜
C.铝和镁
D.锌和铁