微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 银锌电池广泛用作各种电子仪器的电源,它的充电放电过程可表示为:2Ag+Zn(OH)2=Ag2O+Zn+H2O
回答下列有关问题:
(1)电池的放电过程是______________(填“①”或“②”)。
(2)该电池属于______________ (填“酸”“碱”或“中”)性电池。
(3)反应①是______________ (填“放热”或“吸热”)反应。
(4)写出充电时的电极反应式:
阳极:___________________________________________________________。
阴极:___________________________________________________________。
(5)充电时,电池的正极应接电源的______________极。
(6)试简述回收该种废电池的意义__________________________________________________。
参考答案:
(1)②
(2)碱
(3)吸热
(4) 2Ag+2OH--2e-=Ag2O+H2O? Zn(OH)2+2e-=Zn+2OH-
(5)正
(6)可减少重金属Ag+对环境的污染,又可将Ag回收利用。
本题解析:关键是准确判断①②哪个是放电过程和充电过程。原电池反应是自发反应,由性质可知Ag2O有强氧化性,Zn有强还原性,所以②是自发反应,即放电反应。
本题难度:一般
2、选择题 将含有0.4molNaCl和0.5molCu(NO3)2的水溶液用惰性电极电解一段时间后,在
一个电极上得0.3molCu,则在另一个电极上逸出的气体(标准状况下)的体积是(?)
A.4.48L
B.5.6L
C.6.72L
D.11.2L
参考答案:B
本题解析:电极上得0.3molCu,则该电极为正极,得到电子0.6mol,另一极为负极,负极失电子,根据得失电子守恒,负极也将失去0.6mol电子。根据题意,负极发生的反应有2Cl--2e-=Cl2↑,4OH--4e-=2H2O+O2↑,前者先发生,0.4molNaCl失去0.4mol电子,得到0.2mol氯气,则后一反应失去0.2mol电子,将得到0.05mol氧气,因此逸出的气体(标准状况下)的体积是22.4mol/L×(0.2+0.02)mol=5.6L,选项B正确。
点评:本题考查学生对电解池知识的掌握,明确每个电极所发生的反应是解题的关键,难度较大。
本题难度:简单
3、选择题 下列关于铜电极的叙述,正确的是
[? ]
A.铜锌原电池中铜为负极,发生氧化反应
B.用电解法精炼粗铜时,粗铜作阴极
C.在镀件上电镀铜时,可用精铜作阳极
D.电解稀H2SO4制H2、O2时,可用铜作阳极
参考答案:C
本题解析:
本题难度:一般
4、选择题 某同学按右图所示的装置进行电解实验。下列说法正确的是
 ?
?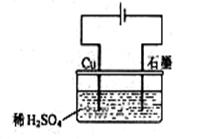
A.电解过程中,铜电极上有H2产生
B.电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑
CuSO4+H2↑
C.电解开始时,石墨电极上有铜析出
D.整个电解过程中,H+的浓度不断增大
参考答案:B
本题解析:电解池的电极反应分别为:
阳极:Cu-2e-=Cu2+
电解初期,溶液中主要是氢离子放电:2H++2e-=H2↑;(而当溶液中铜离子浓度较大时,铜离子才开始放电:Cu2++2e-=Cu)
所以总电解方程式为:Cu+H2SO4 ?CuSO4+H2↑,很容易看出B描述正确。
?CuSO4+H2↑,很容易看出B描述正确。
本题难度:一般
5、填空题 工业上为了处理含有 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬的含量已低于排放标准。请回答下列问题:
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬的含量已低于排放标准。请回答下列问题:
(1)两极发生的电极反应式为:阴极:______________;阳极:__________________。
(2)写出 变为Cr3+的离子方程式:__________________________。
变为Cr3+的离子方程式:__________________________。
(3)工业废水由酸性变为碱性的原因是:___________________________。
(4)_________(填“能”或“不能”)改用石墨电极,原因是______________________。
参考答案:(1)2H++2e-====H2↑? Fe-2e-====Fe2+
(2) +6Fe2++14H+====2Cr3++6Fe3++7H2O
+6Fe2++14H+====2Cr3++6Fe3++7H2O
(3)H+不断放电,且 与Fe2+反应消耗Fe2+,使水的电离平衡被破坏,c(OH-)>c(H+)
与Fe2+反应消耗Fe2+,使水的电离平衡被破坏,c(OH-)>c(H+)
(4)不能?用石墨作电极至Fe2+生成,无法将 还原为Cr3+生成Cr(OH)3而除去
还原为Cr3+生成Cr(OH)3而除去
本题解析:用非惰性电极作阳极电解,铁会失电子,生成的Fe2+具有还原性,与 反应,且反应过程中产生OH-,而使水溶液由酸性变为碱性。
反应,且反应过程中产生OH-,而使水溶液由酸性变为碱性。
本题难度:简单