| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《化学反应与能量》答题技巧(2017年最新版)(四)
参考答案:D 本题解析:A项在人类研究物质微观结构的过程中,先后使用了光学显微镜、电子显微镜、扫描隧道显微镜三种不同层次的观测仪器,A项正确;B项铝硅酸盐形成的分子筛中有许多笼状空穴和通道,常用于分离、提纯气体或液体混合物,还可作干燥剂、离子交换剂、催化剂及催化剂载体等,故B项正确;C项“绿色化学”由美国化学会(ACS)提出,目前得到世界广泛的响应。其核心是利用化学原理从源头上减少和消除工业生产对环境的污染;反应物的原子全部转化为期望的最终产物,故使用可再生资源、提高原子经济性、推广利用二氧化碳与环氧丙烷生成的可降解高聚物等都是绿色化学的内容,C项正确;D.铁盐会水解产生具有吸附性的胶体粒子,可用于饮用水的净化处理,但不能用于饮用水的杀菌消毒,故D项错误;本题选D。 本题难度:一般 2、选择题 下列变化过程中,必需加入氧化剂才能实现的是 参考答案:C 本题解析:分析:必需加入氧化剂才能实现,则选项中的物质为还原剂的变化,还原剂中元素的化合价升高,以此来解答. 本题难度:一般 3、填空题 (12分)已知某反应在不同条件下的反应历程可以表示成下图, |
| 化学键 | H―H | Cl―Cl | O=O | O―H | H―Cl |
| 键能(kJ・mol-1) | 436 | 247 | x | 463 | 431 |
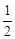 O2(g)=H2O(g) ΔH=" -" 241.8 kJ・mol-1,则x= kJ・mol-1(保留一位小数)。
O2(g)=H2O(g) ΔH=" -" 241.8 kJ・mol-1,则x= kJ・mol-1(保留一位小数)。参考答案:(1)放,减小,D;(2)①496.4 ,
②O2(g)+4HCl(g) =2Cl2(g)+2H2O(g) ΔH=" -" 125.6 kJ・mol-1 555.1
本题解析:(1)依据图象分析反应物的能量大于生成物的能量,反应放热;放热反应升温时,平衡逆向移动,反应物转化率降低;B历程比A历程反应的活化能低,说明加了催化剂;(2)①△H=反应物的总键能-生成物的总键能,则有436+12x-2×431=-241.8,x=496.4;②上述反应的化学方程式为O2(g)+4HCl(g)=2Cl2(g)+2H2O(g),△H=反应物的总键能-生成物的总键能=464.4KJ/mol+4×431KJ/mol-2×247KL/mol-4×463KJ/mol=-125.6KJ/mol,所以,其热化学方程式为:O2(g)+4HCl(g)=2Cl2(g)+2H2O(g)△H=-126.5KJ/mol;上述反应1molO2反应转移4mol电子,反应物的活化能,464.4KJ/mol+4×431KJ/mol=2220.4KJ/mol,所以当有1mol电子转移时吸收的能量为555.1KJ。
考点:考查化学平衡的影响因素,反应热和焓变。
本题难度:困难
4、选择题 分析右面的能量变化示意图,确定下列选项中正确的是( )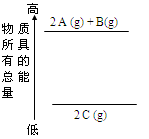
A.2 A(g)+ B(g) = 2 C(g);△H<0
B.2 A(g)+ B(g) = 2 C(g);△H>0
C.2A + B = 2 C;△H<0
D.2C =2 A +B ;△H<0
参考答案:A
本题解析:根据图像可知,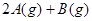 所具的总能量大于
所具的总能量大于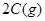 所具有总能量,若
所具有总能量,若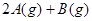 为反应物,
为反应物,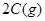 为生成物,则该反应的热化学方程式为:2 A(g)+ B(g) = 2 C(g);△H<0
为生成物,则该反应的热化学方程式为:2 A(g)+ B(g) = 2 C(g);△H<0
本题难度:一般
5、选择题 对于反应H2(g)+Cl2(g)=2HCl(g)的能量变化描述正确的是
A.成键过程中吸收能量
B.断键过程中吸收能量,成键过程中释放能量
C.断键过程中释放能量
D.断键过程中释放能量,成键过程中吸收能量
参考答案:B
本题解析:化学反应H2(g)+Cl2(g)=2HCl(g)为放热反应,断键过程中吸收能量大于成键过程中释放能量,选B。
考点:考查化学反应中的能量变化。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《化学反应速率》高.. | |