��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵���в���ȷ���ǣ�?��
A��Cl2�е���Ԫ�ؾ���ǿ�����ԣ���ԭ��
B��KI�е�Ԫ��ֻ���л�ԭ�ԣ�����������
C��Cl2��NaOH��Һ��Ӧʱ���������������ǻ�ԭ��
D��F2��H2O��Ӧʱ��F2ֻ��������
�ο��𰸣�A
���������Ԫ�ش������̬ʱֻ�������ԣ�������ͼ�̬ʱֻ�л�ԭ�ԣ������м��̬�������������л�ԭ�ԡ�Cl2+2NaOH====NaCl+NaClO+H2O��Cl2�������������ǻ�ԭ����2F2+2H2O====4HF+O2��F2����������
�����Ѷȣ���
2��ѡ���� ����A��ǽ���B����ֱ�ӻ������ɻ�����AxBy���ס�����ͬѧ�ֱ���A��B���ϵ�ʵ�飬ÿ������A��B����������ͬ����������Ϊ12 g���ס�������A��B�����͵õ��Ļ�����AxBy���������£�
?
| A
| B
| AxBy
|
��
| 8 g
| 4 g
| 11 g
|
��
| 7 g
| 5 g
| 11 g
|
��A��B�������ķ�ӦΪ��?��
A.2Cu+O2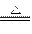 2CuO? B.Fe+S
2CuO? B.Fe+S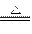 FeS
FeS
C.3Fe+2O2====Fe3O4? D.2Fe+3Cl2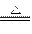 2FeCl3
2FeCl3
�ο��𰸣�B
����������Ƚϼס��ң�������B���������Aʱ��AxByӦ���١��ʼ���A��������Ӧ��AΪ11 g-4 g="7" g����ѡ���������㣬����7��4��ΪB��
�����Ѷȣ���
3������� ������ˮ�к��ж������ӣ�ijУ��ѧ�о���ѧϰС���ͬѧΪ̽������ɣ���������ʵ�飬�ش�
��1������ˮʪ��ĺ�ֽ�е����������Ʊ�����ˮ���۲쵽______����˵��������ˮ�к���______��
��2�����Թ��м��������Ŀ�״̼��ƣ��ټ�������������ˮ����ַ�Ӧ�����������ݲ����������ӷ���ʽ���ʹ�����______��
�ο��𰸣���1����������ˮ������ӦCl2+H2O?HCl+HClO������HClO����Ư���ԣ���ʹ��ɫֽ����ɫ���ʴ�Ϊ��ֽ�ź�ɫ��ȥ��HClO��
��2��������ˮ��Ӧ��������ʹ����ᣬ�����������Ա�̼��ǿ�����������Ա�̼����������̼��������ᷴӦ���ɶ�����̼���壬
��Ӧ������ ����ʽΪCaCO3+2H+�TCa2++CO2��+H2O��
�ʴ�Ϊ��CaCO3+2H+�TCa2++CO2��+H2O��
���������
�����Ѷȣ�һ��
4��ѡ���� ���мס��ҡ�����ƿ�������������ˮ��Ũ�Ⱦ�Ϊ0.1 mol��L-1������ڼ�ƿ�м���������NaHCO3����(m mol)������ƿ�м���������NaHSO3����(m mol)����ƿ���䡣Ƭ�̺ס��ҡ�����ƿ��Һ��HClO�����ʵ���Ũ�ȵĴ�С��ϵ��(��Һ����仯���Բ���(? )
A����=��>��
B����>��>��
C����>��=��
D����>��>��
�ο��𰸣�B
�����������ˮ�д�������ƽ�⣺Cl2+H2O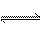 HCl+HClO�����м���NaHCO3��NaHCO3�����ᷴӦ�������ԣ�HCl��H2CO3��HClO������NaHCO3����HCl��Ӧ������HClO��Ӧ������ƽ����HCl�����ģ�ƽ���ƶ���ԭ����ƽ�������ƶ�����Ӧ��������HClO��HClOŨ����������HClO����ǿ�����ԣ���ƿ�У�HClO�ɽ�NaHSO3����������HClOŨ���½�����ƿ��HClOŨ�Ȳ��䡣
HCl+HClO�����м���NaHCO3��NaHCO3�����ᷴӦ�������ԣ�HCl��H2CO3��HClO������NaHCO3����HCl��Ӧ������HClO��Ӧ������ƽ����HCl�����ģ�ƽ���ƶ���ԭ����ƽ�������ƶ�����Ӧ��������HClO��HClOŨ����������HClO����ǿ�����ԣ���ƿ�У�HClO�ɽ�NaHSO3����������HClOŨ���½�����ƿ��HClOŨ�Ȳ��䡣
������������һ���µ��龰�¶Դ���������ʽ����˿��飬�ѶȲ�������Ҫѧ��ȫ����գ��ۺϿ��ǡ�
�����Ѷȣ�һ��
5��ѡ���� ���й���F��Cl��Br��I�ıȽ��У�����ȷ����
A�����ǵ�ԭ�Ӻ�����Ӳ�����ԭ�����������Ӷ�����
B��������±�ص��ʴ�±�������û������Ŀ�������ԭ�����������Ӷ�����
C�����ǵ��⻯����ȶ�����ԭ�����������Ӷ���ǿ
D�����ǵĵ�����ɫ��ԭ�����������Ӷ�����
�ο��𰸣�C
�����������
�����Ѷȣ���