微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一密闭容器中充入一定量的N2和O2,在电火花作用下发生反应N2+O2═2N0,经测定前3s用N2表示的反应速率为0.1mol/(L?s),则6S末N0的浓度为( )
A.1.2?mol?L-1
B.大于1.2?mol?L-1
C.小于1.2?mol?L-1
D.不能确定
参考答案:随反应进行N2浓度降低,反应速率降低,故3s~6s内N2的速率小于0.1mol/(L?s),即6s内N2的速率小于0.1mol/(L?s),速率之比等于化学计量数之比,故v(NO)小于2×0.1mol/(L?s)=0.2mol/(L?s),故6s末NO的浓度小于6s×0.2mol/(L?s)=1.2mol/L,
故选C.
本题解析:
本题难度:一般
2、实验题 教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号
| A溶液
| B溶液
|
①
| 20 mL 0.1 mol·L-1H2C2O4溶液
| 30 mL 0.01 mol·L-1KMnO4溶液
|
②
| 20 mL 0.2 mol·L-1
H2C2O4溶液
| 30 mL 0.01 mol·L-1KMnO4溶液
|

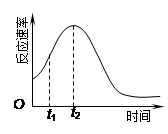
(1) 该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 - (填实验序号)。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),
则在2 min末,c(MnO4-)= mol/L。
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。
(4)小组同学发现反应速率总是如右图,其中t1~t2时间内速 率变快的主要原因可能是:①该反应放热、② 。
参考答案:(1)浓度 ②>①
(2)0.0052
(3)KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间
(4)产物Mn2+(或MnSO4)是反应的催化剂
本题解析:(1)从题中可以看出H2C2O4溶液的浓度不同,KMnO4溶液而的浓度相同,说明该实验探究的是浓度对对化学反应速率的影响,并且浓度越大,反应速率越快,相同时间内针筒中所得CO2的体积为②>①;(2)中,在2 min末收集了4.48 mL CO2(标准状况下),即得到了0.0002mol CO2,根据2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O可知,消耗了0.00004mol MnO4-,则剩下的
(30*0.010/1000)-0.00004=0.00026mol,所以c=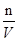 =
= mol/L=0.0052 mol/L;(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;(4)刚开始反应的时候,速率并不快,但是后来逐渐加快,这可能是由于反应放热,或者是生成了具有催化作用的物质,例如Mn2+(或MnSO4)。
mol/L=0.0052 mol/L;(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;(4)刚开始反应的时候,速率并不快,但是后来逐渐加快,这可能是由于反应放热,或者是生成了具有催化作用的物质,例如Mn2+(或MnSO4)。
考点:影响化学反应速率的原因
点评:该题考查了影响化学反应速率的原因,是一道综合题,这有利于提高学生的综合分析能力,但是该题的难度不大,只有最后一个空有点难度,考生在解答这个空时,要联想到催化剂的作用就可以迎刃而解。
本题难度:困难
3、简答题 在2七℃时,向100mL含氯化氢19.6g的盐酸溶液里放入七.60g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2min末,收集到1.12L(标准状况)氢气.在此之后,又经过9min,铁粉完全溶解.则
(1)在前2min?内用FeCl2表示的平均反应速率是______mol?L-1?min-1.
(2)在后9min内用HCl表示的平均反应速率是______mol?L-1?min-1.
参考答案:100mL含氯化氢14.6g的盐酸溶液的浓度c=nV=mMV=14.6g36.5g/mol0.1L=4mol/L,1.12L(标准状况)氢气的物质的量为1.12L22.4L/mol=0.05mol,5.60g纯铁粉物质的量是0.1mol根据题意,2min末,收集到0.05mol氢气时,消耗盐酸的物质的量是0.1mol,生成氯化亚铁是0.05mol,经过4min,0.1mol铁粉完全溶解时,消耗盐酸0.2mol,生成氯化亚铁为0.1mol,则得:
&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp;&n个sp; &n个sp; Fe+2HCl=FeCl2+H2↑
反应前的浓度:4&n个sp;&n个sp;&n个sp;&n个sp; 0
变化浓度:1&n个sp;&n个sp;&n个sp;&n个sp; 0.5
2min末浓度:3&n个sp;&n个sp;&n个sp;&n个sp; 0.5
6min末浓度:2&n个sp;&n个sp;&n个sp;&n个sp;&n个sp; 1
2~6min变化浓度:1&n个sp;&n个sp;&n个sp;&n个sp;&n个sp; 0.5
在前2min&n个sp;内用FeCl2表示的平均反应速率v=△c多=0.5mol/L2min=0.25mol?L-1?min-1,故答案为:0.25;
(2)在后4min内用HCl表示的平均反应速率v=△c多=1mol/L4min=0.25mol?L-1?min-1,故答案为:0.25.
本题解析:
本题难度:一般
4、选择题 下列四种X溶液,均能跟盐酸反应,其中反应最快的是
A.10℃ 20mL 3mol/L的X溶液
B.20℃ 30mL 2molL的X溶液
C.20℃ 10mL 4mol/L的X溶液
D.10℃ 10mL 2mol/L的X溶液
参考答案:C
本题解析:浓度、温度都会影响化学反应速率。温度的影响大于浓度的影响。因此可排除AD选项。在温度都是20℃时,物质的浓度越大,化学反应速率越快。因此反应最快的是20℃ 10mL 4mol/L的X溶液。选项为C。
本题难度:简单
5、选择题 一定温度下,能说明可逆反应: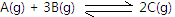 达到限度的是
达到限度的是
A.C的生成速率与A的消耗速率相等
B.单位时间生成n molA,同时生成3n mol B
C.A、B、C的浓度不再变化
D.A、B、C的分子数之比为1:3:2
参考答案:C
本题解析:
正确答案:C
达到限度的是达到平衡状态,化学平衡状态是指在一定条件下的可逆反应里,正反应和逆反应的速度相等,反应混合物中各组成成分的百分含量保持不变的状态。
A、不正确,C的生成速率与A的消耗速率都是正反应速率,此时正反应和逆反应的速度不相等;
B、不正确,单位时间生成n molA,同时生成3n mol B,都是逆反应速率;
D.不正确,A、B、C的分子数之比为1:3:2时,不能说明A、B、C的浓度不再变化,无法确定是否达到平衡状态。
本题难度:一般