��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (1)�����£�0.1 mol��L��1�Ĵ����pH��1�Ĵ����100 mL�ֱ���������п����Ӧ������������ǰ�߱Ⱥ���________(��ࡱ�����١�����ȡ�)��
(2)25��ʱ����pH��5���Ȼ����Һϡ��100����ϡ�ͺ���Һ��pHΪ________(����ĸ����ͬ)��
A��5? B��7? C��3��5֮��? D��5��7֮��
(3)25��ʱ����0.1 mol��L��1�Ĵ�����Һ�м������������ƾ��壬�������ܽ������Һ��pH��________������ĵ����??������ĵ���ƽ�ⳣ��?��ˮ�ĵ���̶�?��
A������? B������C������? D����ȷ��
��4����֪ij�¶���0.01 mol/L HCl��Һ����ˮ�����c(H��)��10��11 mol/L����KW��________�����ڴ��¶��½�pH��a��NaOH��Һ��pH��b�����ᰴ�����1��100��Ϻ���߸պ���ȫ��Ӧ��a��bӦ����Ĺ�ϵΪ________��
��5��������NaHCO3��Һ��PH ?7�����������ԭ���ǣ������ӷ���ʽ��ʾ��??��NaHCO3��Һ������Ũ�ȵĴ�С˳����?
�ο��𰸣���1����?��2��D?��3��A B C A? (4) 10-13 , a+b=15
(5) �� , HCO3-+H2O H2CO3+OH-? C(Na+)��C(HCO3-)��C(OH-)��C(H+)��C(CO32-)
H2CO3+OH-? C(Na+)��C(HCO3-)��C(OH-)��C(H+)��C(CO32-)
���������(1)pH��1�Ĵ�������ʵ���Ũ��ҪԶ����0.1 mol��L��1����������п����Ӧ������������Ҫ�ࡣ
��2����������Һϡ�ͺ����Լ�����pH���ߣ���������ڻ�7
��3��CH3COOH  ?CH3COO�� + H+
?CH3COO�� + H+
�������Һ�м������������ƾ��壬ƽ�����ƣ�����ȼ�С�� H+��С�����Լ�С��ˮ�ĵ���̶���������ƽ�ⳣ��ֻ���¶��йأ��Dz���ı��
��4��ij�¶���0.01 mol/L HCl��Һ����ˮ�����c(H��)��10��11 mol/L������Һ�е�c(OH��)��10��11 KW��10��11��10��2 =10��13���ɹ�ʽ��a+b=13+lg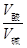 ����a+b=15
����a+b=15
��5����������ʽ�����ˮ�⣬�ϳ�����
�����Ѷȣ�һ��
2������� ij��Һ�п��ܺ���Cl����SO42����NO3����CO32���������ӡ�
��1��������Һ���д���H������ʱ������������������Һ�в����ܴ������ڵ��� ��ԭ���ǣ������ӷ���ʽ��ʾ�� ��
��2��������Һ���д���Ba2������ʱ������������������Һ�в����ܴ������ڵ��� ��
�ο��𰸣���1��CO32�� ��CO32�� + 2H+ = CO2�� + H2O ��2��SO42-��CO32��
�����������1����H����CO32����Ӧ������CO2��H2O�������д���H��ʱ��CO32�������ܴ������ڣ�ԭ��CO32�� + 2H+ = CO2�� + H2O ��2��������Һ���д���Ba2������ʱ��SO42-��CO32�����䷴Ӧ����BaSO4��BaCO3�����Բ����ܴ������ڵ���SO42-��CO32��
���㣺���ӹ������⡣
�����Ѷȣ�һ��
3��ѡ���� ij��Һ�п��ܺ���K����NH4����Ba2����SO42����I����CO32�����ֱ�ȡ��������pH�Ʋ��ԣ���Һ�������ԣ��ڼ���ˮ��CCl4���ã��²����ɫ��Ϊȷ������Һ����ɣ���������������? (����)��
A��K��
B��SO42��
C��Ba2��
D��NH4��
�ο��𰸣�A
����������ɢ�֪��Һ�в�����CO32�����ɢ�֪��Һ�в�����I����������Һ�ʵ����ԣ����ж�SO42��һ�����ڣ���Ba2�������ڡ���Һ�����ԣ���NH4�����ڡ���K���Ƿ���ڣ�������顣
�����Ѷȣ�һ��
4��ѡ���� ����Һ�м�������Na2O2�����ܴ���������������ǣ� ����
A��NH4����Ba2����Cl����NO3��
B��K����AlO2����Cl����SO42��
C��Ca2����Mg2����NO3����HCO3��
D��Na����Cl����CO32����SO32��