��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� [ѡ��һ��ѧ�뼼��]����������Ƽ���Ͱ�����������̼�Ҫ��ʾ����ͼ��
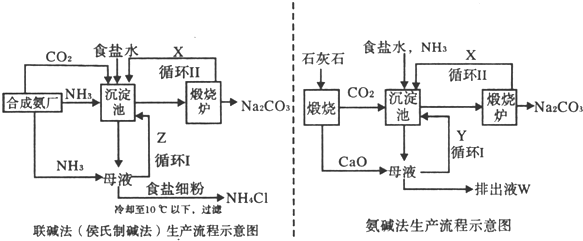
��1���������з�����Ӧ�Ļ�ѧ����ʽΪ______��
��2��X��______��Y��______?���ѧʽ����
��3��Z�г����ܽ�İ�����ʳ���⣬�������ʻ���______���ų�Һ�е����ʳ������������⣬����______��
��4���������Ϸ������ڰ������������______?�����Ҫ����������Ҫ�������䰱������ԭ�ϵ���Ʒ������ܷ�Ӧ�����û�ѧ����ʽ��ʾ����дΪ______��
��5����������д�ĸҺ����ȡ�Ȼ�茶���Ĺ����Ʋ⣬���ý�����ȷ��______��
a������ʱ�Ȼ�淋��ܽ�ȱ��Ȼ���С
b��ͨ�백��Ŀ����ʹ�Ȼ�笠�������
c������ʳ��ϸ��Ŀ�������Na+��Ũ�ȣ��ٽ�̼�����ƽᾧ����
��6������У�ÿ��ͨ��NH3?44.8L�����ۺϳɱ�״���£�ʱ���Եõ�����100.0g��NH3��������Ϊ______������ڰ����ָ�������һ���ŵ�______?
�ο��𰸣���1����������ͼ������֪��������������Ͱ�����������г������з����ķ�Ӧ�ǰ�����������̼��ˮ���Ȼ��Ʒ�Ӧ����̼�����ƾ�����Ȼ�泥����Է�Ӧ�Ļ�ѧ����ʽΪ��NaCl+NH3+CO2+H2O�TNaHCO3��+NH4Cl���ʴ�Ϊ��NaCl+NH3+CO2+H2O�TNaHCO3��+NH4Cl��
��2�������������ͼ�з���ѭ��������̼�����Ʒֽ����ɵĶ�����̼���壻���������������ѭ�����������ƺ�ˮ��Ӧ�����������ƣ�������������η�Ӧ���ɵİ�������ѭ��ʹ�ã��ʴ�Ϊ��CO2��NH3��
��3���������������е����ʷ����ķ�Ӧ���������ĸҺ��Ҫ���Ȼ�李�̼���ơ�̼�����ơ��Ȼ��ƣ�Z�г����ܽ�İ�����ʳ���⣬�������ʻ����Ȼ�李�̼���ƣ�����ų�Һ�е����ʳ������������⣬�����������ƺ��Ȼ�立�Ӧ���ɵ��Ȼ��ƣ��Ȼ��ƣ��ʴ�Ϊ��Na2CO3��NH4Cl��CaCl2��NaCl��
��4���������Ϸ�����������������У�ĸҺ�м��������Ʒ�Ӧ�����������ƻ��������ɰ�������Ӧ�����а���ת��Ϊ��Σ����ת��Ϊ����������ѭ��ʹ�ã�����Ҫ���䰱����
NaCl+NH3+CO2+H2O�TNaHCO3��+NH4Cl��CaCO3�TCaO+CO2����CaO+H2O�TCa��OH��2��Ca��OH��2+2NH4Cl�TCaCl2+2NH3��+2H2O��2NaHCO3�TNa2CO3+H2O+CO2���ϲ��õ��ܻ�ѧ����ʽΪ��CaCO3+2NaCl�TNa2CO3+CaCl2���ʴ�Ϊ������Ҫ��CaCO3+2NaCl�TNa2CO3+CaCl2��
��5������д�ĸҺ����ȡ�Ȼ�茶���Ĺ����У�
a����ʱ�Ȼ�淋��ܽ�ȱ��Ȼ��ƴ�a����
b��ͨ��������������NH4+��Ũ�ȣ�ʹNH4Cl�����������ʹNaHCO3ת��ΪNa2CO3�����������NH4Cl���ȣ���b��ȷ��
c������ʳ��ϸ��Ŀ�������Cl-��Ũ�ȣ��ٽ��Ȼ�什ᾧ��������c����
�ʴ�Ϊ��b��
��6������з����ķ�ӦΪ��NaCl+NH3+CO2+H2O�TNaHCO3��+NH4Cl��2NaHCO3�TNa2CO3+H2O+CO2����ÿ��ͨ��NH3?44.8L�����ۺϳɱ�״���£����ʵ���Ϊ2mol�����������еõ�����100.0g�����ʵ���Ϊ100g106g/mol=5053mol����Ҫ���������ʵ���Ϊ5053��2=10053mol����NH3��������=10053mol2mol��100%=94.3%��
�����Ƽ�백��Ƚϣ��������ŵ���ʹʳ�ε���������ߵ�96%���ϣ�Ӧ��ͬ����ʳ�αȰ����������Ĵ���������ۺ������˰����Ķ�����̼�ͼ�������ӣ�ͬʱ�����������ֿɹ�IJ�Ʒ--������Ȼ�泥��������ķ���������̼��ת��Ϊ�����Ҫԭ������ȡ��������ͽ�ʡ�˼��������ȡ������̼���Ӵ��ʯ��Ҥ����������õijɷ������ӣ�Cl-��������۸�ϸߵ�����̶�������İ�����ȡ�����Ȼ�泥��Ӷ���������û�ж���ô��������ڴ������Ȼ��ƣ������˶Ի�������Ⱦ�����Ҵ���˴���͵��ʵijɱ�����������˴��ģ������������Խ�ԣ�
�ʴ�Ϊ��94.3%�����������õ�CaCl2�������ʳ�ε�ת���ʣ�
���������
�����Ѷȣ�һ��
2��ѡ���� �����й�˵�����������?
[? ]
A��������������������γ��������Ҫ����
B����ҵ�ϳɰ�����NH3�ƻ���(NH4)2SO4�����ڵ��Ĺ̶�?
C��һ�������£�þ����һЩ�ǽ��������ﷴӦ��������һЩ���������ﷴӦ
D�������к��й����ƺͶ�������
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� �йغϳɰ���ҵ��˵���У���ȷ����
[? ]
A���Ӻϳ��������Ļ�����壬����NH3ֻռ15%�������������Ĺ�����Ч�ʶ��ܵ�
B�����ڰ���Һ����N2��H2��ʵ����������ѭ��ʹ�ã�����������˵���IJ��ʺܸ�
C���ϳɰ���ҵ�ķ�Ӧ�¶ȿ�����500�棬Ŀ����ʹ��ѧƽ��������Ӧ�����ƶ�
D���ϳɰ������õ�ѹǿ��2��107Pa~3��107Pa����Ϊ��ѹǿ������ý�Ļ������
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����
[? ]
A�����ϴ�����ֽ������Ʒ�������л�����Ʒ
B���ϳɰ���ҵ��Ӵ�����������SO2�������Ĺ��̶������˸�ѹ����������
C����ҽԺ��Ϊ���ж�������ҺӦ����0.9%�Ȼ����Һ
D��ҹ���������ú��й©ʱ��Ӧ�������Ƽ��ú��й©ԭ���������Ŵ�ͨ��
�ο��𰸣�A
���������
�����Ѷȣ���
5��ѡ���� ���й��̲����ڵ��Ĺ̶�����
[? ]
A. N2��NO
B. NH3��NH4NO3
C. N2��NH3
D. N2 NO3-
NO3-
�ο��𰸣�B
���������
�����Ѷȣ���