��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵������ȷ���ǣ�������
A������Ԫ�ص�������������һ��С��4
B������������Ϊ3��Ԫ�ز�һ��������Ԫ��
C��ͬ����������������ڵ�Ԫ��ԭ������֮�һ������18
D�������ڼ�������R2-����Rһ������VIA��
�ο��𰸣�A������Ԫ�ص����������������С��4��������Ԫ�ص��������������ڻ����4�����顢�ǵȣ���A��ȷ��
B������������Ϊ3��Ԫ��һ��������Ԫ�أ�ns�ܼ�����С�ڣ�n-1��d�ܼ�����������Ԫ������������С�ڻ����2����B����
C��ͬ����������������ڵ�Ԫ��ԭ������֮�һ������18�����ܵ���8����Na��KԪ�ص�ԭ����������8����C��ȷ��
D�������������������Ų���ns2np6��HԪ�س��⣩�������ڼ�������R2-��˵��RԪ�ص�2�����Ӵﵽ�ȶ��ṹ������Rһ������VIA�壬��D��ȷ��
��ѡB��
���������
�����Ѷȣ���
2������� �٢ڢۢܢݢ�����Ԫ�أ���Ԫ�����ڱ��е�λ����ͼ��ʾ���ش��������⣺
| ��A | | | | | | | | 0
��
��A | ��
��A
��A
��A
��A
��A
��
��
��
��
��
|
��1������Ԫ���У���������ǿ��Ԫ��λ��λ��Ԫ�����ڱ�______����Ԫ�صĵ�����ˮ��Ӧ�����ӷ���ʽΪ______��
��2��Ԫ�آٺ͢ڿ����γ��ڶ�Ļ������������ǣ�д����ʽ��______����û��������������ͬ����ԭ�ӷ��ӵĽṹʽΪ______��
��3������Ԫ�آ۵�ԭ�ӽṹʾ��ͼ______����Ԫ���γɵ���̬�⻯��ͨ�������ܽ���ˮ����ԭ����______��
��4��д��Ԫ�آܡ�������������Ӧˮ�������Ӧ�����ӷ���ʽΪ______��
�ο��𰸣���1�����ڱ��У�ͬ����Ԫ�ش�����Ԫ�صĽ�����������ͬ����Ԫ�ش��ϵ���Ԫ�صĽ���������ǿ�����������ǿ��Ԫ��ӦΪNa��λ�ڵ������ڢ�A�壬��Ԫ�صĵ�����ˮ��Ӧ�����ӷ���ʽΪ2H2O+2Na�T2Na++2OH-+H2����
�ʴ�Ϊ���������ڢ�A�壻2H2O+2Na�T2Na++2OH-+H2����?
��2���ٺ͢ۿ����γ��ڶ�Ļ�����Ϊ�������������ΪCH4�������ʽΪ
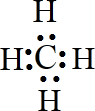
����CH4����������ͬ����ԭ�ӷ�����H2O����ṹʽΪH-O-H��
�ʴ�Ϊ��
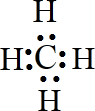
��H-O-H��
��3��Ԫ�آ�ΪNԪ�أ�ԭ�Ӻ�����2�����Ӳ㣬����������Ϊ5��ԭ�ӽṹʾ��ͼΪ
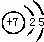
����Ԫ���γɵ���̬�⻯��ΪNH3��NH3�Ǽ��Է��ӣ�����ˮ��Ӧ����ˮ�������γ���������ԣ�ͨ�������ܽ���ˮ��
�ʴ�Ϊ��
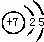
��NH3�Ǽ��Է��ӣ�����ˮ��Ӧ����ˮ�������γ������
��4��Ԫ�آܡ������������ֱ�ΪNaOH��HClO4��Ϊǿ�ǿ�ᣬ���ӷ�Ӧ����ʽΪH++OH-�TH2O��
�ʴ�Ϊ��H++OH-�TH2O��
���������
�����Ѷȣ�һ��
3��ѡ���� A��B��C���ֶ�����Ԫ�������ڱ��е����λ������ͼ��ʾ����֪A��C�ֱ���B�γɻ�����X��Y��A��B��������֮�͵���C����������������˵���ж���ȷ����?

[? ]
A. B��C��������ͬ��������
B. Xһ��������������
C. B���⻯���A��C���⻯���ȶ�
D. Y��NaOH��Һ��Ӧֻ������������
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ������˳���д������
A.���Ӱ뾶��S2-��Cl-��K+��Ca2+
B.���ȶ��ԣ�HI��HBr��HCl��HF
C.��������ϼۣ�C��N��O��F
D.���ԣ�Al(OH)3��Mg(OH)2��Ca(OH)2��KOH
�ο��𰸣�C
���������
�����Ѷȣ�����
5���ƶ��� V��W��X��Y��Z��ԭ���������εݼ������ֳ���Ԫ�ء�XԪ���ǵؿ��к�������Ԫ�أ�Y��Z�����̬������M��ˮ��Һ�ʼ��ԣ�W�ĵ�����X2��ȼ�յIJ����ʹƷ����Һ��ɫ��V��һ����ʷ�ƾã�Ӧ�ù㷺�Ľ���Ԫ�ء���ش�
(1)YԪ�������ڱ��е�λ����___________��д��X��Z����Ԫ����ɵĻ������һ����;��__________
(2)����������Ԫ������������γɵĻ������У���һ����������ˮ��Ӧ��������������������ԭ��Ӧ����д���÷�Ӧ�Ļ�ѧ����ʽ��________________________
(3)X��Y��Z����Ԫ�ؿ����һ��ǿ��U��M���ʵ������±�U��������һ���Ρ����ε�ˮ��Һ��pH
____������ڡ���С�ڡ����ڡ���7��
(4)����V����Ͷ�뵽������Һ�У�������dz��ɫ��ҺN��N��������Һ��˫��ˮ��Ӧ�����ӷ���ʽ��
______________________��
(5)��������Ѱ����ʵĴ����͵缫���ϣ���Y2��Z2Ϊ�缫��Ӧ���HCl-NH4Cl��ҺΪ�������Һ��������ȼ�ϵ�أ���д���õ�ص�������Ӧʽ��__________________���ŵ�ʱ��Һ��H+����_______��������� ������������
(6)W(s)+O2(g)=WO2(g) ��H1��W(g)+O2(g)=WO2(g) ��H2 ���H1___���>����<����=������H2��
�ο��𰸣�(1)��2����VA�壻��ɫ������(H2O2)���ܼ�(H2O)
(2)3NO2+H2O=2HNO3+NO
(3)��
(4)2Fe2++H2O2+2H+=2Fe3++2H2O
(5)N2+6e-+8H+=2NH4+����
(6)>
���������
�����Ѷȣ�һ��