微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有一包白色固体物质,可能含有CuSO4、Na2SO4、KNO3、Na2CO3、NH4Cl中的一种或几种,现进行如下实验:
(1)将白色固体溶于水中,得到无色透明溶液。
(2)取少量上述溶液两份,其中一份滴加BaCl2溶液,立即产生白色沉淀,再加入稀硝酸,沉淀没有溶解。另一份溶液中滴加NaOH溶液,加热,产生刺激性气味的气体。
(1)根据以上实验现象可知,该白色固体中一定含有____________,一定没有__________,可能有______________。
(2)写出产生气体的反应方程式________________________。
参考答案:(1)Na2SO4、NH4Cl;CuSO4、Na2CO3;KNO3
(2)NH4Cl+NaOH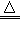 NH3↑+NaCl+H2O
NH3↑+NaCl+H2O
本题解析:
本题难度:一般
2、填空题 为达到预期的实验目的,下列操作正确的是
[? ]
A.配制0.1mol/L的盐酸500mL,应选用的仪器有胶头滴管、烧杯、玻璃棒、天平、500mL容量瓶
B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸
C.为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量
D.测定硫酸铜晶体中结晶水含量, 加热坩埚中晶体完全失水后需在空气中冷却,再称量
参考答案:C
本题解析:
本题难度:一般
3、实验题 有一包白色粉末,可能是由Al2(SO4)3、CuCl2、KNO3、Na2O中的一种或几种组成的。为了探究它的成分,某学习小组做了如下实验。
①取适量白色粉末投入蒸馏水中,粉末完全溶解,得到蓝色透明溶液A。
②取A溶液少量,向其中逐滴滴加烧碱溶液直到过量,观察到先有沉淀出现,而后沉淀逐渐增多,然后沉淀又逐渐减少,但最终仍有部分蓝色沉淀。
③再取A溶液两份,一份滴加BaCl2溶液后,出现白色沉淀;另一份滴加硝酸银溶液后也出现白色沉淀。 请回答下列问题:
(1)原白色粉末一定含有____________,一定不含____________, 可能含有____________。(填化学式)
(2)写出过程②中涉及到的离子方程式:________________________
(3)如果要进一步确定可能存在的物质,应该进行的实验操作是:
____________________________________
参考答案:(1)CuCl2和Al2(SO4)3;Na2O;KNO3
(2)Cu2++2OH-==Cu(OH)2↓、Al3++3OH-==Al(OH)3↓、Al(OH)3+OH-==AlO2-+2H2O
(3)用洁净的铂金丝蘸取原样品在酒精灯火焰上灼烧,透过蓝色钴玻片观察火焰颜色,若为紫色则含有KNO3,否则不含
本题解析:
本题难度:一般
4、填空题 某无色澄清溶液中可能存在下述几种离子:H+、Na+、Ba2+、Cu2+、Ag+、SO42-、CO32-、Cl-、F-、Br-.取该溶液进行下述实验:①用pH试纸检验,该溶液呈强酸性;②取部分溶液,滴入几滴氯水,再加入少量四氯化碳,振荡后静置,四氯化碳层呈橙红色;③另取部分溶液逐滴加入NaOH溶液,使溶液由酸性逐渐呈碱性,然后再加入Na2CO3溶液,有白色沉淀生成.根据上述实验判断:
(1)肯定存在的物质有______;
(2)肯定不存在的物质有______;
(3)可能存在的物质有______.
参考答案:由“无色澄清溶液”可知,原溶液一定没有Cu2+;
①用pH试纸检验,该溶液呈强酸性;排除与强酸反应的F-、CO32-离子存在,阴离子可能是Cl-、SO42-;
②取部分溶液,滴入几滴氯水,再加入少量四氯化碳,振荡后静置,四氯化碳层呈橙红色;说明溶液中一定存在Br-,一定不存在Ag+,
③另取部分溶液逐滴加入NaOH溶液,使溶液由酸性逐渐呈碱性,然后再加入Na2CO3溶液,有白色沉淀生成,证明一定存在Ba2+,所以一定不存在与钡离子反应的SO42-,再结合①溶液为强酸性溶液,一定存在Cl-,
通过以上分析,该溶液中肯定存在的离子有:H+、Ba2+、Br-;肯定不存在的离子有:CO32-、F-、Cu2+、SO42-、Ag+;可能存在的离子有:Na+、Cl-,
故答案为:H+、Ba2+、Br-;CO32-、F-、Cu2+、SO42-、Ag+;Na+、Cl-.
本题解析:
本题难度:一般
5、简答题 有三瓶标签脱落的无色透明溶液,分别是稀盐酸、稀硫酸和稀硝酸.请你帮助实验老师设计两种方法鉴别它们,并贴上标签.
| ?操?作?步?骤 | 现?象?及?结?论
方法一
方法二
参考答案:根据盐酸与硝酸银反应生成难溶于水的AgCl沉淀,硫酸与BaCl2反应生成BaSO4沉淀,以及硝酸具有强氧化性可设计两种实验方案:
方案一:可加入BaCl2溶液鉴别出稀硫酸,再加入AgNO3溶液,生成沉淀的为盐酸;
方案二:根据硝酸具有强氧化性,与铜反应生成NO气体,剩余两种溶液加入BaCl2溶液,生成沉淀的是硫酸.
故答案为:?操?作?步?骤现?象?及?结?论方法一(1)各取少量溶液于试管中,分别滴加BaCl2溶液
(2)各取剩余的两种溶液于试管中,分别滴加AgNO3溶液(1)产生白色沉淀的是稀硫酸
(2)产生白色沉淀的是稀盐酸,剩余的是稀硝酸方法二(1)各取少量溶液于试管中,分别加入铜片
(2)各取剩余的两种溶液于试管中,分别滴加BaCl2溶液(1)有气泡产生的是稀硝酸
(2)产生白色沉淀的是稀硫酸,剩余的是稀盐酸
本题解析:
本题难度:一般
|