微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)Co2(OH)2CO3和Co(CH3COO)2・nH2O均是生产高比能锂电池正极材料的前驱体。
(1)这两种钴的化合物中钴的化合价为 。
(2)Co2(OH)2CO3在空气中充分加热生成四氧化三钴,该反应的化学方程式为 。
(3)为确定Co(CH3COO)2・nH2O中的n值及其热分解过程,取一定量的样品在氮气氛围中加热,样品的固体残留率( )随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
)随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
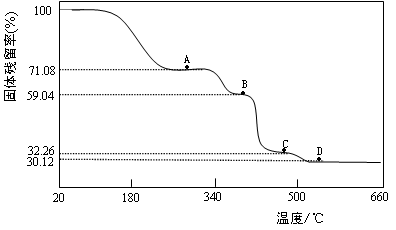
①Co(CH3COO)2・nH2O晶体中n= (填自然数)。
②A→B点反应释放的气体为纯净物(由两种元素组成),该气体的结构简式为 。
③B→C点反应释放CO、CO2两种气体,n(CO)∶n(CO2)= 。
④D点残留固体的化学式为 。(列出上述计算过程)
参考答案:(1)+2 (2分);(2)3Co2(OH)2CO3 + O2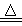 2Co3O4 +3CO2 +3H2O (2分)
2Co3O4 +3CO2 +3H2O (2分)
(3)①4 ② CH3CH3 ③2∶1 ④CoO(共8分,每空2分)
本题解析:(1)根据化合物中正负化合价的代数和是0 的原则可知:在这两种钴的化合物中钴的化合价为+2价;(2)Co2(OH)2CO3在空气中充分加热生成四氧化三钴,根据电子守恒及元素的原子守恒可得该反应的化学方程式为3Co2(OH)2CO3 + O2 2Co3O4+3CO2 +3H2O;(3)在晶体中Co(CH3COO)2・nH2O结晶水与固体残留物的质量成正比,18n:(177+18n)=(100-71.08):100,解得n=4;故原化合物为Co(CH3COO)2・4H2O,其相对分子质量为249; ②
2Co3O4+3CO2 +3H2O;(3)在晶体中Co(CH3COO)2・nH2O结晶水与固体残留物的质量成正比,18n:(177+18n)=(100-71.08):100,解得n=4;故原化合物为Co(CH3COO)2・4H2O,其相对分子质量为249; ② 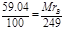
 MrB = 147,减少的物质相对分子质量为177-147=30,因是纯净物该气体只能为乙烷,结构简式是CH3CH3;B处的剩余固体为CoC2O4;③
MrB = 147,减少的物质相对分子质量为177-147=30,因是纯净物该气体只能为乙烷,结构简式是CH3CH3;B处的剩余固体为CoC2O4;③ 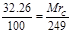 Mrc= 80.33,故为Co3O4,3CoC2O4
Mrc= 80.33,故为Co3O4,3CoC2O4 Co3O4+4CO↑+ 2CO2↑,故n(CO)∶n(CO2)=2∶1; ④
Co3O4+4CO↑+ 2CO2↑,故n(CO)∶n(CO2)=2∶1; ④ 
 MrD="75" ,故为氧化钴,化学式是CoO。
MrD="75" ,故为氧化钴,化学式是CoO。
考点:考查物质的分解产物、得到的固体化学式的确定的知识。
本题难度:困难
2、简答题 实验室使用的浓盐酸的溶质质量分数一般为36.5%,密度1.19g/cm3.
(1)将______升氯化氢(标准状况)通入1.00L水中可以得到36.5%的浓盐酸?
(2)该浓盐酸的物质的量浓度为______.
参考答案:(1)令需要氯化氢的体积为VL,则HCl的物质的量为VL22.4L/mol=V22.4mol,故HCl的质量为V22.4mol×36.5g/mol=36.5V22.4g,1.00L水的质量为1L×1000g/L=1000g,故溶液的质量为(1000+36.5V22.4)g,故(1000+36.5V22.4)g×36.5%=36.5V22.4g,解得:V=352.8L,
故答案为:352.8;
(2)质量分数为36.5%,密度1.19g/cm3的浓盐酸的物质的量浓度为1000×1.19×36.5%36.5mol/L=11.9mol/L,
答:该浓盐酸的物质的量浓度为11.9mol/L.
本题解析:
本题难度:一般
3、选择题 标准状况下,ag气体A与bg气体B的分子数相同,下列说法错误的是( )
A.气体A与气体B的密度之比为a:b
B.气体A与气体B的相对分子质量之比为a:b
C.相同质量的气体A与气体B的物质的量之比为a:b
D.相同体积的气体A与气体B的质量之比为a:b
参考答案:ag气体A与bg气体B的分子数相同,根据N=nNA可知,二者物质的量相等,根据M=mn可知A与B的摩尔质量之比为a:b,
A.同温同压下,两气体的密度之比摩尔质量之比为a:b,故A正确;
B.相对分子质量之比等于摩尔质量之比为a:b,故B正确;
C.根据M=mn可知,相同质量的气体A与气体B的物质的量之比为1a:1b=b:a,故C错误;
D.相同状况下,同体积的气体A与B,二者物质的量相同,质量之比等于摩尔质量之比为a:b,故D正确;
故选:C.
本题解析:
本题难度:一般
4、选择题 设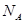 表示阿伏加德罗常数,下列叙述中正确的是?
表示阿伏加德罗常数,下列叙述中正确的是?
①.31g白磷含有的P―P键数为NA?
②. 1mol CH3+(碳正离子)中含有电子数为10NA?
③. 1mol铜与足量硫蒸气反应,转移电子数为2NA?
④.1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2NA个电子?
⑤.用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过的电子数为NA?
⑥.0.84 g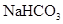 晶体中阳离子和阴离子总数为0.03NA?
晶体中阳离子和阴离子总数为0.03NA?
⑦.3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA?
⑧.标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA?
⑨.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023?
⑩.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
A ②④⑦⑧? B ③④⑥⑦⑧? C ④⑦? D④⑥⑨⑩
参考答案:C
本题解析:①在一个白磷P4分子中含有6个P―P共价键,所以.31g白磷含有的P―P键数为31g ÷(31×4)g/mol×NA=1.5NA.错误. ②. 1molCH3+(碳正离子)中含有电子数为9NA .错误. ③由于S的氧化性弱,在与Cu反应时1个S只能得到1个电子,所以 1mol铜与足量硫蒸气反应,转移电子数为NA。错误。④Mg是+2价的金属,因此1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2NA个电子。正确。⑤.用惰性电极电解CuCl2溶液,实质就是电解CuCl2本身。若阴极析出16g铜时,n(Cu)=16g÷64g/mol=0.25mol,Cu是+2价的金属,所以线路中通过的电子是0. 5mol,即电子数为0. 5NA。错误。⑥电离方程式为NaHCO3=Na++HCO3-,0.84 g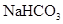 的物质的量0.01mol,所以在晶体中阳离子和阴离子总数为0.02NA.错误。⑦3.9gNa2O2的物质的量为0.05mol,每有1mol的Na2O2吸收足量的CO2时转移电子1mol,所以0.05mol的Na2O2反应转移的电子数是0.05NA。正确。⑧反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O.若有1mold Cu反应,产生NO21mol。n(Cu)=3.2g÷64g/mol=0.05mol,所以在标准状况下,3.2g铜Cu与足量的浓硝酸反应生成的气体含有的分子数是0.05NA.错误。⑨C16O相对分子质量是28,28 g C16O的物质的量为1mol,含有质子数是14×6.02×1023?;C18O相对分子质量是30,28 g C18O中含有的质子的物质的量小于1mol,因此含有的质子数小于14×6.02×1023。错误。⑩.标准状况下,22.4 L氯气的物质的量为1mol,反应方程式为 Cl2+2NaOH=NaCl+NaClO+H2O。所以1mol的氯气与足量氢氧化钠溶液反应转移的电子数为1×6.02×1023 .错误。因此正确的说法是④⑦,选项为C。
的物质的量0.01mol,所以在晶体中阳离子和阴离子总数为0.02NA.错误。⑦3.9gNa2O2的物质的量为0.05mol,每有1mol的Na2O2吸收足量的CO2时转移电子1mol,所以0.05mol的Na2O2反应转移的电子数是0.05NA。正确。⑧反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O.若有1mold Cu反应,产生NO21mol。n(Cu)=3.2g÷64g/mol=0.05mol,所以在标准状况下,3.2g铜Cu与足量的浓硝酸反应生成的气体含有的分子数是0.05NA.错误。⑨C16O相对分子质量是28,28 g C16O的物质的量为1mol,含有质子数是14×6.02×1023?;C18O相对分子质量是30,28 g C18O中含有的质子的物质的量小于1mol,因此含有的质子数小于14×6.02×1023。错误。⑩.标准状况下,22.4 L氯气的物质的量为1mol,反应方程式为 Cl2+2NaOH=NaCl+NaClO+H2O。所以1mol的氯气与足量氢氧化钠溶液反应转移的电子数为1×6.02×1023 .错误。因此正确的说法是④⑦,选项为C。
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值。下列说法错误的是
A.1mol Na作为还原剂时可提供的电子数为NA
B.标准状况下,22.4L氯气中所含的氯原子数为2NA
C.0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
D.18g水中所含的电子数为10NA
参考答案:C
本题解析:A 对 钠化合价由0价升高到+1价,失去1mol电子
B 对 标况下,22.4L氯气为1mol,含的氯原子数为2NA
C 错没有给溶液体积,无法求Cl-个数
D 对18g水为1mol,含电子数为10NA
本题难度:一般