��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��100ml?0.3mol/L�������300ml?0.25mol/L�������Ϻ��ˮϡ�͵�500ml�����Һ��H+���ʵ���Ũ��Ϊ
A.0.26mol/L
B.0.36?mol/L
C.0.45?mol/L
D.0.56?mol/L
�ο��𰸣�B
���������������0.3mol/L��������������Ũ��Ϊ0.3mol/L��0.25mol/L��������Һ��������Ũ��Ϊ0.5mol/L����Ϻ���Һ�е�������Ϊ���������Ậ�е�������֮�ͣ��ݴ˼��㣮
���0.3mol/L��������������Ũ��Ϊ0.3mol/L��0.25mol/L��������Һ��������Ũ��Ϊ2��0.25mol/L=0.5mol/L����Ϻ���Һ�е�������Ϊ���������Ậ�е�������֮�ͣ����Ϻ�������Ũ��Ϊc����
0.1L��0.3mol/L+0.3L��0.5mol/L=0.5L��c��
���c=0.36?mol/L��
��ѡB��
���������⿼�����ʵ���Ũ�ȵ��йؼ��㣬�ѶȲ���ע��Թ�ʽ������Խ������ã�
�����Ѷȣ���
2��ѡ���� ����˵������ȷ����
A.�����һ������Ļ�ѧ�������㷺�ش�������Ȼ����
B.P4��CH4����������������Ҽ��Ƕ�Ϊ109o28�@
C.�з��ӹ��ɵ�������һ�����й��ۼ�
D.�γɹ��ۼ���Ԫ�ز�һ���Ƿǽ���Ԫ��
�ο��𰸣�D
���������
�����Ѷȣ���
3��ѡ���� ���б仯���л�ѧ�����ƻ����л�ѧ�����γɵ���
A.������
B.���ڻ�
C.Ũ����ӷ�
D.NH4Cl���ȷֽ�
�ο��𰸣�D
���������A��B���������������仯����ѧ����û�б��ƻ���Ҳû���γɻ�ѧ����CҲ�������仯��û���ƻ���ѧ�������γ��˻�ѧ����D�ǻ�ѧ�仯���������⡣��ѡD��
�����Ѷȣ�һ��
4��ѡ���� �������ͬ��̼������Һ�����ᡣ�ٽ�̼������Һ��μ������������������μ���̼������Һ�в������������ʵ���֮��Ϊ2 :1����ԭ̼������Һ�����������ʵ����ʵ���֮��Ϊ
A.2��1
B.1��1����
C.3��4 ������
D.1��2
�ο��𰸣�C
�������������٢ڲ�������������ʵ����ֱ�Ϊ2mol��1mol �������ֲ�����������ܾ����������ɵ�CO2����ͬ����������Ϊ��������
�ٽ�̼������Һ��μ������ᣬ�ɷ�ӦNa2CO3+2HCl=2NaCl+H2O+CO2��֪����n��HCl��=4mol��
��������μ���̼�����з�Ӧ�ֲ����У�������ȫ��Ӧ��NaHCO3��ʣ�ࣩ���ɷ���ʽNaHCO3 + HCl =" NaCl" + H2O + CO2����Na2CO3 + HCl = NaHCO3��n��CO2��=1mol�����n��Na2CO3��=3mol���ʴ˷�Ӧ��ԭ̼������Һ�����������ʵ����ʵ���֮��Ϊ3��4��
�����Ѷȣ���
5��ѡ���� ��ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�����ѹ������Ͳ�ڣ������±����еIJ�ͬʵ�飨������ͬ��ͬѹ�²ⶨ����
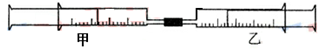
������˵����ȷ����
A.ʵ��1�г������ձ�Ϊ���ɫ
B.ʵ��2�м���Ͳ�ڵ�������������ɫ����һ��������ƶ�
C.ʵ��3�м���Ͳ��������ɫ�����������ѹ��
D.ʵ��4�м���Ͳ�ڳ��а��̲����⣬�������տ�������ѹ������ͷ
�ο��𰸣�C
���������������A����������������Һ��Ӧ�����������������������백ˮ��Ӧ��������������������
B��������Ӧ2HBr+Cl2=Br2+2HCl����ӷ��γ�����������Ͳ�ڵ�������������ɫ�����������ʵ�������
C��������Ӧ2NO+O2=2NO2��ͬʱ����2NO2?N2O4����������ʵ�����С��
D������3Cl2+2NH3=N2+6HCl�����������ٷ���NH3+HCl�TNH4Cl���ʰ�����������3Cl2+8NH3=N2+6NH4Cl���ݴ˼����жϣ�
���A��AgNO3+NH3?H2O�TAgOH��+NH4NO3��AgOHΪ��ɫ��������������AgOH+2NH3?H2O�T[Ag��NH3��2]OH+2H2O��������ʧ����A����
B��������Ӧ2HBr+Cl2=Br2+2HCl������ǡ�÷�Ӧ����ӷ��γ�����������Ͳ��������ɫ�����������ʵ��������������ƶ�����B����
C��������Ӧ2NO+O2=2NO2��ͬʱ����2NO2?N2O4������Ͳ��������ɫ�����������ʵ�����С����������ѹ������A��ȷ��
D�������백�����֮��Ϊ15mL��40mL=3��8��������Ӧ3Cl2+8NH3=N2+6NH4Cl�����ɵ���15mL��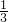 =5mL���а��̲����⣬�������ղ���������ѹ����������D����
=5mL���а��̲����⣬�������ղ���������ѹ����������D����
��ѡC��
���������⿼�鰱������������������������ʣ��Ѷ��еȣ�Cѡ����Ϊ�״��㣬ע����ڵ�ƽ�⣮
�����Ѷȣ���