微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某元素的原子L层上的电子数为K层和M层电子数的2倍,该元素是?(?)
A.Na
B.Mg
C.P
D.S
参考答案:B
本题解析:略
本题难度:简单
2、选择题 右图为短周期的一部分,推断关于Y、Z、M的说法正确的是(?)

A.非金属性:Y>Z>M
B.ZM2分子各原子均满足8e-稳定结构
C.原子半径:M>Z>Y
D.Y离子的结构示意图可表示为: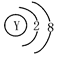
参考答案:D
本题解析:因XYZM为短周期元素,且给出其在元素周期表中的位置,因此可知,XYZM所代表的的元素分别为He、F、S、Cl。
选项A、非金属性强弱:Y>M>Z,故错误。
选项B、ZM2分子的化学式为SCl2,两原子并不满足8e-稳定结构,故错误。
选项C、原子半径大小关系:Z>M>Y>X,故错误。
选项D、Y离子的化学符号为F-,其离子结构示意图为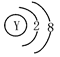 ,故正确。综上,答案选D。
,故正确。综上,答案选D。
点评:本题考查元素周期表的结构,属于基础题。对于元素周期表的考查,应当将元素周期表额结构以及原子的结构结合,明确“位-构-性”三者的关系。
本题难度:简单
3、填空题 (18分) A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B元素原子L层上的电子数为K层电子数的2倍;元素D的2价阴离子的核外电子排布与氖原子相同;E与A同主族;A和E 这两种元素与D都能形成X2Y、X2Y2型化合物。请回答:
(1)写出元素的符号:A?;C_______
(2)画出D的离子结构示意图_____________,B在周期表的位置为?。
(3)B的X2Y2型化合物结构式是_______,E的X2Y型化合物电子式为?。
(4)B与D形成最高价化合物的电子式?。
(5)C的氢化物和C的最高价氧化物的水化物反应生成M,M的化学式为?,M中的化学键类型有__________________。
参考答案:(18分)
(1)H;N(各2分)
(2)S2―结构示意图略,(2分)第二周期第ⅣA族;(2分)
(3)H―O―H,(2分)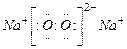 (2分)
(2分)
(4)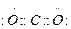 ,(2分)
,(2分)
(5)NH4NO3,(2分)离子键和共价键 (2分)
(2分)
本题解析:略
本题难度:简单
4、填空题 (1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是?。
(2)已知某粒子的结构示意图为: ,试回答:
,试回答:
①当x-y=10时,该粒子为?(填“原子”“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称)???、?、?、?、?。
参考答案:(1)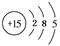
(2)①原子 ②氩原子;氯离子;硫离子;钾离子;钙离子 ③Al(OH)3+3H+=Al3++3H2O
③写出y=3与y=7的元素最高价氧化物对应水化物之间发生反应的离子方程式?。
本题解析:(1)设该元素原子的核电荷数=质子数=a,电子层数为x,最外层电子数为y,依题意:a=5x,a=3y,则5x=3y。因原子的最外层电子数不超过8,即y为1~8的正整数,故仅当y=5,x=3时合理,该元素的核电荷数为15。(2)①当x-y=10时,x=10+y,说明核电荷数等于核外电子数,所以该粒子应为原子;②当y=8时,应为有18个电子的粒子,所以可能为氩原子、氯离子、硫离子、钾离子、钙离子;③y=3时为铝原子、y=7时为氯原子,其最高价氧化物对应的水化物分别为氢氧化铝和高氯酸,反应的离子方程式为Al(OH)3+3H+=Al3++3H2O。
本题难度:一般
5、简答题 四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍; D是形成化合物种类最多的元素。
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为________;写出由甲制高聚物的反应方程式?。
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于________(“极性分子”或“非极性分子”);其电子式________;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式?。
(3)写出B的基态原子电子排布图为 ?。与PH3相比,BA3易液化的主要原因是___________________________________;
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与DC2分子具有相似的结构。故B2C的空间构型是________,其为________(填“极性”或“非极性”)分子 。
参考答案:(1)? 5: 1? n CH2=CH2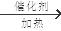
 ?(2)极性分子;
?(2)极性分子;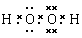 ;2 Fe2+ +2H2O2+2H+=2Fe3++2H2O?(3)
;2 Fe2+ +2H2O2+2H+=2Fe3++2H2O?(3)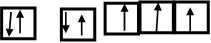 ;NH3中有氢键。(4)?直线型?,非极性分子
;NH3中有氢键。(4)?直线型?,非极性分子
本题解析:根据题意可知:A的H;B是N;C是O;D是 C。(1)H、C形成的某种化合物甲C2H4是一种重要的化工产品,可用作水果和蔬菜的催熟剂,在C2H4分子中σ键是5个和π键数目是1个,所以个数之比为5:1 。由乙烯制高聚物聚乙烯的反应方程式为n CH2=CH2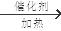
 。(2)A、C形成的某种化合物乙分子中含非极性共价键,则乙分子是H2O2,由于各个化学键的空间排列不对称,所以属于极性分子,其电子式是
。(2)A、C形成的某种化合物乙分子中含非极性共价键,则乙分子是H2O2,由于各个化学键的空间排列不对称,所以属于极性分子,其电子式是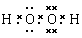 。将H2O2加入浅绿色酸性FeCl2溶液中,溶液变为棕黄色,该反应的离子方程式是2 Fe2+ +2H2O2+2H+=2Fe3++2H2O。(3)B原子的基态原子电子排布图为
。将H2O2加入浅绿色酸性FeCl2溶液中,溶液变为棕黄色,该反应的离子方程式是2 Fe2+ +2H2O2+2H+=2Fe3++2H2O。(3)B原子的基态原子电子排布图为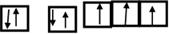 。与PH3相比,NH3易液化的主要原因是因为在分子之间存在氢键,增加了分子之间的相互作用力。(4)笑气(N2O)是一种麻醉剂,有关理论认为N2O 与CO2分子具有相似的结构。因为CO2分子是直线型分子,故B2C的空间构型是直线型。由于各个化学键的空间排列的对称的所以该分子为非极性分子。
。与PH3相比,NH3易液化的主要原因是因为在分子之间存在氢键,增加了分子之间的相互作用力。(4)笑气(N2O)是一种麻醉剂,有关理论认为N2O 与CO2分子具有相似的结构。因为CO2分子是直线型分子,故B2C的空间构型是直线型。由于各个化学键的空间排列的对称的所以该分子为非极性分子。
本题难度:一般