微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-具有相同的电子层结构,下列叙述一定不正确的是
A.离子半径A2->C->B2+
B.它们的原子半径C>B>A
C.它们的原子序数A>B>C
D.原子最外层上的电子数C>A>B
参考答案:B
本题解析:A、C的最低价离子分别为A2-、C-,这说明A是第ⅥA族元素,C是第ⅦA族元素。B2+与C-具有相同的电子层结构,且A、B同周期,这说明B是金属,是第ⅡA族元素,位于A的左侧,且A、B均位于C的下一周期。所以选项ACD都是正确的。同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,所以原子半径是B>A>C,选项B不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力
本题难度:简单
2、选择题 下列各组物质性质的比较不正确的是
A.熔点由高到低SiO2>CsCl>CBr4>CF4
B.热稳定性:HF>H2S>H2O
C.离子半径:O2->Na+>Mg2+
D.酸性:HClO4>H2SO4>H3PO4
参考答案:B
本题解析:略
本题难度:简单
3、填空题 (12分)[选做题]本题包括A、B两小题,分别对应于 “物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.铁是地壳中含量较丰富的元素,仅次于氧、硅、铝元素,其单质及合金是在生产生活中应用广泛的金属材料。化学上常用KSCN溶液等来检验溶液中是否存在Fe3+。
(1)Fe3+离子基态的电子排布式可表示为?。
(2)一种铁晶体的晶胞属于体心立方堆积,则该晶胞中所包括的铁原子的个数是?。
(3)C、N两种元素的简单气态氢化物的热稳定性由强到弱的顺序为?。
(填化学式)
(4)C、N、O三种元素的第一电离能由大到小的顺序为?。(填元素符号)
(5)离子化合物Fe2O3的熔点高于KC1的熔点的原因是?。
(6)据报道:由Q、X、Z三种元素形成的一种晶体具有超导性,其晶体结构如右图所示。晶体中距每个X原子周围距离最近的Q的原子的个数是?。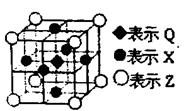
参考答案:A.(1)1s22s22p63s23p63d5(2)2
(3)NH3>CH4(4)N>O>C
(5)Fe2O3的晶格能大于KCl的晶格能(6)2
本题解析:(1)根据构造原理可知,Fe3+离子基态的电子排布式可表示为1s22s22p63s23p63d5。
(2)在体心立方堆积中,含有的铁原子个数是8×1/8+1=2。
(3)非金属性越强,相应氢化物的稳定性越强,N的非金属性强于C的,所以稳定性是NH3>CH4。
(4)非金属性越强,第一电离能越大。但由于氮元素的2p轨道电子处于半充满状态,所以第一电离能大于氧元素的,即N>O>C。
(5)由于Fe2O3的晶格能大于KCl的晶格能,所以离子化合物Fe2O3的熔点高于KC1的熔点。
(6)Q位于体心处,X位于面心处,所以晶体中距每个X原子周围距离最近的Q的原子的个数是2个。
本题难度:一般
4、选择题 设某元素原子核内的质子数为m,中子数为n,则下述论断正确的是
A.不能由此确定该元素的相对原子质量
B.这种元素的相对原子质量为m+n
C.若碳原子质量为wg,此原子的质量为(m+n)wg
D.核内中子的总质量小于质子的总质量
参考答案:A
本题解析:元素的相对原子质量是按其各种天然同位素原子所占的一定百分比计算山来的平均值,因此,只知道某元素一种同位素的质子数和中子数只能算出这种同位素的质量数,而不能确定该元素的相对原子质量,A对。B错。若碳原子质量为wg,碳的相对原子质量近似为12,则此原子的质量为(m+n)w/12(g),而不是(m+n)wg,C错。原子核内质子数和中子数之间没有必然关系,而且质子的总质量和中子的总质量之间也无必然关系,质子的总质量大于、等于、小于中子的总质量都可能,D错。
本题难度:一般
5、选择题 人类探索月球发现,在月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一。氦的该种同位素应表示为……( )
A.34He
B.23He
C.24He
D.33He
参考答案:B
本题解析:原子的表示方法为ZAX,其中A为质量数,Z为质子数(核电荷数、原子序数)。
本题难度:一般