微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法中正确的是?
[? ]
A.氯气通入澄清石灰水中,制取漂粉精?
B.可用化合反应的方法制取Fe(OH)3
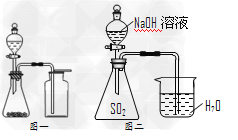
C.选择合适的试剂,用图一所示装置可分别?制取少量CO2、NO和O2
D.图二装置证明SO2与NaOH发生了反应(系统装置不漏气)
参考答案:B
本题解析:
本题难度:一般
2、实验题 高纯MnCO3是制备高性能磁性材料的主要原料。研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制得硫酸锰晶体,再以MnSO4为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中加入一定MnO2和水,搅拌,通入SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2?+?H2SO3=?MnSO4?+?H2O)
①MnO2和水,搅拌,通入SO2的化学方程式为_________________________
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可用_____________
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是_______________________

(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解Mn(OH)2开始沉淀时pH=7.7.请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
①__________________
?②过滤,用少量水洗涤2~3次;
③是否被洗涤除去?检验SO42-
④________________?
⑤低于100℃干燥
(3)向物质的量浓度均为0.01?mol・L-1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的是___________(填离子符号);当两种沉淀共存时,溶液中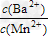 =__________。(已知Ksp(BaCO3)=8.1×10-9,Ksp(MnCO3)=1.8×10-11)
=__________。(已知Ksp(BaCO3)=8.1×10-9,Ksp(MnCO3)=1.8×10-11)
参考答案:(1)①SO2+MnO2=MnSO4;②控制适当的温度、缓慢通入混合气体;③Mn2+催化与O2 与H2SO3反应生成H2SO4
(2)①边搅拌边加入NaHCO3(或Na2CO3),并控制溶液pH < 7.7;④用少量C2H5OH洗涤?(凡合理答案均可)
(3)Mn2+ ;450
本题解析:
本题难度:一般
3、实验题 硫酸亚铁容易被氧化,而硫酸亚铁铵晶体[(NH4)2SO4・FeSO4・6H2O]较稳定,常用于代替硫酸亚铁作还原剂。现以铁屑为主要原料制备硫酸亚铁铵晶体的反应如下:Fe +H2SO4(稀)=FeSO4+H2↑、FeSO4+(NH4)2SO4+6H2O=(NH4)2SO4・FeSO4・6H2O。
步骤1:在盛有适量铁屑的锥形瓶中加入某种试剂除去油污,加热,充分反应后过滤、洗涤、干燥、称量,铁屑质量为m1;
步骤2:将处理过的铁屑加入到一定量的稀硫酸中,加热至50~80℃充分反应,趁热过滤并用少量热水洗涤,滤液及洗涤液都转移至蒸发皿中。滤渣干燥后称重,剩余铁屑质量为m2;
步骤3:准确称取所需质量的硫酸铵晶体加入“步骤2”的蒸发皿中,搅拌使之溶解,缓缓加热一段时间,将其冷却、结晶、过滤。用无水乙醇洗涤晶体并自然干燥,称量所得晶体质量为m3。
回答下列问题:
(1)能够用于除去铁屑表面油污的试剂是_________(填字母)。
A.纯碱溶液 B.烧碱溶液 C.明矾溶液 D.稀硫酸
(2)实验中三次用到过滤操作,完成该操作的玻璃仪器有________________;步骤2中趁热过滤的目的是_____________________。
(3)硫酸亚铁在潮湿的空气中易被氧化生成一种物质(碱式硫酸铁),该反应的化学方程式为________________________。
(4)铁屑表面常有少量的铁锈(Fe2O3・nH2O),对FeSO4的制备_______(填“有”或“无”)影响,理由是
_________________________ (用离子方程式回答)。
(5)若忽略铁锈的影响,上述实验中硫酸亚铁铵晶体的产率为____________。
(6)请设计一个简单的实验,检验硫酸亚铁铵晶体中含有结晶水___________________________ (简述实验操作、现象和结论)。
参考答案:(1)AB
(2)玻璃棒、烧杯、漏斗;避免FeSO4因结晶而造成损失
(3)4FeSO4+O2+2H2O=4Fe(OH)SO4
(4)无;Fe2O3+6H+=2Fe3++3H2O、2Fe3++Fe=3Fe2+
(5)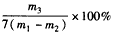
(6)取少量硫酸亚铁铵晶体于试管中,用酒精灯加热,在试管口有液体(水珠)生成,说明其中含有结晶水
本题解析:
本题难度:一般
4、实验题 某化工厂排放的污水中含有Al3+、Hg2+、 Fe3+、Cu2+四种离子,甲、乙、丙三位同学设计从污水中回收铜的方案如下:
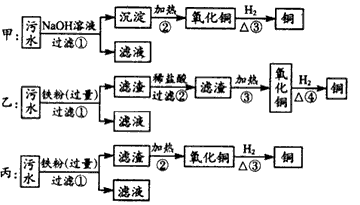
(1)以上实验方案能否得到铜:甲____, 乙____,丙____。(填“能”或“不能”)
(2)在制得铜的方案中会导致环境污染的一步操作是___,其原因是___。
(3)在可制得铜的方案中,主要的离子方程式是______。
参考答案:(1)不能 ;能 ;不能
(2)③ ;加热乙中操作②后的滤渣,此时汞蒸气将挥发进入空气中
(3) Fe+2Fe3+=3Fe2+,Fe+Hg2+=Fe2++ Hg, Fe+ Cu2+= Fe2++ Cu,Fe +2H+=Fe2++ H2↑
本题解析:
本题难度:一般
5、填空题 已知氢氧化铁胶体是氢氧化铁胶粒吸附多余Fe3+生成的。现将氢氧化铁固体粉碎使粒子直径在10-9~10-7m,并悬浮于水中,再向悬浊液中加入______或______,即可制得Fe(OH)3胶体。(填两类不同物质)
参考答案:含三价铁的盐;适量的强酸
本题解析:
本题难度:一般