微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子组在指定条件下一定能大量共存的是( )
A.可使甲基橙溶液呈黄色的溶液中:I-、Cl-、NO3-、Na+
B.pH=12的溶液中:CO32-、Cl-、F-、K+
C.含大量Al3+的溶液中:K+、Na+、NO3-、ClO-
D.与铝反应产生大量氢气的溶液:Na+、K+、HCO3-、NO3-
参考答案:A.使甲基橙溶液呈黄色的溶液,显酸性,酸性溶液中I-、NO3-发生氧化还原反应,则不能共存,故A错误;
B.pH=12的溶液,显碱性,该组离子在碱性溶液中不反应,则能够共存,故B正确;
C.Al3+与ClO-相互促进水解,则不能共存,故C错误;
D.与铝反应产生大量氢气的溶液,为酸或强碱溶液,HCO3-既能与酸反应又能与碱反应,则一定不能共存,故D错误;
故选B.
本题解析:
本题难度:简单
2、选择题 在下列溶液中,一定能够大量共存的离子组是( )
A.pH=1的溶液中:Na+、Ca2+、Mg2+、NO3-
B.滴加石蕊试液显红色的溶液中:Fe3+、NH4+、I-、SCN-
C.常温下,水电离出c(H+)=1×10-14mol/L的溶液中:CO32-、SO42-、Na+、K+
D.与铝反应放出氢气的溶液中:Fe2+、SO42-、NO3--、Na+
参考答案:A.pH=1的溶液呈酸性,酸性溶液中,四种离子之间不发生任何反应,可大量共存,故A正确;
B.滴加石蕊试液显红色的溶液呈酸性,Fe3+可与I-发生氧化还原反应,Fe3+与SCN-发生络合反应而不能大量共存,故B错误;
C.常温下,水电离出c(H+)=1×10-14mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性溶液中CO32-不能大量存在,故C错误;
D.与铝反应放出氢气的溶液可能呈酸性,也可能呈碱性,酸性条件下Fe2+与NO3--发生氧化还原反应,在碱性条件下Fe2+不能共存,故D错误.
故选A.
本题解析:
本题难度:简单
3、选择题 下列叙述正确的是
[? ]
A.可以根据PbI2和AgCl的Ksp的大小比较两者的溶解能力
B.常温下,同浓度的Na2S与NaHS溶液相比,NaHS溶液的pH大
C.等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大
D.能使碘化钾淀粉试纸变蓝的溶液中,Na+、S2-、Br-、NH4+等离子可以大量存在
参考答案:C
本题解析:
本题难度:一般
4、填空题 (8分)无色透明溶液中可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-,取该溶液进行如下实验:①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取原溶液少许,加铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色;
③取原溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取原溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。请回答下列问题:
(1)根据上述实验判断原溶液中上述离子肯定存在的是 ,
肯定不存在的是 。
(2)写出与②③两个实验有关的离子方程式:
② ,
③ 。
参考答案:(1)Al3+、NO3-、SO42-;Fe3+、Ba2+、HCO3-;
(2)②3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
③Al3++3NH3?H2O=Al(OH)3↓+3NH4+
本题解析:由题意知:溶液无色透明,则Fe3+肯定不存在;
①用蓝色石蕊试纸检测该溶液,试纸显红色,可知溶液显酸性,HCO3-肯定不存在;②取原溶液少许,加铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色,反应方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,2NO+O2=2NO2,则原溶液中一定存在NO3-;
③取原溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失,Al3++3NH3?H2O=Al(OH)3↓+3NH4+ 说明原溶液中有Al3+存在;
④取原溶液少许,滴入氯化钡溶液产生白色沉淀,可知原溶液中有SO42-存在,则Ba2+肯定不存在;
⑤由于④加入了氯化钡,所以不能证明原溶液有没有Cl-;
综上所述:肯定存在的离子是Al3+、NO3-、SO42-
肯定不存在的离子是Fe3+、Ba2+、HCO3-。
考点:认识离子共存,掌握常见离子的性质及检验方法。
点评:本题考查了常见离子的化学性质及检验办法,要求学生熟练掌握K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-的化学性质及反应现象,特别是NO3-在酸性溶液中的强氧化性。
本题难度:一般
5、填空题 以食盐为原料进行生产并综合利用的某些过程如下图所示:
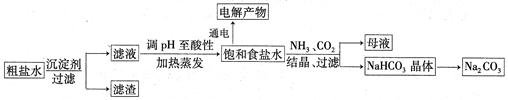
(1)为除去粗盐中的Ca2+、Mg2+和SO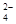 ,得到纯净的NaCl晶体,需加入以下试剂:
,得到纯净的NaCl晶体,需加入以下试剂:
A.过量的NaOH溶液;
B.过量的Na2CO3溶液;
C.适量的盐酸;
D.过量的BaCl2溶液。
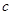 (OH-)的比值是_________。
(OH-)的比值是_________。