微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1?g?H2完全燃烧生成液态水,放出142.9?kJ热量。则H2燃烧的热化学方程式为__________________________________。
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景。现氢氧燃料电池进行下图所示实验:①氢氧燃料电池中,正极的电极反应式为____________
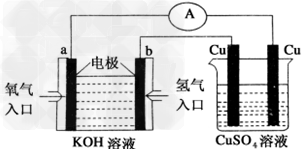
②上图装置中,某一铜电极的质量减轻3.2?g,则a极上消耗的O2在标准状况下的体积为____________L
(3)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g) 2NH3(g);ΔH=-92.4?kJ/mol
2NH3(g);ΔH=-92.4?kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。
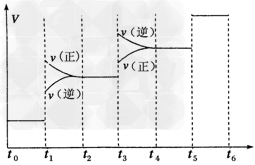
图中t1时引起平衡移动的条件可能是____________其中表示平衡混合物中NH3的含量最高的一段时间是____________
②温度为T?℃时,将2?a?mol?H2和a?mol?N2放入0.5?L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为____________。
参考答案:(1)2H2(g)+O2(g)=2H2O(l)ΔH=-571.6?kJ/mol
(2)①O2+4e-+2H2O=4OH-;②0.56
(3)①增大压强;t2-t3;②4/a2
本题解析:
本题难度:一般
2、选择题 在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,在仅改变某一条件后,达到乙平衡,对此条件的分析正确的是( )

A.图Ⅰ是增大反应物浓度
B.图Ⅱ可能是加入正催化剂
C.图Ⅱ可能是增大压强
D.图Ⅲ是增大压强或升高温度
参考答案:A、增大反应物浓度,正逆反应速率均加快,且正反应速率大于逆反应速率,但是逆反应速率不会摆脱原来的速率变化,故A错误;
B、加入正催化剂,正逆反应速率同等程度的增大,化学平衡不移动,故B正确;
C、反应X2(g)+Y2(g)?2XY(g)为反应前后体积不变的反应,若增大压强,正逆反应速率同等程度的增大,但化学平衡不移动,故C正确;
D、增大压强正逆反应速率同等程度的增大,但化学平衡不移动,由图象可知乙的温度大于甲的温度,升高温度化学平衡逆向移动,XY的含量减小,纵坐标是XY的含量时,才会吻合图象,故D错误.
故选:BC.
本题解析:
本题难度:简单
3、填空题 在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染。
(1)N2(g)+?O2(g)=2NO(g)?△H=+180.5?kJ/mol?
2C(s)+?O2(g)=2CO(g)?△H=-221.0?kJ/mol?
C(s)+?O2(g)=CO2(g)?△H=-393.5?kJ/mol?
写出NO(g)与CO(g)反应的热化学方程式____________________。
(2)某研究性学习小组在技术人员的指导下,在某温度时按下列流程探究催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如表

①前2s内的平均反应速率v?(N2)?=__________。
②列式计算该温度下反应的平衡常数K_______________。
③对于该可逆反应,下列叙述正确的是___________(填序号)。
A.该反应在一定条件下能自发进行
B.该反应能有效减少有害气体的排放
C.该反应一旦发生将在很短的时间内完成?
D.该反应达到平衡时CO、NO的转化率相等
(3)CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列叙述错误的是____(填序号)。

A.负极的电极反应式为:CO+O2--2e-=CO2?
B.工作时O2-在固体介质中由电极a流向电极b
C.工作时电子由电极a通过电流计流向电极b
D.电流计中显示的电流越大,汽车尾气中CO的含量越高
参考答案:(1)2NO(g)+2CO(g)=N2(g)+2CO2(g)? △H=-746.5 kJ/mol
(2)①1.875×10-4 mol・L-1・s-1;②5.00 ×103;③ABC
(3)B
本题解析:
本题难度:一般
4、填空题 (14分)某化学反应2A(g) B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol/L)随反应时间(min)的变化情况,根据下述数据,完成下列填空:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol/L)随反应时间(min)的变化情况,根据下述数据,完成下列填空:
实验
序号
| 温度/℃
| 时间/min
|
0
| 10
| 20
| 30
| 40
| 50
| 60
|
1
| 800℃
| 1.0
| 0.80
| 0.67
| 0.57
| 0.50
| 0.50
| 0.50
|
2
| 800℃
| c2
| 0.60
| 0.50
| 0.50
| 0.50
| 0.50
| 0.50
|
3
| 800℃
| c 3
| 0.92
| 0.75
| 0.63
| 0.60
| 0.60
| 0.60
|
4
| 820℃
| 1.0
| 0.40
| 0.25
| 0.20
| 0.20
| 0.20
| 0.20
|
?
(1)在实验l过程中,10 min~20 min时间内用B表示该反应的平均化学反应速率为?mol/(L・min)。
(2)在实验2过程中,A的初始浓度c2=?mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是?。
(3)设实验3的化学反应速率为v3,实验1的化学反应速率为v1,则v3?v1,且c3?1.0 mol/L (填“<”、“>”或“=”)。
(4)比较实验4和实验l,可推测该反应是?反应(填“吸热”或“放热”)。理由是?
?。
参考答案:(1) 0.0065? (2)1.0;?催化剂? (3)? >;>
(4) 吸热;温度升高时,平衡向右移动,说明正反应为吸热反应
本题解析:⑴化学化学反应速率为单位时间内浓度的变化量:
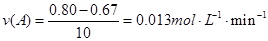
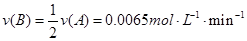
⑵因为达到平衡时实验2的平衡浓度跟实验1相等,所以起始浓度也是相等的,即1.0为
⑶单位时间内反应物浓度的变化量可以看出:v3>v1,引起反应速率大的原因只能是起始浓度大,所以有c3>1.0 mol/L
⑷实验4和实验l比较是温度的不同,升高温度,平衡是向着吸热的方向移动,因此,正向是吸热的方向。
本题难度:一般
5、填空题 下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
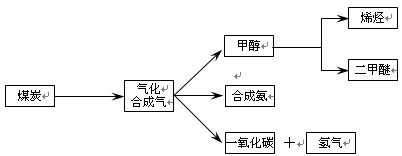
(1)已知该产业链中某反应的平衡表达式为:K=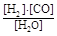
它所对应反应的化学方程式为?。
已知在一定温度下,在同一平衡体系中各反应的平衡常数如下:
C(s)+CO2(g) 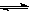 ?2CO(g),K1
?2CO(g),K1
CO(g)+H2O(g) 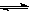 ?H2(g)+CO2(g),K2
?H2(g)+CO2(g),K2
C(s)+H2O(g) 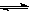 ?CO(g)+H2(g),K3
?CO(g)+H2(g),K3
则K1、K2、K3之间的关系为?。
(2)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)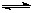 H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
该反应的逆反应方向是?反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时CO的转化率为?。
(3)对于反应N2O4(g)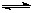 2NO2(g);△H=Q(Q>0),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ? 。
2NO2(g);△H=Q(Q>0),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ? 。

A.两种不同的温度比较:T1 > T?2
B.A、C两点的反应速率:A<C
C.B、C两点的气体的平均相对分子质量:B<C ?
D.由状态B到状态A,可以用加热的方法实现
(4)如右图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率,反应原理为:NO(g) + NO2(g) + 2NH3(g)  ?2N2(g) + 3H2O(g)
?2N2(g) + 3H2O(g)

 以下说法正确的是(注:脱氮率即氮氧化物转化率)
以下说法正确的是(注:脱氮率即氮氧化物转化率)
A.上述反应的正反应为吸热反应
B.相同条件下,改变压强对脱氮率没有影响
C.曲线①、②最高点表示此时平衡转化率最高
D.催化剂①、②分别适合于250℃和450℃左右脱氮
参考答案:(1)(2分)C(s)+H2O(g) CO(g)+H2(g)? K3=K1?K2
CO(g)+H2(g)? K3=K1?K2
(2)(2分)吸热,75% (各1分)
(3)(2分)B、D (一个1分,错一个扣2分)
(4)(2分)D
本题解析:(1)平衡常数的定义为:可逆反应达到平衡后,生成物浓度幂之积与反应物浓度幂之积的比值。所以,由平衡常数表达式K=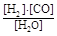 可知:对应的方程式为:C(s)+H2O(g)
可知:对应的方程式为:C(s)+H2O(g) CO(g)+H2(g);
CO(g)+H2(g);
由方程式C(s)+CO2(g) 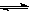 ?2CO(g),K1①;CO(g)+H2O(g)
?2CO(g),K1①;CO(g)+H2O(g) 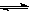 ?H2(g)+CO2(g),K2②;?
?H2(g)+CO2(g),K2②;?
C(s)+H2O(g) 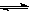 ?CO(g)+H2(g),K3 ③;得将①+②=③,即可知K1、K2、K3之间的关系为K3=K1?K2;
?CO(g)+H2(g),K3 ③;得将①+②=③,即可知K1、K2、K3之间的关系为K3=K1?K2;
(2)由表中平衡常数与温度的关系:温度越高K越小,即可知逆反应方向的反应为吸热反应;
由方程式:CO(g)? +? H2O(g)?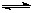 ?H2(g)? +? CO2(g),
?H2(g)? +? CO2(g),
起始浓度:0.020mol/L? 0.020mol/L? 0? 0
变化浓度:? x? x? x? x
平衡浓度:0.020-x? 0.020-x? x? x
500℃时平衡常数K=9=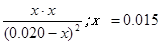 ;平衡时CO的转化率
;平衡时CO的转化率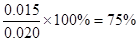
 ;
;
(3)由方程式N2O4(g)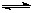 2NO2(g);△H=Q(Q>0),温度越高,NO2(g)的含量越高,即T2 > T?1,A错;相同温度下,压强越大,体积越小,气体的浓度越高,反应速率越快,所以A、C两点的反应速率:A<C,B正确;B、C两点NO2(g)的体积分数相同,即B、C两点的气体的平均相对分子质量:B=C,C错;B→A的过程中NO2(g)的的体积分数增大,可用加热的方法实现,D正确;
2NO2(g);△H=Q(Q>0),温度越高,NO2(g)的含量越高,即T2 > T?1,A错;相同温度下,压强越大,体积越小,气体的浓度越高,反应速率越快,所以A、C两点的反应速率:A<C,B正确;B、C两点NO2(g)的体积分数相同,即B、C两点的气体的平均相对分子质量:B=C,C错;B→A的过程中NO2(g)的的体积分数增大,可用加热的方法实现,D正确;
(4)由于反应为:NO(g) + NO2(g) + 2NH3(g)  ?2N2(g) + 3H2O(g),由图像可知,相同条件下,开始时随温度的升高脱氮率逐渐增大,后随温度的升高脱氮率逐渐减小;最高点表示达到平衡状态,平衡后再升高温度脱氮率反而是减小的,所以,该反应的正反应方向为放热反应,A错;该反应为非等体积反应,压强的改变必须会影响脱氮率,所以B错;曲线①、②最高点表示反应达到平衡状态,C错;由图形分析可知催化剂①、②分别适合于250℃和450℃左右脱氮,D正确;
?2N2(g) + 3H2O(g),由图像可知,相同条件下,开始时随温度的升高脱氮率逐渐增大,后随温度的升高脱氮率逐渐减小;最高点表示达到平衡状态,平衡后再升高温度脱氮率反而是减小的,所以,该反应的正反应方向为放热反应,A错;该反应为非等体积反应,压强的改变必须会影响脱氮率,所以B错;曲线①、②最高点表示反应达到平衡状态,C错;由图形分析可知催化剂①、②分别适合于250℃和450℃左右脱氮,D正确;
本题难度:简单