微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 两种有机物以一定比例混合,一定条件下在aLO2(足量)中充分燃烧恢复到原状态,再通过足量的过氧化钠,得到气体仍是 aL,下列组合中符合此条件的是:
A.CH4、C2H4
B.CH3CH2OH 、CH3COOH
C.C2H6、HCHO
D.HCHO、HCOOCH3
参考答案:D
本题解析:气体体积不变,所以相当于氧气没有参与反应,因此根据Na2O2→2NaOH、Na2O2→Na2CO3可知,有机物的组成应该是(CO)n(H2)m,所以选项D正确,答案选D。
本题难度:简单
2、选择题 某物质在灼烧时火焰呈紫色,说明该物质中一定含有(? )
A.钾原子
B.钾离子
C.钾元素
D.钾的化合物
参考答案:C
本题解析:某些金属或它们的化合物在灼烧时呈特殊颜色为焰色反应。焰色反应是元素的一种性质,它可以是金属原子,也可以是金属离子。焰色反应可以检验某些金属或它们的化合物,但不能确定其存在的形式或粒子的种类。
本题难度:简单
3、填空题 (10分)如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要的固氮反应。
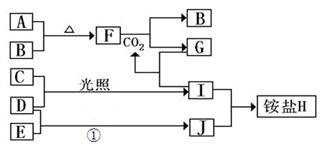
(1)单质E的结构式_____________
(2)F和H2O反应的化学方程式为_____________________________,该反应中被氧化与被还原的物质的物质的量之比是_________________
(3)铵盐H中阳离子的电子式_______________,检验H 中阳离子的方法是____________________
_____________________________________________________________________________
参考答案:(1)N≡N
(2)2Na2O2+2H2O=4NaOH+O2↑ ;? 1:1
(3)? ;取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有NH4+
;取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有NH4+
本题解析:化合物G的焰色反应为黄色,含有Na元素,F能与二氧化碳反应得到气体单质B与G,可推知F为Na2O2,B为O2,G为Na2CO3,而A与B(氧气)反应得到F(过氧化钠),则A为Na.G(Na2CO3)与I反应得到CO2,则I属于酸,I由气体非金属单质C与D在光照条件下得到,则I为HCl,C、D分别为H2、Cl2中的一种,I和J通常状况下呈气态,二者反应得到铵盐,且反应①是化工生产中的一种重要固氮反应,可推知J为NH3,D为H2,E为N2,铵盐H为NH4Cl,故C为Cl2;
(1)单质E为N2,分子中N原子之间形成3对共用电子对,其结构式为N≡N;
(2)F为过氧化钠,与H2O反应生成氢氧化钠与氧气,化学方程式为2Na2O2+2H2O=4NaOH+O2↑,该反应中被氧化与被还原的物质都是过氧化钠,由电子转移守恒可知,被氧化与被还原过氧化钠的物质的量之比是1:1;
(3)铵盐H为NH4Cl,NH4+离子的电子式为 ,检验NH4+离子的方法是:取少量H?样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子。
,检验NH4+离子的方法是:取少量H?样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子。
本题难度:一般
4、选择题 纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。下列说法不正确的是? ( )。
A.“联合制碱法”和“氨碱法”的化学反应原理中都有下列化学反应
NH3+CO2+NaCl+H2O=Na HCO3↓+NH4Cl
2NaHCO3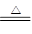 Na2CO3+H2O↑+CO2↑
Na2CO3+H2O↑+CO2↑
B.“联合制碱法”生产中有氨的循环利用工艺
C.“氨碱法”生产中有氨的循环利用工艺
D.“联合制碱法”和“氨碱法”都有一定的局限性
参考答案:B
本题解析:“氨碱法”将NH4Cl和Ca(OH)2再反应,使NH3循环利用;“联合制碱法”是制得纯碱和副产品氯化铵。
本题难度:一般
5、选择题 把足量的稀硫酸分为质量相等的两份,倒入质量相等的甲、乙两个烧杯中,然后向甲杯中投入2.4 g镁,向乙杯中小心地投入2.3 g钠,等反应停止后,称量两杯溶液,结果是
A.甲杯质量稍大
B.乙杯质量稍大
C.两杯质量相等
D.无法确定
参考答案:C
本题解析:根据差量法,加入镁烧杯增加2.2g,加入钠的烧杯也增加2.2g,故最后两烧杯质量相等。
本题难度:一般