微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 甲醇、氧气和强碱溶液做电解质的手机电池中的反应为:
2CH3OH+3O2+4OH-?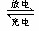 2CO32-+6H2O,有关说法正确的是?
2CO32-+6H2O,有关说法正确的是?
A.放电时,CH3OH参与反应的电极为正极
B.放电时,负极电极反应:CH3OH+8OH--6e- =CO32-+6H2O
C.标况下,通入11.2LO2完全反应有1mol电子转移
D.充电时电解质溶液的pH逐渐减小
参考答案:B
本题解析:A、放电时,CH3OH发生氧化反应,所以CH3OH参与反应的电极为负极,错误;B、放电时,负极为甲醇的氧化反应,结合电解质溶液,反应式为CH3OH+8OH--6e- =CO32-+6H2O,正确;C、标况下,11.2LO2的物质的量为0.5mol,所以11.2LO2完全反应有0.5mol×4=2mol电子转移,错误;D、充电时,反应从右向左进行,氢氧根离子浓度增大,溶液pH逐渐升高,错误,答案选B。
本题难度:一般
2、选择题 2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述错误的是(?)
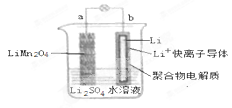
A.a为电池的正极
B.电池充电反应为LiMn2O4=Li1-xMn2Ox+xLi
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
参考答案:C
本题解析:A、由图示可知:活动性b>a,所以b是负极,a是正极。Li失电子为负极,LiMn2O4得电子为正极,所以a为电池的正极,正确;B、充电时,Li+在阴极得电子,Li1-xMn2O4在阳极失电子,电池充电反应为LiMn2O4=Li1-xMn2O4+xLi,因此选项B正确;C、放电时,a为正极,正极上LiMn2O4中Mn元素得电子,所以锂的化合价不变,错误;D、放电时,根据同种电荷相互排斥,异种电荷相互吸引的原则,溶液中阳离子向负电荷较多的正极移动,即溶液中Li+从b向a迁移,因此该选项正确。
本题难度:一般
3、选择题 铜锌原电池(如下图)工作时,下列叙述正确的是 (?)

A.正极反应为:Zn―2e-=Zn2+
B.电池反应为:Zn+Cu2+=Zn2+ +Cu
C.在外电路中,电子从正极流向负极
D.盐桥中的K+移向ZnSO4溶液
参考答案:B
本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,据此可知,该原电池中锌是负极,铜是正极,溶液中的铜离子在正极得到电子,所以选项B是正确的,其余选项都是错误的,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确原电池的工作原理,然后结合题意灵活运用即可。
本题难度:简单
4、填空题 依据氧化还原反应:2Ag+(aq)+ Cu(s)===Cu2+(aq) +2Ag(s)设计的原电池如图所示。

请回答下列问题:
(1)电极X的材料是____;电解质溶液Y是____;
(2)银电极为电池的______极,发生的电极反应为__________________ ;X电极上发生的电极反应为________________,
(3)外电路中的电子是从____电极流向____电极。
参考答案:(1)铜;AgNO3溶液?
(2)正;Ag+ e- ===Ag;Cu -2e- ===Cu2+?
(3)铜;银
本题解析:
本题难度:一般
5、选择题 纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:Zn-2e-+2OH-= Zn(OH)2 Ag2O +H2O + 2e-= 2Ag+2OH-
下列说法正确的是
A.溶液中OH-向正极移动,K+、H+向负极移动
B.锌发生还原反应,氧化银发生氧化反应
C.锌是负极,氧化银是正极
D.在电池放电过程中,负极区溶液碱性增强