��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��8�֣���ͼ��ʾ��ԭ����У��ش���������
��1����������
��2��д���缫��Ӧʽ�������� �������� ��
��3��д���缫��Ӧ�ܷ�Ӧʽ
��4�������� ������ ������дZn��Cu��
�ο��𰸣���1��Zn (2��) ��2��2H++2e-=H2 (1��) Zn-2e-=Zn2+ (1��)
Zn+2H+=Zn2++H2 (2��) ��4��Zn Cu (2��)
�������������ԭ��ص��й��жϺ�Ӧ�á���ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ����ʧȥ�ĵ��Ӿ����ߴ��ݵ������ϡ�п��ͭ���ã�����п�Ǹ�����ʧȥ���ӡ�ͭ����������Һ�е��������������õ����ӣ�������ԭ��Ӧ����������
�����Ѷȣ�һ��
2������� ��ѧ������̫���ֽܷ�ˮ���ɵ������ڴ����������������̼��Ӧ���ɼ״���ˮ����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�ء�
��֪H2��g����CO��g����CH3OH��l������ֵ�ֱ�Ϊ143kJ��g-1��10kJ��g-1��23kJ��g-1��
��ش��������⣺
��1���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽΪ______________��
��2����ֱ���Լ״�Ϊȼ�ϵ���У��������ҺΪ���ԣ������ķ�ӦʽΪ________,?�ܷ�Ӧʽ_____________��
��3����350��ʱ�������¶Ȳ��䣬��1molCO2��3molH2����һ�ܱպ������У���ַ�Ӧ���ɼ״�������ˮ�����ﵽƽ�����CO2ת����Ϊa,�������ڵ�ѹǿ����ʼѹǿ֮��Ϊ______����350��ʱ�������¶Ȳ��䣬��1molCO2��3molH2����һ�ܱպ�ѹ���У���ַ�Ӧ�ﵽƽ�����CO2ת����Ϊb,��a________b���á���������������ʾ��
�ο��𰸣���1��CH3OH(l)+O2(g)=?CO(g)+2H2O(l)?��H?=-456KJ/mol?
��2��CH3OH+8OH-?-6e-=CO32-+6H2O?��?2CH3OH+3O2+4OH-=2CO32- +6H2O?��
��3��(2-a)/2 ��?��
���������
�����Ѷȣ�һ��
3��ѡ���� ���з����У��ܹ�ʹ��ӦCu+2H2O�TCu��OH��2��+H2���������ǣ�������
A��ͭƬ��ԭ��صĸ�����̼����ԭ��ص��������Ȼ������������Һ
B��ͭп�Ͻ��ڳ�ʪ�Ŀ����з����绯ѧ��ʴ
C����ͭƬ���������缫�������������Һ
D����ͭƬ���������缫���������ͭ��Һ
�ο��𰸣�����ͭ��ˮ֮�䷢���ķ�Ӧ�Ƿ��Է���������ԭ��Ӧ��Ӧ��Ƴɵ��أ��ڷ�ӦCu+2H2O�TCu��OH��2��+H2���У�ʧ���ӵ��ǽ���ͭ�����Ա���ѡ�����ͭ���������ϣ�����������������������ϼ��ɣ���������Ӧ����ˮ�е������ӵõ��ӵķ�Ӧ������ѡ�������Ƶ���������ʣ�
A��ԭ���ԭ������ʵ�ָ÷��Է���������ԭ��Ӧ����A����
B��ͭп�Ͻ��ڳ�ʪ�Ŀ����з����绯ѧ��ʴʱ������п����ʴ��ͭ����������B����
C����ͭƬ���������缫�������������Һ������ʵ�ָ÷�Ӧ�ķ�������C��ȷ��
D����ͭΪ�缫�������ͭ��Һ��ԭ��������������������ͭ�����������������D����
��ѡC��
���������
�����Ѷȣ���
4��ѡ���� һ����ѧ��ص��ܷ�Ӧ����ʽΪ��Zn+Cu2+==Zn2++Cu���û�ѧ��ص���ɿ���Ϊ�� ��
| A
| B
| C
| D
|
����
| Cu
| Mg
| Zn
| Fe
|
����
| Zn
| Zn
| Cu
| Zn
|
�������Һ
| H2SO4
| CuSO4
| ZnCl2
| CuCl2
|
�ο��𰸣�D
�������������ԭ��صĹ��ɣ�����ԭ��ص������ǻ����Բ�ͬ�Ľ���������ͷǽ������������������뵽�������Һ�С����ݷ���ʽ��֪��пʧȥ���ӣ�������������ͭ���ӵõ����ӣ���˵������Һ�б��뺬��ͭ���ӣ���ѡD��
�����Ѷȣ�һ��
5��ѡ���� ��ͼΪͭпԭ���ʾ��ͼ������˵����ȷ����
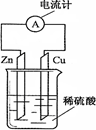
A��������ͭƬͨ����������пƬ
B���ձ�����Һ����ɫ
C��пƬ���ܽ�
D����װ���ܽ�����ת��Ϊ��ѧ��