��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� A��B��C��D��E��F����Ԫ��Ϊԭ��������������Ķ�����Ԫ�ء�AΪԭ�Ӱ뾶��С��Ԫ�أ�A��B���γ�4ԭ��10���ӵķ���X��C���������������ڲ��3���� Dԭ�ӵ����������������ڲ��������һ�룻E�ǵؿ��к������Ľ���Ԫ�أ�FԪ�ص��������������۴�����Ϊ6��
��ش��������⣺
(1)B��C��D��E��F����Ԫ��ԭ�Ӱ뾶�ɴ�С��˳����________��
(2)A��C��ԭ�Ӹ�����1��l�γ�4ԭ�ӷ���Y��Y�Ľṹʽ��________��
(3)����X�ĵ���ʽ��_____________��D������Һ̬X�з�����������A2C�ķ�Ӧ��
д����Ӧ�Ļ�ѧ����ʽ_________________________________ ��
(4)ʵ��֤�������ڵ�EF3�����磬��ԭ����__________________________��
(5)E�ĵ��ʿ�����A��C��D�γɵĻ�����Z��ˮ��Һ�С���������֤ʵ�˷�Ӧ���ɵ���������Ҫ��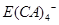 ����ʽ���ڣ�д��E����Z��Һ�����ӷ���ʽ��_________________________________________.
����ʽ���ڣ�д��E����Z��Һ�����ӷ���ʽ��_________________________________________.
(6)��ҵƷZ����Һ�к���ijЩ����������ʣ��������ӽ���Ĥ������ᴿ��������װ�������ӽ���Ĥ��ֻ����������ͨ�������乤��ԭ����ͼ��ʾ��
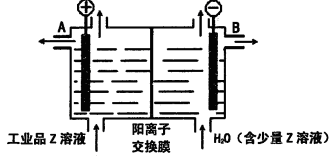
�ٸõ��۵�������Ӧʽ��____________________��
��ͨ�翪ʼ������������ҺpH_________________������������С�����䡱����
�۳�ȥ���ʺ��Z��Һ��Һ�����___________________����д��A����B����������
�ο��𰸣���1��Na Al Cl N O?��1�֣�
��2��H��O��O��H?��1�֣�
��3��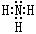 ?��1�֣�
?��1�֣�
2Na��2NH3��2NaNH2��H2��?��2�֣�
��4��AlCl3 �����ڵ�״̬�²��������룬û�в��������ƶ�������?��1�֣�
��5��2Al��2OH����6H2O��2Al(OH)4����3H2��?��2�֣�
��6���� 4OH����4e����2H2O��O2��?��2�֣�
������?��2�֣�
�� B?��2�֣�
���������A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ�����Aԭ�Ӱ뾶��С����AΪ��Ԫ�أ�A��B���γ�4ԭ��10���ӵķ���X����BΪNԪ�أ�C���������������ڲ��3��������?CΪOԪ�أ�Dԭ�ӵ����������������ڲ��������һ�룬��?DΪNaԪ�أ�E�ǵؿ��к������Ľ���Ԫ�أ���?EΪ?A lԪ�أ�FԪ�ص��������������۴�����Ϊ6,��?FΪ?ClԪ��
��ͬ�����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶N��O��Na >Al >Cl ,B��C��D��E��F����Ԫ��ԭ�Ӱ뾶�ɴ�С��˳����Na Al Cl N O���𰸣�Na Al Cl N O��
��A��C��ԭ�Ӹ�����1��l�γ�4ԭ�ӷ���Y��YΪH2O2���ṹʽ��H��O��O��H ���𰸣�H��O��O��H ��
�Ƿ���XΪNH3��NH3�ĵ���ʽ��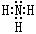 ,Na��Һ����Ӧ�ķ���ʽΪ��2Na��2NH3��2NaNH2��H2��?���𰸣�
,Na��Һ����Ӧ�ķ���ʽΪ��2Na��2NH3��2NaNH2��H2��?���𰸣�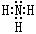 ��2Na��2NH3��2NaNH2��H2�� ��
��2Na��2NH3��2NaNH2��H2�� ��
��AlCl3�ǹ��ۻ�������ۻ�״̬ʱ���ܵ��룬û�в��������ƶ������ӣ��ʲ��ܵ��磬��;AlCl3 �����ڵ�״̬�²��������룬û�в��������ƶ������ӣ�
��E��Al��Al�ĵ��ʿ�����A��C��D�γɵĻ�����Z��NaOH��ˮ��Һ�С�������������[Al(OH)4]�D�����ӷ���ʽΪ?��2Al��2OH����6H2O��2Al(OH)4����3H2�� ���𰸣�2Al��2OH����6H2O��2Al(OH)4����3H2�� ��
�ʢٵ��NaOH��Һ��ʵ�����ǵ��ˮ��������4OH����4e����2H2O��O2������������4H2O��4e��=2H2��4OH�D ,?����pH�����ɢڿ�֪��B�����Ի����Һ�ϸߵ�NaOH��Һ���𰸣��� 4OH����4e����2H2O��O2��������� B
�����Ѷȣ�һ��
2��ѡ���� ���ֶ����ڽ���Ԫ����Ԫ�����ڱ��е����λ����ͼ��ʾ�������ж���ȷ����(? )
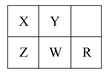
A��ԭ�Ӱ뾶��Z��W��R
B�������ԣ�X��Z
C����������ļ��ԣ�Z��W��R
D��������������X��Y
�ο��𰸣�C
������������⿼��Ԫ��λ����֮��Ĺ�ϵ��ͬһ���ڣ��������ң�ԭ�Ӱ뾶��С���õ���������ǿ����������ǿ������������Ӧ��ˮ������Լ�����A����C��ȷ��ͬһ���壬���ϵ��£�Ԫ�صĽ�������ǿ��B����������������Y��X��D����
�����Ѷȣ�һ��
3������� ��8�֣�X��Y��Z��TΪ�����ڵ�����Ԫ�أ��������������Ϊ+1��+4��+5��+7���˵����Y��Z��X��T����
��1��Ԫ�ط���X?Y?Z?T?��
��2��д��X������������Ӧˮ������Z������������Ӧˮ���ﷴӦ�����ӷ���ʽ?��
��3�������Լ���������ǿ��˳��д����Ԫ������������Ӧˮ����Ļ�ѧʽΪ?
�ο��𰸣���1����ÿ��1�֣�X? Na?Y? C?Z? N?T? Cl?��
��2����2�֣�___ H+_+_OH- ="==" H2O_____��
��3����2�֣�NaOH? H2CO3? HNO3? HClO4��
�����������Ϊ�����������Ϊ+1��+4��+5��+7������Ԫ��������۵�����������������X��Y��Z��T����Ԫ�طֱ��ǵ�һ���ĵ����������Ԫ�أ���Ϻ˵����Y��Z��X��T����������Ԫ�طֱ���X��Na Y��C?Z��N T Cl ��
��2��X��������������������ƣ�Z����������������ᣬ����ǿ���ǿ������ӷ�Ӧ��_ H+_+_OH- ="==" H2O_��
��3�����ռ����������ǿ��˳��һ�£����Ժͷǽ�����˳��һ�£��ó�NaOH? H2CO3? HNO3? HClO4��
�����Ѷȣ�һ��
4��ѡ���� ���±��ṩ��������ҩƷ���ܴﵽʵ��Ŀ�ĵ���
���
| ����
| ҩƷ
| ʵ��Ŀ��
|
A
| �ձ�����Һ©������ͷ�ιܡ�����̨
| ���ᴿ��AlCl3��Һ��NaOH��Һ
| �ᴿ����MgCl2���ʵ�AlCl3��Һ
|
B
| ��Һ©������ƿ����ƿ�����ܼ���Ƥ��
| ���ᡢ����ʯ��
̼������Һ
| ֤���ǽ����ԣ�Cl��C��Si
|
C
| ��ʽ�ζ��ܡ���ͷ�ιܡ�����̨(������)
| ��֪Ũ�ȵ����ᡢ
����NaOH��Һ
| �ⶨNaOH��Һ�����ʵ���Ũ��
|
D
| �ƾ��ơ���������
����������̨(����Ȧ)
| NaCl��Һ
| ������Һ�õ�����
|
?
�ο��𰸣�D
���������A���ᴿ����MgCl2���ʵ�AlCl3��Һ��ʵ������Ϊ�����ᴿ��AlCl3��Һ�ӹ���NaOH��Һ�����ˡ�����Һ��ͨ�����������̼�����ˡ������������������ᣬ���������ҩƷ��ʵ�֣�����B����������֪��Ҫ֤���ǽ����ԣ�Cl��C��Siѡ�õ�ʵ������Ϊ��֤��������������������ǿ�������ҩƷ��ʵ�֣�����C����������к͵ζ����ⶨNaOH��Һ�����ʵ���Ũ�ȣ�ҩƷȱ�����ָʾ��������ȱ�ټ�ʽ�ζ��ܣ���ʵ�֣�����D������NaCl��Һ�õ�����Ļ�������Ϊ����������ʵ�֣���ȷ��
�����Ѷȣ�һ��
5��ѡ���� ���й��ڼ����Ԫ�ص�ԭ�ӽṹ�����ʵ���������ȷ����
A�������ԭ������㶼ֻ��1�����ӣ��ڻ�ѧ��Ӧ������ʧȥ
B����������ʶ���ǿ��ԭ��
C����������ʶ�����������ȼ�����ɹ�������
D����������ʶ�����ˮ��Ӧ����ǿ��
�ο��𰸣�C
�����������������϶��£�����������ǿ������������ȼ�յ��������Dz�ͬ�ģ�����Li����Li2O��������Na2O2��ѡ��C����ȷ������ѡ�����ȷ�ģ���ѡC��
�����������Ǹ߿��еij������㣬�����е��Ѷȵ����⡣������۽̲Ļ�����ּ������ѧ���������Ԫ�������ɽ��ʵ������������������ڵ���ѧ����ѧϰ��Ȥ����ǿѧ����ѧϰ�����ġ�
�����Ѷȣ�һ��