微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 钙元素是人体必需的常量元素,正常人血液中Ca2+的浓度为2.2×10-3~2.7×10-3mol/L。已知2KMnO4+
5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O。现抽取某人血样20mL,稀释后用草酸铵
[(NH4)2C2O4]溶液处理,使Ca2+完全转变为草酸钙(CaC2O4)沉淀;过滤,洗涤,将得到的沉淀用稀硫酸溶解可得到草酸(H2C2O4);溶解得到的草酸与2.0 mL5.0×10-3 mol/L KMnO4溶液恰好完全反应。根据上述信息,求此人血液中Ca2+的浓度,并判断其血液含钙量是否正常?
参考答案:1.25×10-3mol/L,不正常
本题解析:
本题难度:一般
2、填空题 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图I、II所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算
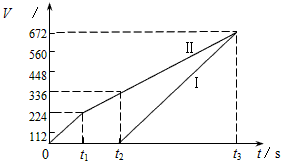
(1)原混合溶液NaCl和CuSO4的物质的量浓度分别为________________ 、_______________ 。
(2)假设溶液体积变化忽略不计,则 t3时刻溶液的pH________________ 。
参考答案:(1)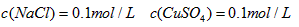
(2)1
本题解析:
本题难度:一般
3、选择题 下列有关氧化还原反应的叙述正确的是
A.金属单质在反应中既可作氧化剂又可作还原剂
B.非金属单质在反应中只可能作氧化剂
C.金属原子失电子越多其还原性越强
D.氧化还原反应,必须有元素化合价的变化,但不一定所有元素的化合价都变化
参考答案:D
本题解析:氧化还原反应是指有化合价变化的反应,但不一定所有元素的化合价都变化.金属元素只有正价无负价,所以参加反应时只能作还原剂,而非金属元素既有负价也有正价,所以,非金属单质在反应中既可能作氧化剂,也可能作还原剂.物质的氧化性、还原性只与得失电子的能力有关,与得失电子数目无关.
本题难度:一般
4、选择题 下列氧化还原反应:6NO+4NH3=5N2+6H2O,氧化产物与还原产物的物质的量之比为:
A.1∶1
B.5∶6
C.3∶2
D.2∶3
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列实验现象描述错误的是
A.氯水、溴水、碘水分别加入淀粉碘化钾溶液都可变蓝
B.钠投入足量的CuSO4溶液中,产生气体,同时生成蓝色沉淀
C.将CCl4加入碘水中,上层呈橙红色
D.Na2O2和盐酸反应,生成的气体能使带火星的木条复燃
参考答案:C
本题解析:
本题难度:困难