微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列方程式中,正确的是
A.氯气与氢氧化钠溶液反应:Cl2+2OH-═Cl-+ClO-+H2O
B.盐酸跟氢氧化铜反应:H++OH-═H2O
C.CH3COOH在水中电离:CH3COOH═H++CH3COO-
D.氢气燃烧的热化学方程式:H2+O2═H2O;△H=-571.6kJ/mol
参考答案:A
本题解析:分析:A.反应生成氯化钠、次氯酸钠和水;
B.氢氧化铜在离子反应中保留化学式;
C.醋酸为弱酸,电离为可逆过程;
D.热方程式中应注明物质的状态.
解答:A.氯气与氢氧化钠溶液反应的离子反应为Cl2+2OH-═Cl-+ClO-+H2O,故A正确;
B.盐酸跟氢氧化铜反应的离子反应为2H++Cu(OH)2═2H2O+Cu2+,故B正确;
C.CH3COOH在水中电离为CH3COOH?H++CH3COO-,故C错误;
D.氢气燃烧的热化学方程式为2H2(l)+O2(g)═2H2O(l);△H=-571.6kJ/mol,故D错误;
故选A.
点评:本题考查化学用语,涉及离子反应的书写、电离方程式的书写及热化学方程式的书写,注意归纳书写方法,明确其差别即可解答,题目难度不大.
本题难度:一般
2、选择题 200℃时,11.6 g CO2和水蒸气的混合气体与过量的Na2O2充分反应后,固体质量增加了3.6 g,再将反应后剩余固体冷却后加入含有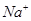 、
、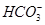 、
、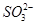 、
、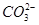 等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是 ( )
等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是 ( )
A.原混合气体的平均摩尔质量为23.2 g/mol
B.混合气体与Na2O2反应过程中电子转移的物质的量为0.25 mol
C.溶液中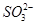 的物质的量浓度基本保持不变
的物质的量浓度基本保持不变
D.溶液中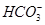 的物质的量浓度减小,
的物质的量浓度减小,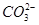 的物质的量浓度增大,但是
的物质的量浓度增大,但是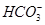 和
和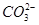 的物质的量浓度之和基本保持不变
的物质的量浓度之和基本保持不变
参考答案:A
本题解析:A项:设混合物中CO2和H2O的物质的量分别为m、n
则44m+18n=11.6①
1mol的CO2和1mol的H2O与Na2O2反应,固体质量分别增加(44-16)=28g、(18-16)=2g
所以28m+2n=3.6②
合并①②
解得m=0.1mol? n=0.4mol
M(平均)=m(总)/n(总)=11.6g/(0.1mol+0.4mol)= 23.2 g/mol。A正确。
B项:2CO2 + 2Na2O2 = 2Na2CO3 + O2①,2Na2O2+2H2O="==4NaOH+" O2↑②,①中转移电子0.1mol,②中转移电子0.4mol,总转移电子书为0.5mol。B错误。
C、D项:剩余固体加入到溶液中,OH-和HCO3-发生反应,OH-+ HCO3-=CO32-+H2O③,溶液中HCO3-浓度减少,CO32-浓度增加来源2个方面,剩余固体Na2CO3中的和反应③的,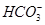 和
和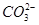 的物质的量浓度之和会增大。
的物质的量浓度之和会增大。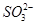 水解方程式为,
水解方程式为,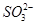 +H20
+H20 HSO32-+OH-④,剩余固体NaOH加入到溶液中会有大量的OH-,反应④会逆向移动,
HSO32-+OH-④,剩余固体NaOH加入到溶液中会有大量的OH-,反应④会逆向移动,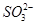 浓度会增大。C、D错误。故选A。
浓度会增大。C、D错误。故选A。
点评:考查的内容不多但繁琐,过氧化钠的性质,水解反应及其移动都是常考的知识点。
本题难度:简单
3、选择题 在Cl2+2Fe2+=2Cl-+2Fe3+的离子反应中,Fe2+代表的化合物不可以是(?)
①Fe(OH)2?②FeCl2?③FeSO4?④FeCO3
A.①④
B.①③
C.①③④
D.②
参考答案:A
本题解析:离子反应中可以拆成离子的是可溶于水的酸碱盐类,不溶解的不能拆成离子,①Fe(OH)2和④FeCO3都不溶解,Fe2+代表的化合物不可以是①④。选A.
本题难度:简单
4、填空题 有A、B、C、D四种可溶性离子化合物,它们的阳离子是Ag+、Na+、Mg2+、Cu2+,阴离子是Cl-、OH-、NO3-、SO42-(每种离子只能用一次)
现将溶液两两混合,记录现象如下:
A+B→白色沉淀?;B+?D→白色沉淀;C+D→蓝色沉淀
则A、B、C、D的化学式分别是_________、__________、___________、_________。
参考答案:AgNO3 ;MgCl2 ;CuSO4 ;NaOH
本题解析:
本题难度:一般
5、填空题 (10分)有一透明溶液,可能含有 等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
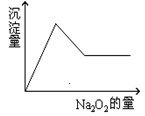
试推断:原溶液中一定含有?;一定没有?,可能含?,为了进一步确定可能含有的离子,应增加的实验操作为?,现象为?。
参考答案:Al3+、Mg2+? Fe3+、Cu2+、NH4+? K+
用洁净的铂丝蘸取待测液,在酒精灯上灼烧?火焰呈紫色
本题解析:加入Na2O2粉末只有无色无味的气体放出,说明没有NH4+。同时析出白色沉淀,则一定没有Fe3+和Cu2+。根据图像可知,生成的沉淀先增加,然后减少,最后不再发生变化,说明一定含有Al3+和Mg2+,最后生成的沉淀是氢氧化镁。钾离子无法确定,要进一步确定钾离子,可用通过焰色反应。
本题难度:一般