微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
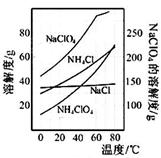
1、选择题 甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是

A.脱氢反应的△H<0
B.600K时,Y点甲醇的υ(正) <υ(逆)
C.从Y点到Z点可通过增大压强
D.在t?1K时,该反应的平衡常数为8.1mol・L-1
参考答案:BD
本题解析:A中由图像可以看出随着温度升高甲醛平衡转化率升高,说明脱氢反应是吸热反应,故A错误;B中600K时由图像可以看出,Y点所对应的转化率比平衡转化率高,说明此时反应向逆反应方向进行,故甲醇的υ(正) <υ(逆),正确;D中由图像看出转化率为0.9,利用三段法解得:设形如时甲醇的物质的量为1mol,则K=0.9*0.9/0.1=8.1
本题难度:一般
2、填空题 已知在某密闭容器中进行的反应a A (g)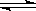 ?b B (g)+ c C (g),(其中a、 b、c分别为方程式中的物质计量数),某物理量Y随时间(t)变化的情况如右图所示(X1、X2表示不同温度或压强),请回答下列问题:
?b B (g)+ c C (g),(其中a、 b、c分别为方程式中的物质计量数),某物理量Y随时间(t)变化的情况如右图所示(X1、X2表示不同温度或压强),请回答下列问题:
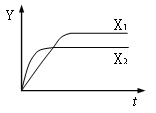
(1)当X1、X2分别表示不同的温度状况时,Y可代表生成物C在平衡时混合物中的质量分数,则该反应的正反应是?反应(填“放热”或“吸热”);
(2)当X1、X2分别表示不同的压强状况时,Y可代表反应物A的转化率,则X1?X2(选填“>”或“<”或“=”);a、 b 、c三者之间的关系为a? (b+c)(填“>”或“<”或“=”)
(3)将 4mol A、3mol B、2mol C充入该反应容器中,在温度为T,压强为P的条件下达平衡后,测得A、B、C的物质的量分别是2mol A、5mol B、3mol C,则a、b、c的最简整数比为???;此时A的转化率为?。若将最初充入该反应容器中的各物质的物质的量变为5mol A、2mol B、1.5mol C,也在温度为T,压强为P的条件下建立平衡,此时容器中的C在混合气体中的体积分数为30%,则此时A的转化率为?。
(4)将 4mol A、3mol B、2mol C充入该反应容器中并达平衡,下列措施能提高物质B在平衡混合气体中体积分数的是?(填写序号)
①增加B的物质的量?②加入合适的催化剂
③增加A的物质的量?④降低温度
参考答案:(1)放热(2分)
(2)<(2分)?<(2分)
(3)2∶2∶1 (2分)? 50% (2分)? 60%(3分)
(4)①④(2分)
本题解析:(1)由图像可知,先拐先平温度高,X2温度大于X1,但温度高时,生成物C在平衡时混合物中的质量分数减小,所以,该反应的正反应是放热反应。
(2)先拐先平压强大,X1 < X2,但压强增大时A 的转化率减小,即增大压强,平衡左移,所以,a <(b+c)
(3)根据可逆反应三步走计算a、b、c的最简整数比为2∶2∶1,此时A的转化率为50%
第二种情况A的转化率为60%
(4)能提高物质B在平衡混合气体中体积分数的是①④。②不能,因为催化剂只改变反应速率,不影响平衡移动。③不能,增加A的物质的量,平衡右移,B 的转化率增大,B在平衡混合气体中体积分数减小。
本题难度:一般
3、计算题 (4分)在带有活塞的密闭容器中压入5molH2和5molN2,在某温度下经反应生成2molNH3,若此时容器的压强不变,则容器体积是反应前的多少倍?
参考答案:N2?+? 3H2 2NH3
2NH3
起始量(mol)? 5? 5? 0
转化量(mol)? 1? 3? 2
某时刻(mol)? 4? 2? 2
因为等温等压时体积之比是相应的物质的量之比容器体积是反应前的(4+2+2)÷10=0.8倍。
本题解析:考查可逆反应的有关计算。
本题难度:一般
4、填空题 (4分)在一密闭容器中,发生可逆反应
aA(g)+bB(g) cC(g)+dD(g)
cC(g)+dD(g)
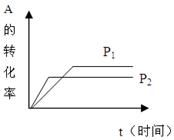
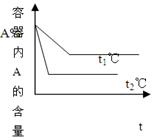
试据图回答:
(1)压强P1?P2,a+b?c+d?(填<、>、=)
(2)温度t1℃比t2℃?(填高或低),正方向为?反应。(填放热或吸热)
参考答案:
(1)压强P1< P2, a+b < c+d
(2)_低__ 正方向为吸热反应 (每空1分)
本题解析:由图一知道,在P2下比在P1下先达到平衡拐点,因此知P1< P2,而在P2条件下A的转化率又比P1条件下的低,因此知a+b < c+d;由图二知道,t2℃比在t1℃温度下先达到平衡,说明t1℃比t2℃低,而在t2℃温度下A的含量又比t1℃温度下的低,说明温度越高,平衡向正反应方向进行,因此正反应为吸热反应。
点评:化学平衡类型的题目经常与图像相结合,关键在于如何分析图像,需要抓住图像中几个关键因素,即起点,拐点和曲线的变化趋势。
本题难度:一般
5、选择题 在3?L容积不变的容器中,发生?N2?+?3H2?==?2NH3的反应。现通入10 mol?H2和10?mol?N2?,?用H2表示的反应速率为0.3 mol/(L・s)?,则10?s末容器中N2的物质的量是
A.7 mol
B.5 mol
C.4 mol
D.1 mol
参考答案:A
本题解析:根据速率之比是相应的化学计量数之比可知,在这段时间内用N2表示的反应速率为0.1 mol/(L・s) ,所以氮气的浓度减少了1 mol/L,物质的量为3 mol,所以10 s末容器中N2的物质的量是10 mol-3 mol=7 mol。答案是A。
本题难度:简单