��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������CO2����ͨ��KOH��Ba(OH)2��KAlO2�Ļ����Һ�У����ɳ�����ͨ��CO2������Ĺ�ϵ�ɱ�ʾΪ?
[? ]
A.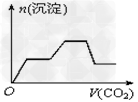
B.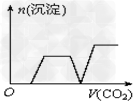
C.
D.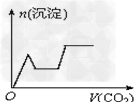
�ο��𰸣�A
���������
�����Ѷȣ�һ��
2��ѡ���� ij��ɫ��Һ�У����ܴ����������������
A.Na+��K+��HCO3-��OH-
B.Na+��H+��SiO32-��CO32-
C.MnO4-��K+��Cl-��H+��SO42-
D.Na+��SiO32-��OH-��Cl-
�ο��𰸣�D
���������������������Ӽ����������ѧ��Ӧ�����ܴ������棬��֮���Դ������档A��HCO3-��OH-���ܴ������棻B��H+��SiO32-��CO32-���ܴ������棻C��MnO4-���Ϻ�ɫ�����ܴ������棬��ѡD��
���㣺�������ӹ���������ж�
�����������Ǹ߿��еĸ�Ƶ�⣬�����е��Ѷȵ����⣬������ؿ���ѧ����������������Ҫ��ȷ���Ӳ��ܴ��������һ�����������1���ܷ������ֽⷴӦ������֮�䣻��2�������������������֮�䣻��3���ܷ���������ԭ��Ӧ������֮�䣻��5���ܷ�����Ϸ�Ӧ������֮�䣨�� Fe3+�� SCN-����������ӹ�������ʱ��Ӧ��ע����Ŀ����������������Ŀ������������һ���У���1����Һ������ԣ��ݴ����ж���Һ���Ƿ��д����� H+��OH-����2����Һ����ɫ������ɫʱ���ų� Cu2+�� Fe2+��Fe3+��MnO4-����ɫ���ӵĴ��ڣ���3����Һ�ľ��巴Ӧ�������硰������ԭ��Ӧ�������������۲�������������4���ǡ����ܡ����棬���ǡ�һ��������ȡ�
�����Ѷȣ�һ��
3��ѡ���� ��ͬ�����£���ͬŨ�ȵ�NH4Cl��Һ��NH3��H2O��Һ�ĵ�������
A.ǰ�ߴ�
B.���ߴ�
C.���
D.��ȷ��
�ο��𰸣�A
���������NH4Cl����Һ����ȫ���룬NH4��H2O����Һ�в��ֵ��룬����Ũ����ͬʱ��NH4Cl��Һ�е�����Ũ�ȴ���NH3��H2O��Һ�е�����Ũ�ȣ�����ǰ�ߵ�������ǿ��
�����Ѷȣ���
4��ѡ���� ����NaOH��Һ��������Һ������������Ŀ����٣�������
A��CO32-?
B��Fe3+
C��SO42-
D��K+
�ο��𰸣�A��̼������Ӻ����������е��������Լ����������Ӿ�����Ӧ��̼���������Ŀ���䣬��A����
B�������Ӻ�����������Һ�е����������ӻ������������������������Ի���٣���B��ȷ��
C������������������е��������Լ����������Ӿ�����Ӧ�������������Ŀ���䣬��C����
D�������Ӻ����������е��������Լ����������Ӿ�����Ӧ����������Ŀ���䣬��D����
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� �������ӷ���ʽ��д��ȷ����
A.��������Һ�м������������������Һ��Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+AlO2-+2H2O
B.̼������Һ��ͨ������������̼���壺CO32-+CO2+H2O�THCO3-
C.������ˮ��Һ��ͨ������CO2��2CH3COO-+CO2+H2O��2CH3COOH+CO2-3
D.���������Ũ�ȵ�Ca��HCO3��2��Һ��NaOH��Һ��ϣ�Ca2++2HCO3-+2OH-��CaCO3+CO32-+2H2O
�ο��𰸣�AB
���������������A��������ȫ��Ӧ����Ӧ�������ᱵ��ƫ����ء�ˮ��
B����Ӧ����̼�����ƣ�
C����������ѧ��Ӧ��
D�������ʵ�����Ӧ������̼�����ơ�ˮ��̼��ƣ�
���A����������Һ�м������������������Һ�����ӷ�ӦΪAl3++2SO42-+2Ba2++4OH-�T2BaSO4��+AlO2-+2H2O����A��ȷ��
B��̼������Һ��ͨ������������̼��������ӷ�ӦΪCO32-+CO2+H2O�THCO3-����B��ȷ��
C����������ѧ��Ӧ��������д���ӷ�Ӧ����C����
D�����������Ũ�ȵ�Ca��HCO3��2��Һ��NaOH��Һ��ϵ����ӷ�ӦΪCa2++HCO3-+OH-�TCaCO3+H2O����D����
��ѡAB��
���������⿼�����ӷ�Ӧ����ʽ����д��ע�����ٵ�������ȫ��Ӧ����ȷ�����Ļ�ѧ��Ӧ���ɽ��ѡ��CΪ�״��㣬��Ŀ�ѶȲ���
�����Ѷȣ���