微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 图为相互串联的甲、乙两电解池.试回答:
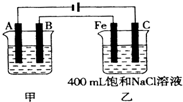
(1)若甲电解池利用电解原理在铁上镀银,则A是 (填电极材料),电极反应式 ;B(要求同A)是 ,电极反应式 ;应选用的电解质溶液是 。
(2)乙电解池中若滴入少量酚酞试液,开始电解一段时间,铁极附近呈 ,C极附近呈 。
(3)若甲电解池阴极增重4.32g,则乙槽中阳极上放出的气体在标准状况下的体积是 。
(4)若乙电解池中剩余溶液仍为400mL,则电解后所得溶液中新生成溶质的物质的量浓度为 mol?L-1,溶液的pH等于 。
参考答案:(1)铁、阴极,Ag++e-
本题解析:
本题难度:一般
2、选择题 1L溶液中含有下列离子,用Pt电极电解该溶液,当电路中有3mol?e-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是( )
| 离子 | Cu2+ | Al3+ | NO3- | Cl-
物质的量浓度(mol/L)
1
1
a
1
|
A.电解后溶液的pH=0
B.a=3
C.阳极生成1.5molCl2
D.阴极析出的金属是铜和铝
参考答案:依据电解过程中存在电子守恒,结合电极反应计算分析产物,用Pt电极电解该溶液,当电路中有3mol e-通过时
阳极电极反应为:2Cl--2e-=Cl2↑;
?1mol?1mol?1mol?
? 4OH--4e-=2H2O+O2↑
?2mol?2mol? 1mol?
阴极电极反应为:Cu2++2e-=Cu
?1mol?2mol 1mol
? ?2H++2e-=H2↑
? 1mol 1mol 0.5mol
A、电解后溶液PH计算,依据两电极上的反应计算,阳极减少2mol氢氧根离子,同时阴极上减少1mol氢离子,综合计算分析得到溶液中增加氢离子物质的量为1mol,氢离子浓度为1mol/L,pH=0,故A正确;
B、依据溶液中电荷守恒计算忽略氢离子和氢氧根离子浓度:2c(Cu2+)+3c(Al3+)=c(Cl-)+c(NO3-),计算得到c(NO3-)=4mol/L,故B错误;
C、依据电极反应电子守恒可知阳极生成1molCl2,故C错误;
D、阴极析出的金属是铜,无金属铝析出,故D错误;
故选A.
本题解析:
本题难度:简单
3、选择题 利用如图所示装置模拟电解原理在工业生产上的应用.下列说法正确的是( )
A.氯碱工业中,X电极上反应式是4OH-4e-=2H2O+O2↑
B.电解精炼铜时,Z溶液中的铜离子浓度不变
C.在铁片上镀铜时,Y是纯铜
D.制取金属镁时,Z是熔融的氯化镁
