��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����йؾ�������������ȷ����
[? ]
A.�����Ǿ������С�Ľṹ�ظ���Ԫ
B.��ͬ�ľ����о����Ĵ�С����״����ͬ
C.�����е��κ�һ�����Ӷ����ڸþ���
D.��֪��������ɾͿ���֪��������
�ο��𰸣�AD
���������
�����Ѷȣ���
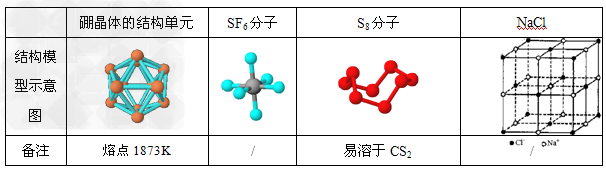
2��ѡ���� �۲�����ģ�Ͳ�����й���Ϣ���ж��й�˵����ȷ����
[? ]
A�������������Ӿ��壬��ṹ��ԪB12�к���30��B-B������20����������
B��SF6���ɼ��Լ����ɵķǼ��Է���
C����̬��S8����ԭ�Ӿ���?
D��NaCl�ۻ�������ˮ���ܲ��������ƶ������ӣ����ƻ�����ͬ��������
�ο��𰸣�BD
���������
�����Ѷȣ�һ��
3��ѡ����
A��2��3
B��1��3
C��1��1
D��1��2
�ο��𰸣�A
�����������ʯī�ľ���ṹ��֪��ÿ��̼ԭ��Ϊ�����������ι��ã�ÿ����������ռ�и�̼ԭ�ӵ�1/3����ˣ�ÿ����������ռ��̼ԭ����Ϊ6��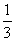 ����������ÿ��C��C����Ϊÿ���������εıߣ�ÿ����Ϊ2���������ι��ã�ÿ����������ռ�и�C��C����
����������ÿ��C��C����Ϊÿ���������εıߣ�ÿ����Ϊ2���������ι��ã�ÿ����������ռ�и�C��C����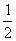 ����ÿ����������ռ��C��C����ĿΪ6��
����ÿ����������ռ��C��C����ĿΪ6��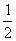 =3����ѡ��A����
=3����ѡ��A����
�����Ѷȣ�һ��
4������� ?����ѧ�D�Dѡ�����ʽṹ�����ʡ���15�֣�
��A��B��C��D��E����Ԫ�ء��������Ϣ���£�

��ش��������⡣
(1) д��EԪ��ԭ�ӻ�̬ʱ�ĵ����Ų�ʽ__________________��
(2) CԪ�صĵ�һ�����ܱ���Ԫ���ĵ�һ������ ______ ______ (���С��)��
(3) CA3������Cԭ�ӵ��ӻ����������____________��
(4) A��C��E����Ԫ�ؿ��γ�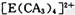 �����ӣ����д��ڵĻ�ѧ�������� ______ (����ţ���
�����ӣ����д��ڵĻ�ѧ�������� ______ (����ţ���
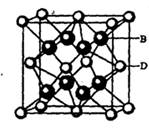
����λ�� �ڽ������ۼ��Թ��ۼ��ܷǼ��Թ��ۼ������Ӽ� �����
��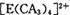 ���жԳƵĿռ乹�ͣ��ҵ�
���жԳƵĿռ乹�ͣ��ҵ�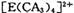 �е�����CA3������Cl-ȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ����
�е�����CA3������Cl-ȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ���� �Ŀռ乹��Ϊ ____________ (�����)��
�Ŀռ乹��Ϊ ____________ (�����)��
a.ƽ��������b.��������c.������ ?d. V��
(5) B��D���γ����ӻ�����,�侧���ṹ����ͼ��ʾ������D���ӵ���λ��Ϊ_____,���þ�����ܶ�Ϊag ? cm��3,��þ����������______cm-3(д������ʽ����)��
�ο��𰸣�(1) 1s2 2s2 2p6 3s2 3p6 3d10 4s1��[Ar] 3d10 4s1(2)��(3)sp3(4)�٢ۣ�a (5) 8��(4��78/ NAa) cm3.
������������⿼�����ʽṹ�����ʵ��й�֪ʶ������A��B��C��D��E����Ԫ�ص������Ϣ�������ƶϳ�A��B��C��D��E����Ԫ�طֱ���H��F��N��Ca��Cu��(1) Cu�Ļ�̬�����Ų�ʽΪ1s2 2s2 2p6 3s2 3p6 3d10 4s1��[Ar] 3d10 4s1(2)����N��P����������ع����������ͣ���һ���������ߣ���NԪ�صĵ�һ�����ܱ���Ԫ���ĵ�һ�����ܴ�(3)NH3�е�ԭ���������5�����ӣ������3�����ӣ���8���ӽṹ�����ݼ۲���ӶԻ������ۣ��ĶԵ��ӵ��Ų���ʽΪ�����幹�Σ������ӻ�������ۣ�ӦΪsp3�ӻ���(4)[Cu(NH3)4]2+��Cu��NH3ͨ����λ����ϣ�NH3��N��Hͨ�����Թ��ۼ���ϡ�����[Cu(NH3)4]2+�ǶԳƽṹ��������NH3������Cl-ȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ�����[Cu(NH3)4]2+����������ṹ������NH3������Cl-ȡ��ʱ���ܵõ�һ�ֲ���������⣬��[Cu(NH3)4]2+��ƽ�������νṹ��(5)F��Ca�γ�CaF2���Ӿ���ṹ���Կ����������ƽṹ�ֳ�өʯ�ͽṹ�������ᾧϵ�����������ṹ����������AB2�����Ӿ��塣����������A(Ca2+)�������ܶѻ���������B(F-)������������϶�У�������������Խ��ߵ�1/4��3/4�������������ӵ���λ���ֱ�Ϊ4��8�����������Ӱ뾶��R2+/R->0.732��������һ�������ƾ�������4�������ơ��þ�����ܶ�Ϊag ? cm��3����þ����������(4��78/ NAa) cm3��
�����Ѷȣ�һ��
5������� ͼΪ�ס��ҡ����������Ӿ���ľ�������������С���ظ���Ԫ���ṹ���ڼ�����X���ھ������ģ�����A���ھ������ġ�����֪��������X��Y�ĸ�������_____���Ҿ�����A��B�ĸ�������______����Ʒ���һ���������и�C���ӣ���_______��D���ӡ�
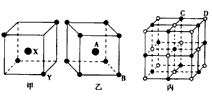
�ο��𰸣�2:1��1:1��4
���������
�����Ѷȣ�һ��