微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在用Zn片、Cu片和稀硫酸组成的电池装置中,经过一段时间工作后,下列说法中正确的是( )
A.锌片是正极,铜片上有气泡产生
B.电流方向是从锌片经导线流向铜片
C.溶液中的阳离子向正极移动,阴离子向负极移动
D.电解液的pH值逐渐减小
参考答案:A、锌片是负极,铜片上有气泡产生,故A错误;
B、电流方向是从Cu片经导线流向Zn片,故B错误;
C、溶液中的阳离子向正极移动,阴离子向负极移动,故C正确;
D、因氢离子参加反应生成氢气,氢离子减少,则电解液的pH增大,故D错误;
故选C.
本题解析:
本题难度:一般
2、实验题 Al-Mg在不同的电解质溶液中分别构成原电池A、B。如下图所示:
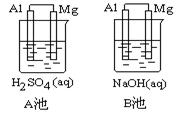
指出各池中的负极材料并写出其电极方程式。
①负极材料:
A池?,B池?。
②电极反应式:
A池:正极?,负极?。
B池:正极?,负极?。
③从构成原电池的几个组成部分来看,判断原电池的负极,除了要考虑金属的活泼性外,还要考虑?
参考答案:(1)①A池镁作负极材料,B池中铝作负极材料 ②A池:正极2H++2e-=H2↑,负极Mg-2e-=Mg2+;B池:正极6H2O+6e-=3H2↑+6OH-,负极2Al-6e-+8OH-=2AlO2-+4H2O;③池中能够发生的氧化还原反应
本题解析:在A池中可与稀硫酸发生化学反应的有镁和铝Mg+H2SO4=MgSO4+H2↑;2Al+3H2SO4=Al2(SO4)3+3H2↑由于镁的金属活泼性大于铝,所以该电池中的化学反应为Mg+H2SO4=MgSO4+H2↑,镁失电子作电池负极,铝作正极。在B池中能发生的化学反应只有铝和碱的反应,即2Al+2NaOH+2H2O=2NaAlO2+3O2↑,所以该电池中铝失电子作电池负极,而镁只能作正极。
本题难度:简单
3、实验题 (8分)某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
方案Ⅰ:有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为 。
方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性。试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式。

正极反应式: ;负极反应式: 。
若该电池中有0.1mol的电子转移,请问消耗 克Fe
方案Ⅲ.结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同): __________________,用离子方程式表示其反应原理:______________
参考答案:(共8分)
方案Ⅰ:Fe+2H+=Fe2++H2↑(1分)
方案Ⅱ:(画装置图完全正确2分,合理的均给分)

2H++2e- =H2↑(1分) Fe-2e-=Fe2+(1分) 2.8 g
方案Ⅲ:把铁片插入CuSO4溶液中,一段时间后,观察铁片表面是否生成红色物质(1分)Fe+Cu2+ = Cu+Fe2+(1分)
本题解析:金属的活动性有多种验证方法。例如与水和酸置换氢气的能力;最高价氧化物水化物的碱性强弱;原电池原理;电解原理的应用、金属之间的置换等等。
本题难度:一般
4、填空题 氢氧燃料电池是最常见的燃料电池,该电池在正极通入氧气,在负极通入氢气,而电解质溶液通常是KOH溶液。
(1)请写出氢氧燃料电池的正极反应方程式。
(2)氢氧燃料电池有何优点?
参考答案:1/2O2 + H2O + 2e- = 2OH-(3分)?无污染,环保(2分)
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。所以在氢氧燃料电池中,氢气在负极通入,氧气在正极通入。由于电解质是氢氧化钾,所以正极电极反应式是1/2O2 + H2O + 2e- = 2OH-;由于氢气燃烧的生成物是水,对环境没有污染,属于环保电池。
点评:在书写氢氧燃料电池时,除了要注意判断正负极之外,在书写电极反应式时,还要注意电解质溶液的酸碱性。
本题难度:一般
5、实验题 (16分)MnO2是重要无机材料,某学习小组设计了将粗MnO2(含有较多的MnO、 MnCO3和Fe2O3,其中Fe2O3质量百分含量为10%)样品转化为纯MnO2实验,其流程如下:
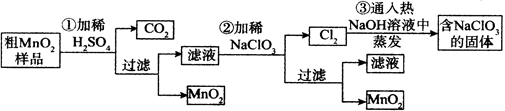
(已知:氧化性强弱顺序: ClO3-> MnO2 > Fe3+)
(1)铝与二氧化锰在高温下发生铝热反应,相关反应的化学方程式为: 。
(2)第②步反应离子方程式为: 。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、玻璃棒、 、 ;
第③步蒸发得到的固体中除了含有NaClO3和NaOH外,还一定含有 (写化学式)。
(4)MnO2是碱性锌锰电池的正极材料,则碱性锌锰电池放电时,正极的电极反应式是: 。
(5)若粗MnO2样品的质量为28.2g,第①步反应后,经过滤得到17.4g MnO2,并收集到448mL CO2(标准状况下),则在第②步反应中至少需要 mol NaClO3才能将Mn2+完全转化为MnO2。
参考答案:(1)2Al+ 3MnO2 3Mn + 2Al2O3(3分)
3Mn + 2Al2O3(3分)
(2)5Mn2+ + 2ClO3- +4H2O =" 5" MnO2↓ + Cl2↑ + 8H+(3分)
(3)酒精灯 蒸发皿(2分,各1分)NaCl(2分)
(4)MnO2 + e- + H2O =" MnO(OH)" + OH-或2MnO2 + 2e- + H2O = Mn2O3 + OH-(3分)
(5)0.04(3分)
本题解析:(1)铝与二氧化锰在高温下发生铝热反应,产生氧化铝和锰,反应的化学方程式为:2Al+ 3MnO2 3Mn + 2Al2O3;(2)粗二氧化锰中含有MnO、MnCO3和Fe2O3,当加入稀硫酸时,MnO、MnCO3和Fe2O3会发生反应转化为可溶性的MnSO4、Fe2(SO4)3,将MnO2过滤除去,然后向溶液中加入稀NaClO3溶液, Mn2+被氧化为MnO2,根据电子守恒、原子守恒及电荷守恒可得第②步反应反应离子方程式为:5Mn2+ + 2ClO3- +4H2O =" 5" MnO2↓ + Cl2↑ + 8H+;(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、玻璃棒、酒精灯 蒸发皿;第③步发生的是氧化还原反应,Cl2失去电子被氧化为NaClO3,则被还原得到的是NaCl,因此蒸发得到的固体中除了含有NaClO3和过量的未反应的NaOH外,还一定含有NaCl;(4)MnO2是碱性锌锰电池的正极材料,则碱性锌锰电池放电时,正极上发生还原反应,该电极的电极反应式是MnO2 + e- + H2O =" MnO(OH)" + OH-;(5)n(CO2)=0.448L÷22.4L/mol=0.02mol;则根据C元素守恒可得n(MnCO3)= n(CO2)= 0.02mol;若剩余的物质完全是MnO,则其物质的量是n(MnO)=(28.2g―17.4g―0.02mol×115g/mol―28.2g×10%)÷71g/mol=0.08mol, 溶液中含有的Mn2+的物质的量是n(Mn2+)=" n(MnO)+" n(MnCO3)= 0.08mol+0.02mol=0.1mol则根据方程式5Mn2+ + 2ClO3- +4H2O = 5MnO2↓ + Cl2↑ + 8H+可知消耗NaClO3的物质的量是n(NaClO3)="2/5" n(MnO)= 2/5×0.1mol=0.04mol, 即在第②步反应中至少需要0.04mol mol NaClO3才能将Mn2+完全转化为MnO2。
3Mn + 2Al2O3;(2)粗二氧化锰中含有MnO、MnCO3和Fe2O3,当加入稀硫酸时,MnO、MnCO3和Fe2O3会发生反应转化为可溶性的MnSO4、Fe2(SO4)3,将MnO2过滤除去,然后向溶液中加入稀NaClO3溶液, Mn2+被氧化为MnO2,根据电子守恒、原子守恒及电荷守恒可得第②步反应反应离子方程式为:5Mn2+ + 2ClO3- +4H2O =" 5" MnO2↓ + Cl2↑ + 8H+;(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、玻璃棒、酒精灯 蒸发皿;第③步发生的是氧化还原反应,Cl2失去电子被氧化为NaClO3,则被还原得到的是NaCl,因此蒸发得到的固体中除了含有NaClO3和过量的未反应的NaOH外,还一定含有NaCl;(4)MnO2是碱性锌锰电池的正极材料,则碱性锌锰电池放电时,正极上发生还原反应,该电极的电极反应式是MnO2 + e- + H2O =" MnO(OH)" + OH-;(5)n(CO2)=0.448L÷22.4L/mol=0.02mol;则根据C元素守恒可得n(MnCO3)= n(CO2)= 0.02mol;若剩余的物质完全是MnO,则其物质的量是n(MnO)=(28.2g―17.4g―0.02mol×115g/mol―28.2g×10%)÷71g/mol=0.08mol, 溶液中含有的Mn2+的物质的量是n(Mn2+)=" n(MnO)+" n(MnCO3)= 0.08mol+0.02mol=0.1mol则根据方程式5Mn2+ + 2ClO3- +4H2O = 5MnO2↓ + Cl2↑ + 8H+可知消耗NaClO3的物质的量是n(NaClO3)="2/5" n(MnO)= 2/5×0.1mol=0.04mol, 即在第②步反应中至少需要0.04mol mol NaClO3才能将Mn2+完全转化为MnO2。
考点:考查化学反应方程式和离子方程式的书写、混合物分离方法的操作方法及仪器的使用、原电池电极反应式的书写、关于化学反应方程式的计算的知识。
本题难度:一般