��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������RO3-���������������������NO3-�ĵ�������10��������˵����ȷ����
[? ]
A��Rԭ�ӵĵ��Ӳ�����N�ĵ��Ӳ�����2
B��RO3-��R�Ļ��ϼ���NO3-�е�N�Ļ��ϼ۲����
C��RO3-���ܱ���ԭ��Ҳ�ܱ�����
D��R��NΪͬ��Ԫ��
2��ѡ���� ����Ԫ������±��Ԫ�ص���
[? ]
A��F
B��P
C��He
D��Li
3������� ��ͼ��Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���д���пո�

��1������10��Ԫ���У��ǽ�������ǿ����______������ţ���
��2��Ԫ�آٵ����������ṹʽΪ______��Ԫ�آ�����γɵ�18e-������ĵ���ʽ______��
��3���ڡ��ᡢ������Ԫ���γɵĻ�����M��ԭ�Ӹ�����Ϊ3��4��2����������Ϊ42��M�к��еĻ�ѧ��������______��
��4���Ƚ�Ԫ�آޢߢ��γɵ���̬�⻯����ȶ��ԣ�______��______��______���û�ѧʽ��ʾ��
��5��Ԫ�آݵ�������������������Һ��Ӧ�����ӷ���ʽ______��
��6��Ԫ�آ���ݵĵ���������������Һ�й���ԭ��أ���������ķ����ڻ���ԭ���װ�ü�ͼ�����ԭ��صĵ缫���ϼ���������
4���ƶ��� �±���Ԫ�����ڱ���һ���֣�A��B��C��D��E��X�DZ��и���Ԫ����ɵij������ʻ����֪A��B��C��D��E��X������ͼ��ʾת����ϵ������������ͷ�Ӧ������ȥ��
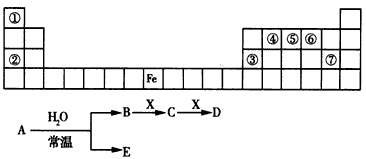
(1)����EΪ�������A��ˮ��Ӧ�Ļ�ѧ����ʽΪ___________________��
�ڵ�X�Ǽ�������Һ��C��������22������ʱ��C�ĵ���ʽΪ___________��������д����ŷ�C���ܵ��µĺ����_________________��
�۵�XΪ��������ʱ��X��B��ϡ��Һ��Ӧ����C�����ӷ���ʽΪ________________��
(2)��EΪ���嵥�ʣ�DΪ��ɫ������A�Ļ�ѧʽ������__________��B���еĻ�ѧ������Ϊ_________��
(3)��BΪ���嵥�ʣ�D����ˮ������һ�������·������淴Ӧ������C��һ�ֿ�ȼ�����嵥�ʣ�д���ÿ��淴Ӧ�Ļ�ѧ����ʽ_________________��
5������� ����֪a��b��c��d��eΪ����������Ԫ�أ�����
��a��b��ͬ����Ԫ�أ��������γɶ�����̬�����
��a��c��ͬ����Ԫ�أ��������γ�������̬�����
��a��d��ͬ����Ԫ�أ��������γ����ֳ��������
��e�ɷֱ��a��b��c��d�γɾ�����ͬ�������Ĺ��ۻ�����ס��ҡ���������
��ش�
��1��aԪ��Ϊ______���ķ���ʽΪ______�����ĵ���ʽΪ______��
��2��������һ�ֻ���Ԫ���γɵ����ʿ���ˮ����������ԭ��Ӧ���������û���Ӧ��д��һ������Ҫ��Ļ�ѧ��Ӧ����ʽ��______��
��̼��̼�Ļ����������������������е�Ӧ�÷dz��㷺������ �����������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ������ʽ��
��1������ȼ��ʱ�ų��������ȣ�����Ϊ��ԴӦ������������������
��֪��2CH4��g��+3O2��g���T2CO��g��+4H2O��l������H1=-1214.6kJ/mol��
��CO2?��g���TCO?��g��+
O2��g������H2=+283kJ/mol
�����ȼ���ȵ��Ȼ�ѧ����ʽΪ______��
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g�����õ������������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min
H2O
CO
CO2
CO
1
650
2
4
1.6
2.4
5
2
900
1
2
0.4
1.6
3
3
900
a
b
c
d
t
|
��ʵ��1�У���v��H2����ʾ��ƽ����Ӧ����Ϊ��______?mol/L?min��
�ڸ÷�Ӧ������ӦΪ______��������š����ȷ�Ӧ��
����Ҫʹʵ��3�ﵽƽ��״̬ʱ�����ʵ����������ʵ��2�ֱ���ȣ���a��bӦ����Ĺ�ϵ��______���ú�a��b��ʾ����