微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 漂白粉在社会生活、工业生产中用途广泛,漂白粉除了具有漂白作用外,还能杀菌消毒。2003年抗“非典”期间,各商场漂白粉及其他漂白产品曾一度脱销。1998年,我国长江流域和松花江流域都发生了百年不遇的特大洪水。灾区人们的饮用水,必须用漂白粉等药品消毒后才能饮用,以防传染病发生,但瓶装漂白粉久置空气中会呈稀粥状而失效。试用化学方程式表示漂白粉在空气中易失效的原因是①________________;②__________________。
参考答案:①Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO②2HClO 2HCl+O2↑
2HCl+O2↑
本题解析:漂白粉的成分是Ca(ClO)2和CaCl2,而能起漂白作用的是Ca(ClO)2,所以漂白粉的有效成分是Ca(ClO)2,它在空气中失效的化学方程式为:
①Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO
②2HClO 2HCl+O2↑
2HCl+O2↑
所以,漂白粉应密闭保存,避免与空气接触。
本题难度:简单
2、选择题 人们常用的“84”消毒液的主要成分是
[? ]
A.NaCl
B.NaClO
C.双氧水
D.苯酚
参考答案:B
本题解析:
本题难度:简单
3、计算题 用15.8g高锰酸钾氧化密度为1.19g/cm3,质量分数为36.5%的盐酸以制取氯气。反应如下:
2KMnO?4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
求:(1)生成Cl2在标况下的体积;
(2)被KMnO4氧化的盐酸的体积;
(3)反应中转移的电子总数。
参考答案:(1)5.6L(2) ?42ml ?(3)3.01×1023(或0.5NA)
本题解析:
(1)首先计算15.8g高锰酸钾的物质的量为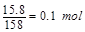
设反应生成的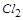 的物质的量为
的物质的量为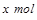 ,则由反应的化学方程式
,则由反应的化学方程式
2KMnO?4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
知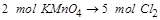
则有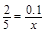 ,解得
,解得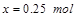
标准状况下产生的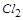 的体积为
的体积为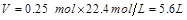
(2)在反应2KMnO?4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,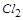 是氧化产物,且
是氧化产物,且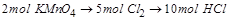
即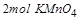 能将
能将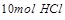 氧化成
氧化成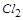
设被氧化的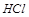 的物质的量为
的物质的量为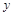 ,则有
,则有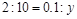 ,解得
,解得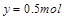
设反应中被氧化的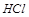 的体积为
的体积为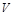 ,则有
,则有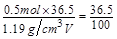
解得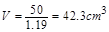 即被氧化的盐酸的体积大约为
即被氧化的盐酸的体积大约为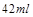
(3)在这个反应中,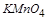 中的
中的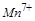 变成了
变成了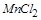 中的
中的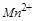 ,反应中每个
,反应中每个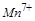 得到了
得到了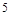 个电子,面参加反应的
个电子,面参加反应的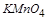 共有
共有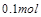 ,所电子转移的总数为
,所电子转移的总数为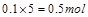 ,即
,即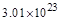 个(或0.5NA)
个(或0.5NA)
本题难度:简单
4、选择题 向盛有氯气的集气瓶中,注入约五分之一的下列液体并轻轻振荡,观察到的现象记录如图所示,判断瓶中注入的液体是(?)
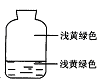
A.AgNO3溶液
B.NaOH溶液
C.水
D.KBr溶液
参考答案:C
本题解析:所得溶液是浅黄绿色的,说明是氯气是水溶液,C正确。硝酸银和氯气反应生成氯化银白色沉淀,A不正确。氯气和氢氧化钠反应,溶液是无色的,且氯气不可能剩余。氯气和溴化钾反应生产物是单质溴,溶液显橙色,D不正确,答案选C。
本题难度:一般
5、选择题 为防止储存 氯气的钢瓶被腐蚀,钢瓶在装Cl2之前必须
氯气的钢瓶被腐蚀,钢瓶在装Cl2之前必须
A.清洗干净
B.冲入惰性气体
C.除去铁锈
D.彻底干燥
参考答案:D
本题解析:略
本题难度:一般