| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《物质的量》高频考点预测(2017年最新版)(六)
参考答案:B 本题解析:略 本题难度:一般 3、填空题 (11分)下图是中学化学的一个重要定量实验过程示意图,回答下列问题: 参考答案:[第(5)小题2分,其余每空1分,共11分] 本题解析:(1)该实验中的一处错误是图①中氢氧化钠易吸潮,应在称量瓶或小烧杯中称量,不能在纸上称量;(2)量筒和容量瓶都是量器,能准确量取溶液的体积。(3)玻璃棒,在实验操作②溶解中起到搅拌作用、在实验操作③转移中起到引流的作用;(4)a.在第②步操作中,有少量液体溅出烧杯外,溶质的物质的量减小,溶液浓度偏小;b.在第③步操作中,容量瓶内本来有少量水对溶液浓度没有影响;c.在第⑤步操作中,若俯视刻度线,溶液的体积偏小,浓度偏大;d.在第⑥步操作中,经振荡、摇均、静置后发现液面低于刻度线,再加蒸馏水至刻度线,溶液体积增大,浓度偏低;(5)标签上应注明溶液的名称及溶液的浓度,4g氢氧化钠配成100ml溶液,浓度为1mol/L。 本题难度:一般 4、选择题 0.5mol氢气在标准状况下所占的体积约是( ) |
参考答案:B
本题解析:标准状况下,气体的摩尔体积是22.4L/mol,所以根据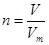 可知,0.5mol氢气在标准状况下所占的体积0.5mol×22.4L/mol=11.2L,答案选B。
可知,0.5mol氢气在标准状况下所占的体积0.5mol×22.4L/mol=11.2L,答案选B。
本题难度:一般
5、选择题 设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L0.5mol・L-1 的(NH4)2SO4溶液中含NH4+数为NA
B.常温常压下,1molCH4中含有4NA个C-H键
C.常温常压下,48g O3含有原子数为2NA(相对原子质量:O 16)
D.标准状况下,22.4LC6H6(苯)的分子数目为NA
参考答案:B
本题解析:由于c?V=n,则(NH4)2SO4的物质的量为0.5mol,虽然(NH4)2SO4==2NH4++SO42―中铵根离子与硫酸铵的系数之比等于物质的量之比,但是少部分铵根离子能水解生成一水合氨,则平衡时溶液中铵根离子小于0.5 mol,故A选项错误;1个甲烷分子含有4个C―H键,则1molCH4中含有4molC―H键,故B选项正确;由于臭氧的相对分子质量为48,m/M=n,则臭氧的物质的量为1mol,臭氧分子是三原子分子,则1molO3含有3mol原子,故C选项错误;苯是液体,不能用V/Vm求其物质的量,故D选项错误。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《化学平衡常.. | |