微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
-->
1、选择题 下列说法正确的是
A.7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.2×6.02×1023
B.标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.0×6.02×1023
C.2.24LSO2与O2混合气体中所含氧原子数为0.2×6.02×1023
D.Vlamol・L-1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023
参考答案:D
本题解析:氯气与NaOH转移电子为;Cl2~e?,7.1g氯气反应转移的电子数为0.1×6.02×1023,A项错;NO与O2反应生成NO2,2 NO2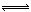 N2O4,分子数减少,所以混合后气体的分子总数<1.0×6.02×1023,B项错;C项没有注明外界条件,2.24LSO2的物质的量不确定;因为Fe3+水解,所以Cl?的数目大于Fe3+数目的3倍,D项正确。
N2O4,分子数减少,所以混合后气体的分子总数<1.0×6.02×1023,B项错;C项没有注明外界条件,2.24LSO2的物质的量不确定;因为Fe3+水解,所以Cl?的数目大于Fe3+数目的3倍,D项正确。
本题难度:一般
2、简答题 向50mL1mol/L的Al2(SO4)3溶液中加入50mLKOH溶液,充分反应得到3.9g沉淀,则KOH溶液的物质的量浓度可能是______或______.
参考答案:1、氢氧化钾不足量,氢氧根全部转化为沉淀.
设KOH溶液的物质的量浓度是xmol/L,
3OH-+Al3+=Al(OH)3↓
3 78g
0.05xmol 3.9g
x=3
2、硫酸铝不足量,先生成沉淀,后沉淀部分溶解.
硫酸铝中Al3+的物质的量为2×1mol/L×0.05L=0.1mol,3.9g沉淀需要Al3+的物质的量为3.9g78g/mol=0.05mol
转变成AlO2-的Al3+的物质的量为0.05mol.
设KOH溶液的物质的量浓度是ymol/L,
3OH-+Al3+=Al(OH)3↓
3mol 78g
0.15mol3.9g
4OH-+Al3+=AlO2-+2H2O
4mol 1mol
0.2mol 0.05mol
所以KOH溶液的物质的量浓度是c=nV=0.15mol+0.2mol0.05L=7mol/L,
故答案为:3mol/L;7mol/L.
本题解析:
本题难度:简单
3、选择题 下列溶液中Cl-浓度与50mL?1mol?L-1?AlCl3溶液中Cl-的物质的量浓度不相等的是( )
A.150mL 1mol?L-1的NaCl溶液
B.75mL 3mol?L-1NH4Cl溶液
C.150mL 3mol?L-1的KCl溶液
D.75mL 1mol?L-1的FeCl3溶液
参考答案:A.150mL1mol?L-1的NaCl溶液中Cl-的物质的量浓度1mol/L,不相等,故A选;
B.75mL3mol?L-1NH4Cl溶液中Cl-的物质的量浓度3mol/L,相等,故B不选;
C.150mL3mol?L-1的KCl溶液中Cl-的物质的量浓度3mol/L,相等,故C不选;
D.75mL1mol?L-1的FeCl3溶液Cl-的物质的量浓度1mol/L×3=3mol/L,相等,故D不选;
故选A.
本题解析:
本题难度:简单
4、选择题 向100g浓度为18mol/L、密度为ρg/mL的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加入水的体积?
A.小于100mL
B.等于100mL
C.大于100mL
D.等于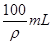
参考答案:A
本题解析:稀释前后溶质的质量不变,设加水的质量为x,
则100g×w1=(100g+x)×w2,
18mol・L-1的浓硫酸加到一定量的水中稀释成9mol・L-1的硫酸,
由c=1000ρw/M
及硫酸的浓度越大,密度越大,
则w1>w2,w1<2w2,
所以(100+x)/100<2,
解得x<100g,
又水的密度约为1g・mL-1,
则加水的体积小于100mL,
故选A.
本题难度:一般
5、选择题 100mL0.3mol・L-1的Na2SO4溶液和50mL 0.1mol・L-1的Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度为
A.0.20mol?L-1
B.0.25mol?L-1
C.0.30mol?L-1
D.0.50mol?L-1