��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ѪҺ�������Ҫ�����ƽ�⣺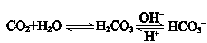 ��ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��c(HCO3��)��c(H2CO3)�仯��ϵ���±���
��ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��c(HCO3��)��c(H2CO3)�仯��ϵ���±���
c(HCO3��) ��c(H2CO3)
| 1.0
| 17.8
| 20.0
| 22.4
|
pH
| 6.10
| 7.35
| 7.40
| 7.45
|
����˵������ȷ����
A����������ѪҺ�У�HCO3����ˮ��̶ȴ��ڵ���̶�
B������ѪҺ���ж�ʱ����ע��NaHCO3��Һ����
C��pH=7.00��ѪҺ�У�c(H2CO3)��c(HCO3��)?
D��pH=7.40��ѪҺ�У�HCO3����ˮ��̶�һ������H2CO3�ĵ���̶�
�ο��𰸣�D
�������������ѪҺpH������7.35��7.45����������ƽ�⣺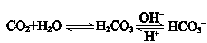
�Ӹ�ƽ����Կ��������������̼���̼�����������ѪҺpHС��7.35ʱ̼���ת����̼�������ʹ���Խ��ͣ�������ѪҺpH����7.45��̼�������ת����̼��������ȡ�
������������ѪҺ�У�HCO3����ˮ��̶ȴ��ڵ���̶ȣ�����ѪҺ���ж�ʱ��ֻҪ����̼��������ɻ��⣬���Կ�ע��NaHCO3��Һ��Ȼ���Ի������ж�����pH��c(HCO3��)��c(H2CO3)�仯��ϵ����
c(HCO3��) ��c(H2CO3)
1.0
17.8
20.0
22.4
pH
6.10
7.35
7.40
7.45
?
���Կ���PH=6.10ʱc(H2CO3)=c(HCO3��) ���˺�����PHֵ������̼�����Ѹ����������pH=7.00��ѪҺ�У�c(H2CO3)��c(HCO3��) ��pH=7.40��ѪҺ�У�c(HCO3��)��c(H2CO3)=20.0
ֻ��˵��ѪҺ�е�HCO3��Զ����H2CO3��������˵��HCO3����ˮ��̶�һ������H2CO3�ĵ���̶ȣ�����D������ѡD��
������ץס��������ƽ�⣺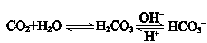 ?��pH��c(HCO3��)��c(H2CO3)�仯��ϵ����������Ϣ��������ѧ���Ը�������ƽ��ķ�����������Ϣ�ķ���������
?��pH��c(HCO3��)��c(H2CO3)�仯��ϵ����������Ϣ��������ѧ���Ը�������ƽ��ķ�����������Ϣ�ķ���������
�����Ѷȣ���
2��ѡ���� ����������Һ�У���pHֵΪ0�������0.1mol/L�������0.01mol/L������������Һ����pHֵΪ11������������Һ����ˮ�������ɵ�c��H����֮������Ϊ
A��0�U1�U12�U11
B��14�U13�U12�U11
C��14�U13�U2�U3
D��1�U10�U100�U1000
�ο��𰸣�D
������������������ˮ�ĵ��룬���Ԣ٢ڢۢ�����ˮ�������ɵ�c��H�����ֱ�Ϊ10��14��10��13��10��12��10��11����c��H����֮������Ϊ1�U10�U100�U1000����ѡD��
�����Ѷȣ���
3������� ��1��AgNO3��ˮ��Һ��?����ᡱ�����С���������ԣ�����ʱ��pH ?7���>������=������<������ʵ����������AgNO3����Һʱ������AgNO3���������ڽ�Ũ�������У�Ȼ����������ˮϡ�͵������Ũ�ȣ���?����ٽ����������ơ�����ˮ�⡣
��2��������ˮ��ҺPH?7 �����>������=������<����ԭ���ǣ������ӷ���ʽ��ʾ����______����AlCl3��Һ���ɣ����գ����õ�����Ҫ���������?��
��3���Ȼ����Һ�еμ�������ˮ������Һ�����ԣ���c(Cl-)??c(NH4��)���>������=������<��������4����25���£�ijŨ��Na2CO3��Һ����ˮ�������c(OH-)=1��10-6 mol/L�������Һ��PHֵΪ?
�ο��𰸣�1���ᣬ pH <7������
��2��PH >7 ��CH3COO- + H2O  ?CH3COOH+OH-��Al2O3
?CH3COOH+OH-��Al2O3
��3��c(Cl-)?=?c(NH4��)��
��4��8
�����������1���У�AgNO3Ϊǿ�������Σ�ˮ�������ԣ�����ʱ��pH<7�����ڽ�Ũ��������Ϊ��������ˮ�⣻��2���У�������Ϊǿ�������Σ�ˮ���ʼ��ԣ�����ʱ��PH >7�������ӷ���ʽ��ʾΪ��CH3COO- + H2O  ?CH3COOH+OH-��AlCl3Ϊǿ�������Σ�ˮ�������ԣ���AlCl3��Һ���ɣ����գ����õ�����Ҫ���������Al2O3����3���У���Һ�����ԣ����ݵ���غ��֪��c(Cl-) ?= c(NH4��)����4��Na2CO3��Һ�̼��ԣ�����25���£���ˮ�������c(OH-)=1��10-6 mol/L������c��H+��=1��10-8 mol/L����PH=8��
?CH3COOH+OH-��AlCl3Ϊǿ�������Σ�ˮ�������ԣ���AlCl3��Һ���ɣ����գ����õ�����Ҫ���������Al2O3����3���У���Һ�����ԣ����ݵ���غ��֪��c(Cl-) ?= c(NH4��)����4��Na2CO3��Һ�̼��ԣ�����25���£���ˮ�������c(OH-)=1��10-6 mol/L������c��H+��=1��10-8 mol/L����PH=8��
���������⿼��������ˮ�⣬����PH���Ǹ߿��ij������ͣ�����Ƚϻ�����ѧ�������ø߷֡�
�����Ѷȣ�һ��
4������� ��4�֣�ˮ�ĵ���ƽ��������ͼ��ʾ��
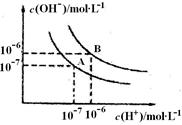
(1)A���ʾ25��ʱˮ����ƽ��ʱ���ӵ�Ũ�ȣ����¶����ߵ�100��ʱ��ˮ�ĵ���ƽ��״̬�䵽B�㣬��100��ʱˮ�����ӻ�Ϊ_____________��
(2) 100��ʱ����10�����ijǿ����Һ��l�����ijǿ����Һ��Ϻ���Һ�����ԣ�����֮ǰ����ǿ���pHa��ǿ���pHb֮��Ӧ����Ĺ�ϵ��______________��
�ο��𰸣���1��10-12?��2��pHa+pHb=13��ÿ��2�֣�
�����������1��ˮ�����ӻ�KW=c��H+��?c��OH-����100��ʱ��KW=c��H+��?c��OH-��=10-6��10-6=10-12����2����ǿ����Һ��pHΪa�����Ϊ10L����Һ��������Ũ��Ϊ10-amol/L��ǿ����Һ��pHΪb�����Ϊ1L����Һ�����������ӵ�Ũ��Ϊ��10b��12mol/L����Ϻ���Һ�����ԣ�����Һ�������ӵ����ʵ����������������ӵ����ʵ�������10-amol/L��10L=10b��12mol/L ��1L�����a+b=13��
�����Ѷȣ�һ��
5��ѡ���� �������¼����Ȼ�ѧ����ʽ����ʾ��̬̼����̬����ȼ��ʱȼ���ȵ���
A.C��s����1/2O2��g��==CO(g) ��H =-110.5 kJ/mol
B.C��s����O2��g��==CO2(g) ��H =-393.5 kJ/mol
C.2H2(g)��O2(g)==2H2O(l)��H =-571.6 kJ/mol
D.H2(g)��1/2O2(g)==H2O(g)��H =-241.8 kJ/mol
�ο��𰸣�B
���������ȼ������ָ��һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų���������A��̼�Dz���ȫȼ�գ�����ȷ�����B��ȷ��C����������1mol������ȷ��D��ˮ���ȶ�״̬����Һ̬������ȷ����ѡB��
�����Ѷȣ�����